Clear Sky Science · it
PDHB attivato da TGFβ promuove il metabolismo mitocondriale del piruvato e contribuisce alla differenziazione dell’endoderma umano tramite BRG1 dipendente da ATP
Come l’uso del carburante modella lo sviluppo umano precoce
I nostri corpi iniziano come piccole sfere di cellule staminali che devono decidere quale tipo di tessuto diventare. Questo studio pone una domanda sorprendentemente concreta: in che modo il modo in cui queste prime cellule consumano zucchero influenza la loro decisione di formare organi come fegato, polmoni e pancreas? Monitorando fianco a fianco l’uso di energia e la regolazione del DNA, i ricercatori mostrano che uno specifico cambiamento nel metabolismo degli zuccheri non è solo uno sfondo, ma un motore attivo dello sviluppo umano precoce.
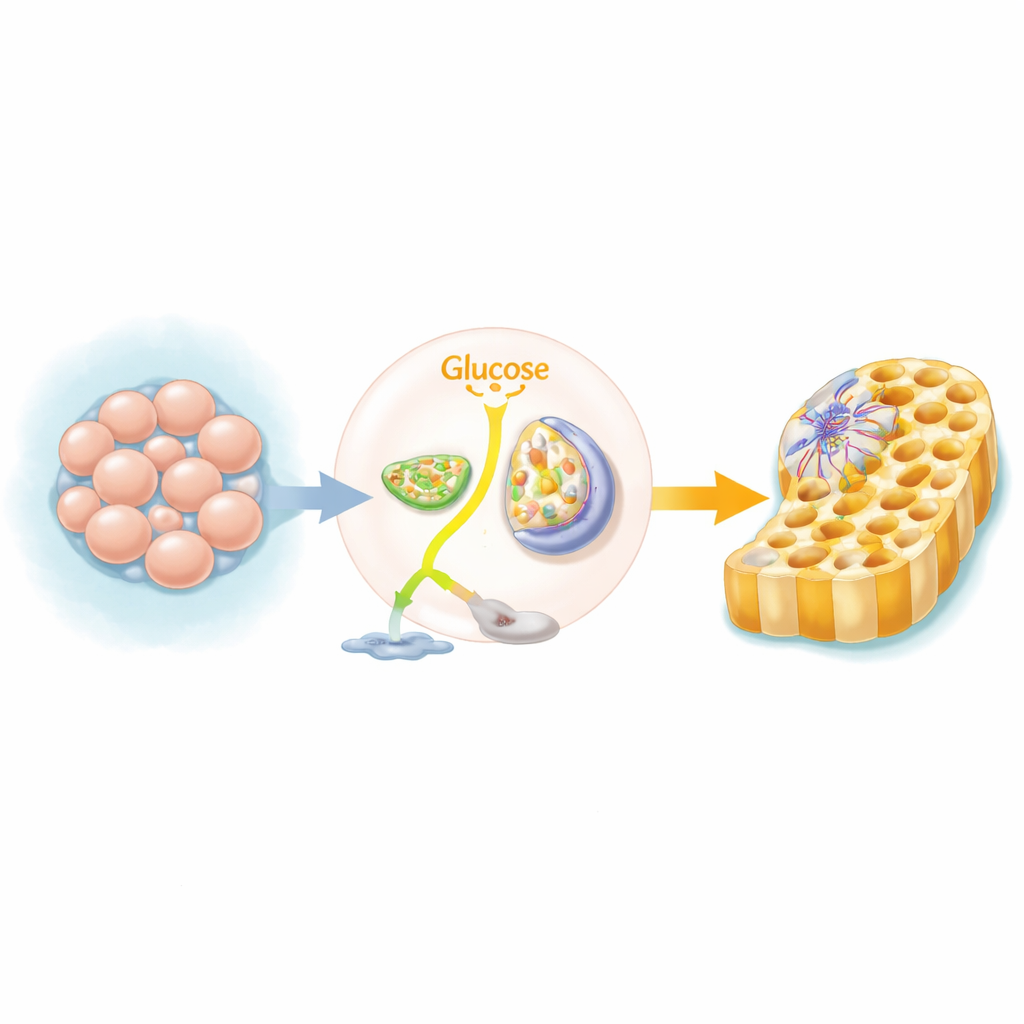
Un interruttore metabolico nei tessuti in formazione
Le cellule staminali pluripotenti umane, che possono dare origine a quasi ogni tessuto, si affidano normalmente a una via rapida ma inefficiente di utilizzo dello zucchero, degradando il glucosio fino a lattato anche quando c’è ossigeno disponibile. Quando queste cellule cominciano a formare lo strato di “endoderma definitivo” — il precursore dell’intestino, del fegato e del pancreas — capovolgono la loro via energetica principale. Invece di deviare lo zucchero verso il lattato, ne inviano di più nei mitocondri, le centrali energetiche della cellula, per alimentare il ciclo degli acidi tricarbossilici (TCA) e la fosforilazione ossidativa. Il team ha utilizzato schermate CRISPR a livello genomico e una batteria di inibitori chimici per mostrare che quando questo interruttore è bloccato, molte meno cellule acquisiscono con successo l’identità dell’endoderma.
Trasformare lo zucchero in energia mitocondriale
Al centro di questo cambio c’è il piruvato, un prodotto chiave della degradazione del glucosio. Il piruvato può essere convertito in lattato oppure importato nei mitocondri e trasformato in acetil‑CoA, il biglietto d’ingresso al ciclo TCA. I ricercatori hanno scoperto che indirizzare il piruvato verso i mitocondri favorisce fortemente la formazione dell’endoderma. Farmaci che inibiscono gli enzimi che producono lattato spingono più piruvato nei mitocondri e potenziano la differenziazione, mentre composti che impediscono al piruvato di entrare nei mitocondri o di essere lì metabolizzato riducono nettamente i marker dell’endoderma. Supplementare le cellule con piruvato o glutammina, un altro combustibile per il ciclo TCA, aiuta a ristabilire questo percorso di sviluppo quando i primi passaggi dell’uso degli zuccheri sono bloccati.
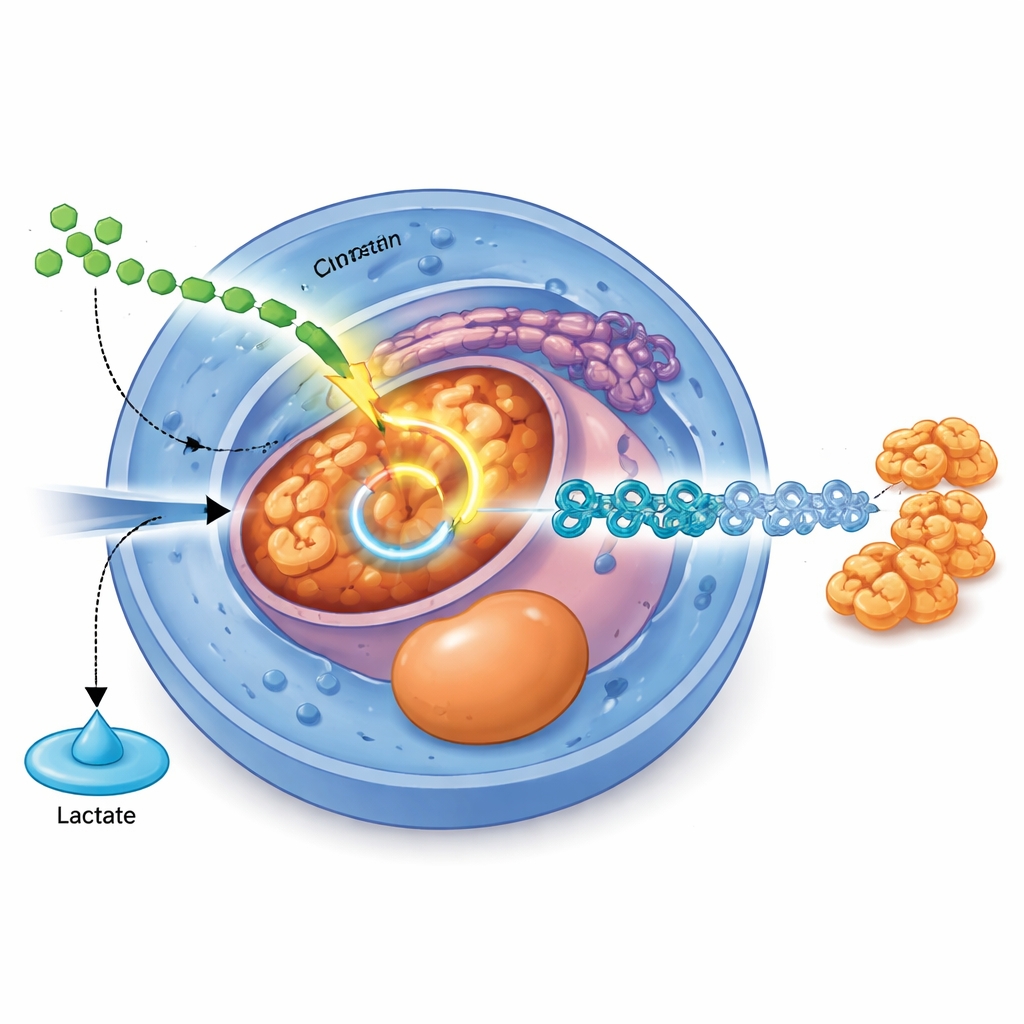
Una via di segnale che riorienta il metabolismo
Lo studio identifica un interruttore molecolare specifico che collega segnali esterni a questo ripindirizzamento interno del carburante. Un noto segnale di crescita chiamato TGFβ, agendo tramite le proteine messaggere SMAD2 e SMAD3, aumenta direttamente la produzione di PDHB, un componente centrale del complesso della piruvato deidrogenasi che introduce il piruvato nel ciclo TCA. Quando i livelli di PDHB sono ridotti mediante editing CRISPR, le cellule producono più lattato, meno acetil‑CoA e faticano a progredire dalle staminali verso l’endoderma e gli stadi pancreatici successivi. Al contrario, aumentare i livelli di PDHB migliora l’attività mitocondriale, aumenta l’energia cellulare e migliora l’efficienza della differenziazione in endoderma, soprattutto quando il segnale TGFβ è debole.
I livelli di energia controllano l’accesso al copione genetico
Perché questa scelta del carburante è così importante per l’identità cellulare? Gli autori ricondotto l’effetto all’ATP, la principale valuta energetica della cellula. Bloccare la degradazione del glucosio o l’ingresso mitocondriale abbassa i livelli di ATP, e semplicemente fornire ATP extra dall’esterno può salvare la differenziazione dell’endoderma non riuscita in diversi contesti. Il principale consumatore di ATP è il complesso BAF, una grande macchina di “rimodellamento della cromatina” centrata sulla proteina BRG1 che usa ATP per aprire il DNA ripiegato. Quando il BAF è chimicamente inibito o BRG1 è degradato o mutato in modo che il suo motore ATP‑dipendente non funzioni più, la formazione dell’endoderma rallenta e ATP aggiuntivo non può più aiutare. Mappature dell’accessibilità della cromatina a livello genomico mostrano che, quando PDHB o l’uso mitocondriale del piruvato sono ridotti, molte regioni vicine a geni correlati all’endoderma diventano meno accessibili, in particolare gli enhancer dove BRG1 normalmente si lega.
Cosa significa questo per costruire organi a partire dalle cellule
Nel complesso, il lavoro delinea una catena di eventi chiara: i segnali TGFβ aumentano i livelli di PDHB, PDHB convoglia il piruvato nei mitocondri, il metabolismo mitocondriale aumenta l’ATP e l’ATP alimenta l’apertura di regioni chiave del DNA guidata da BRG1, permettendo l’accensione dei geni dell’endoderma. In termini semplici, il modo in cui le prime cellule umane bruciano zucchero determina quanto “budget energetico” hanno per sbloccare le parti del genoma necessarie a diventare tessuto formatore di intestino e organi. Comprendere e controllare questo interruttore metabolico potrebbe migliorare i metodi per far crescere tessuti umani specifici da cellule staminali per ricerca, modellazione delle malattie e future terapie basate su cellule.
Citazione: Meng, L., Lv, J., Yi, Y. et al. TGFβ-activated PDHB promotes mitochondrial pyruvate metabolism and contributes to human endoderm differentiation via ATP-dependent BRG1. Nat Commun 17, 2846 (2026). https://doi.org/10.1038/s41467-026-69510-0
Parole chiave: metabolismo delle cellule staminali, differenziazione dell’endoderma, piruvato mitocondriale, rimodellamento della cromatina, segnalazione TGF beta