Clear Sky Science · ar
تنشيط PDHB بواسطة TGFβ يعزز أيض البيروفات الميتوكوندري ويساهم في تمايز الأديم الباطن البشري عبر BRG1 المعتمد على ATP
كيف تشكّل استخدام الوقود التطور البشري المبكر
تبدأ أجسامنا ككرات صغيرة من الخلايا الجذعية التي يجب أن تقرر أي أنواع الأنسجة ستصبح. يسأل هذا البحث سؤالاً عملياً بشكل مدهش: كيف يؤثر أسلوب هذه الخلايا المبكرة في حرق السكر على قرارها بتشكيل أعضاء مثل الكبد والرئتين والبنكرياس؟ من خلال تتبع استخدام الطاقة وتنظيم الحمض النووي جنباً إلى جنب، يظهر الباحثون أن تغييراً محدداً في استقلاب السكر ليس مجرد خلفية بل هو محرك نشط للتطور البشري المبكر.
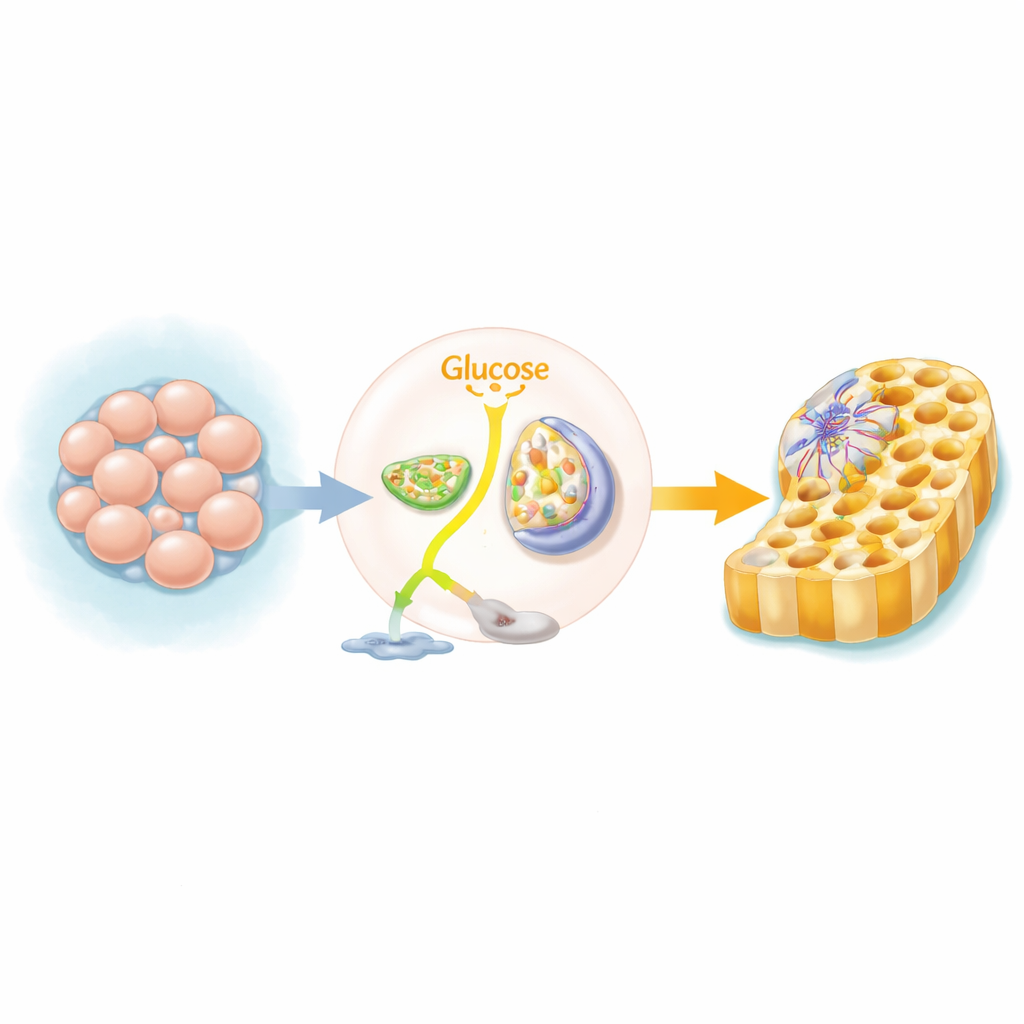
مفتاح استقلابي في الأنسجة النامية
تعتمد خلايا الإنسان المتعددة القدرات، القادرة على تكوين أي نسيج تقريباً، عادةً على طريقة سريعة لكنها غير فعالة لاستعمال السكر، حيث تكسر الغلوكوز إلى لاكتيت حتى في وجود الأكسجين. عندما تبدأ هذه الخلايا في تكوين طبقة «الأديم الباطن النهائي»—المقدمة للأمعاء والكبد والبنكرياس—تغير طريقها الرئيسي للوقود. بدلاً من تحويل السكر إلى لاكتيت، توجه كمية أكبر منه إلى الميتوكوندريا، محطات طاقة الخلية، لتشغيل دورة حمض ثلاثي الكربوكسيل (دورة TCA) والفوسفورية التأكسدية. استخدم الفريق شاشات CRISPR على مستوى الجينوم ومجموعة من الموانع الكيميائية ليظهر أن حجب هذا التحول يؤدي إلى فشل عدد أكبر بكثير من الخلايا في تبني هوية الأديم الباطن.
تحويل السكر إلى طاقة ميتوكوندرية
في قلب هذا التحول يكمن البيروفات، المنتج الأساسي لتفكك الغلوكوز. يمكن تحويل البيروفات إما إلى لاكتيت أو استيراده إلى الميتوكوندريا وتحويله إلى أسيتيل-كوإنزيم A، تذكرة الدخول إلى دورة TCA. وجد الباحثون أن توجيه البيروفات نحو الميتوكوندريا يفضّل بقوة تكوين الأديم الباطن. العقاقير التي تثبط إنزيمات صنع اللاكتيت تدفع مزيداً من البيروفات إلى الميتوكوندريا وتعزز التمايز، بينما تقلل المركبات التي تمنع دخول البيروفات إلى الميتوكوندريا أو معالجته هناك بشكل حاد من مؤشرات الأديم الباطن. كما أن تزويد الخلايا بالبيروفات أو بالجلوتامين، وقود آخر لدورة TCA، يساعد على استعادة هذا المسار التطوري عند حجب خطوات مبكرة من استعمال السكر.
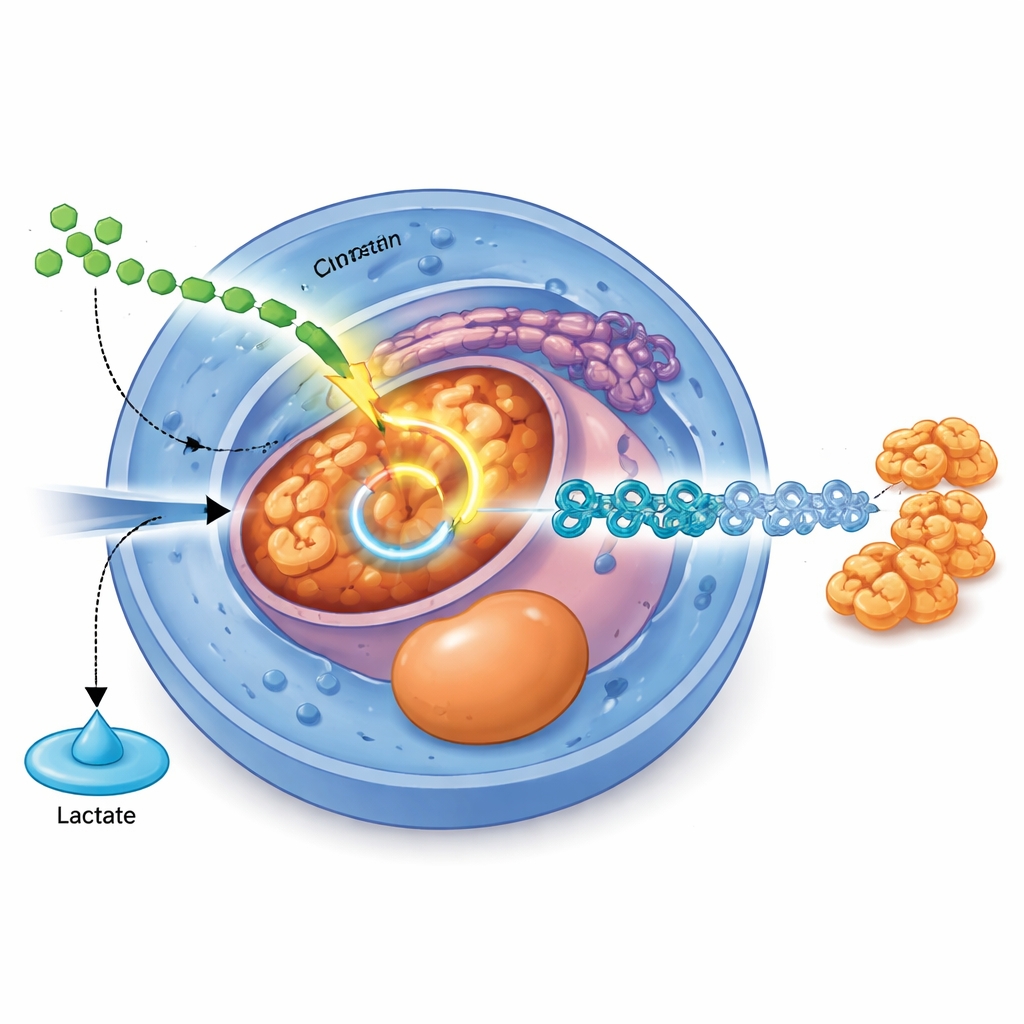
مسار إشاري يعيد توصيل الاستقلاب
يحدد البحث مفتاحاً جزيئياً يربط الإشارات الخارجية بهذا إعادة توجيه الوقود الداخلي. إشارة نمو معروفة تسمى TGFβ، تعمل عبر بروتيني الإرسال SMAD2 وSMAD3، تعزز مباشرة إنتاج PDHB، وهو مكوّن أساسي لمركب بيروفات ديهيدروجيناز الذي يمد دورة TCA بالبيروفات. عندما تُخفض مستويات PDHB باستخدام تعديل CRISPR، تنتج الخلايا لاكتيت أكثر، وأسيتيل-كوإنزيم A أقل، وتجد صعوبة في التقدم من الخلايا الجذعية نحو الأديم الباطن والمراحل البنكرياسية التالية. وبالعكس، رفع مستويات PDHB يعزز النشاط الميتوكوندري، ويزيد طاقة الخلايا، ويحسن كفاءة تمايز الأديم الباطن، خاصة عندما تكون إشارة TGFβ نفسها ضعيفة.
مستويات الطاقة تتحكم في الوصول إلى نص الجينوم
لماذا تهم هذه الاختيارات الوقودية الهوية بهذا القدر؟ يعيد المؤلفون الأثر إلى ATP، العملة الطاقية الرئيسية للخلية. يؤدي حظر تفكيك الغلوكوز أو دخول الميتوكوندريا إلى خفض مستويات ATP، ويمكن لتزويد الخلايا بـ ATP إضافي من الخارج أن ينقذ فشل تمايز الأديم الباطن في عدة حالات. المستهلك الرئيسي لـ ATP هو مركب BAF، آلة كبيرة لإعادة تشكيل الكروماتين تتمحور حول البروتين BRG1 وتستخدم ATP لفتح الحمض النووي المطوي. عندما يتم تثبيط BAF كيميائياً أو يتم تدهور BRG1 أو طفرته بحيث لا تعمل آليته المعتمدة على ATP، يتعثر تكوين الأديم الباطن ولا يعود ATP الإضافي قادراً على المعاونة. تُظهر خرائط الوصول إلى الكروماتين على مستوى الجينوم أنه عندما تُخفض مستويات PDHB أو استخدام البيروفات الميتوكوندرية، تصبح العديد من المناطق القريبة من الجينات المتعلقة بالأديم الباطن أقل قابلية للوصول، خاصة مناطق المحفزات حيث يرتبط BRG1 عادةً.
ماذا يعني هذا لبناء الأعضاء من الخلايا
تحدد هذه الدراسة مجمل الأحداث بوضوح: ترفع إشارات TGFβ مستويات PDHB، يوجه PDHB البيروفات إلى الميتوكوندريا، يرفع الاستقلاب الميتوكوندري ATP، ويستخدم ATP لتمكين BRG1 من فتح مناطق مهمة من الحمض النووي بحيث يمكن تشغيل جينات الأديم الباطن. ببساطة، يحدد أسلوب حرق الخلايا البشرية المبكرة للسكر مقدار «ميزانية الطاقة» المتاحة لها لفتح أجزاء من الجينوم اللازمة لتشكيل الأنسجة المكونة للأمعاء والأعضاء. قد يحسن فهم هذا التحول الوقودي والتحكم فيه طرق زراعة أنسجة بشرية محددة من الخلايا الجذعية لأغراض البحث، ونمذجة الأمراض، والعلاجات الخلوية المستقبلية.
الاستشهاد: Meng, L., Lv, J., Yi, Y. et al. TGFβ-activated PDHB promotes mitochondrial pyruvate metabolism and contributes to human endoderm differentiation via ATP-dependent BRG1. Nat Commun 17, 2846 (2026). https://doi.org/10.1038/s41467-026-69510-0
الكلمات المفتاحية: استقلاب الخلايا الجذعية, تمايز الأديم الباطن, البيروفات الميتوكوندرية, إعادة تشكيل الكروماتين, إشارة TGF بيتا