Clear Sky Science · de
Durch TGFβ aktiviertes PDHB fördert die mitochondriale Pyruvatverwertung und trägt über ATP-abhängiges BRG1 zur Differenzierung des menschlichen Endoderms bei
Wie der Brennstoffverbrauch die frühe menschliche Entwicklung formt
Unser Körper beginnt als winzige Kugel aus Stammzellen, die entscheiden müssen, zu welchen Geweben sie werden. Diese Studie stellt eine überraschend bodenständige Frage: Wie beeinflusst die Art, wie diese frühen Zellen Zucker verbrennen, ihre Entscheidung, Organe wie Leber, Lunge und Bauchspeicheldrüse zu bilden? Indem Energieverbrauch und DNA‑Regulation parallel verfolgt werden, zeigen die Forschenden, dass ein spezifischer Wechsel im Zuckerstoffwechsel nicht nur Kulisse ist, sondern ein aktiver Treiber der frühen menschlichen Entwicklung.
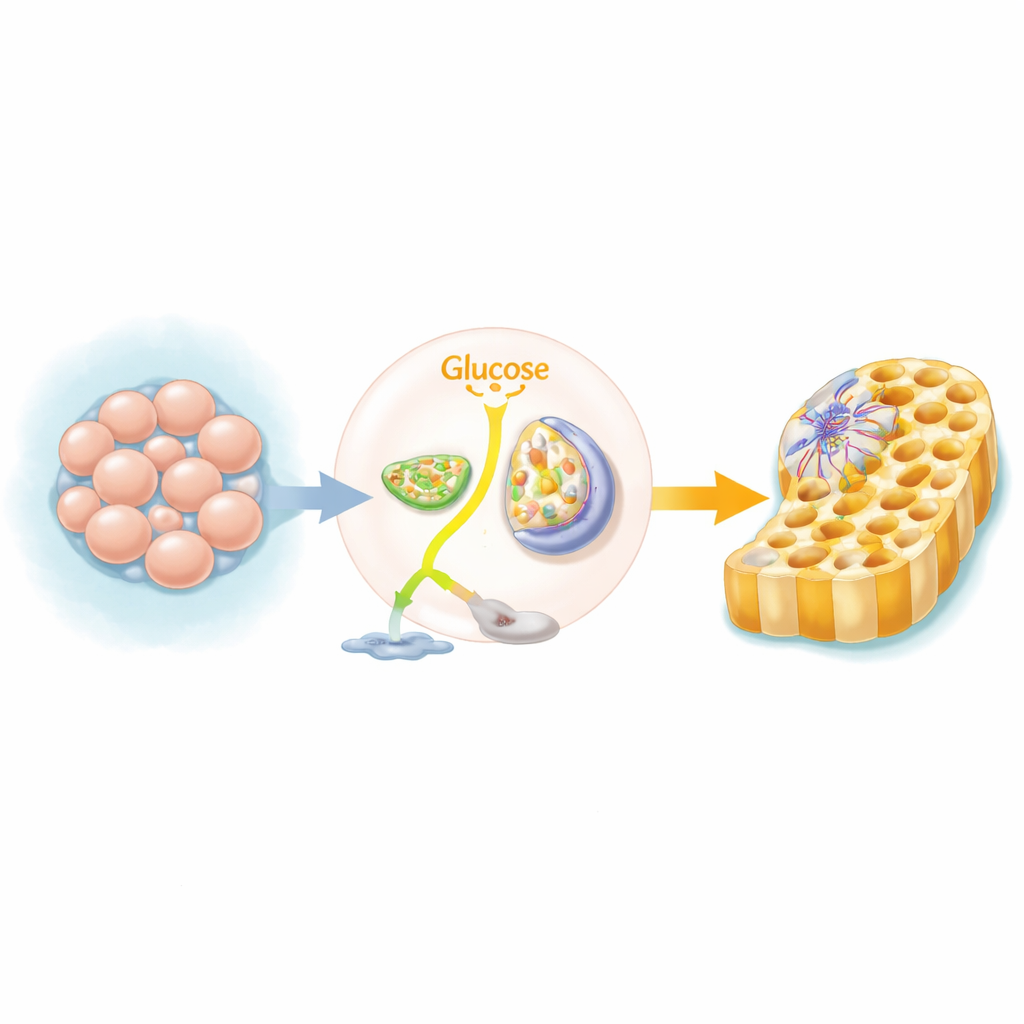
Ein metabolischer Schalter in entstehenden Geweben
Humane pluripotente Stammzellen, die fast jedes Gewebe bilden können, verlassen sich normalerweise auf eine schnelle, aber wenig effiziente Zuckernutzung und bauen Glukose zu Lactat ab, selbst wenn Sauerstoff vorhanden ist. Wenn diese Zellen beginnen, die „definitive Endoderm“-Schicht zu bilden – den Vorläufer von Darm, Leber und Bauchspeicheldrüse – kippt ihre hauptsächliche Brennstoffroute. Statt Zucker in Lactat zu leiten, schicken sie mehr davon in die Mitochondrien, die Kraftwerke der Zelle, um den Zitratzyklus (TCA) und die oxidative Phosphorylierung zu betreiben. Das Team verwendete genomweite CRISPR-Screens und eine Reihe chemischer Hemmstoffe und zeigte, dass bei Blockade dieses Schalters deutlich weniger Zellen erfolgreich die Endodermidentität annehmen.
Zucker in mitochondriale Energie verwandeln
Im Zentrum dieses Wechsels steht Pyruvat, ein zentrales Abbauprodukt der Glukose. Pyruvat kann entweder zu Lactat umgewandelt oder in die Mitochondrien importiert und dort zu Acetyl‑CoA gemacht werden, dem Eintrittsticket in den TCA‑Zyklus. Die Forschenden fanden, dass die Lenkung von Pyruvat in die Mitochondrien die Endodermbildung deutlich begünstigt. Wirkstoffe, die Lactat bildende Enzyme hemmen, treiben mehr Pyruvat in die Mitochondrien und steigern die Differenzierung, während Verbindungen, die den Eintritt von Pyruvat in Mitochondrien oder dessen Verarbeitung dort verhindern, Endodermmarker stark reduzieren. Die Ergänzung der Zellen mit Pyruvat oder Glutamin, einem weiteren Brennstoff für den TCA‑Zyklus, hilft, diesen Entwicklungsweg wiederherzustellen, wenn frühe Schritte der Zuckernutzung blockiert sind.
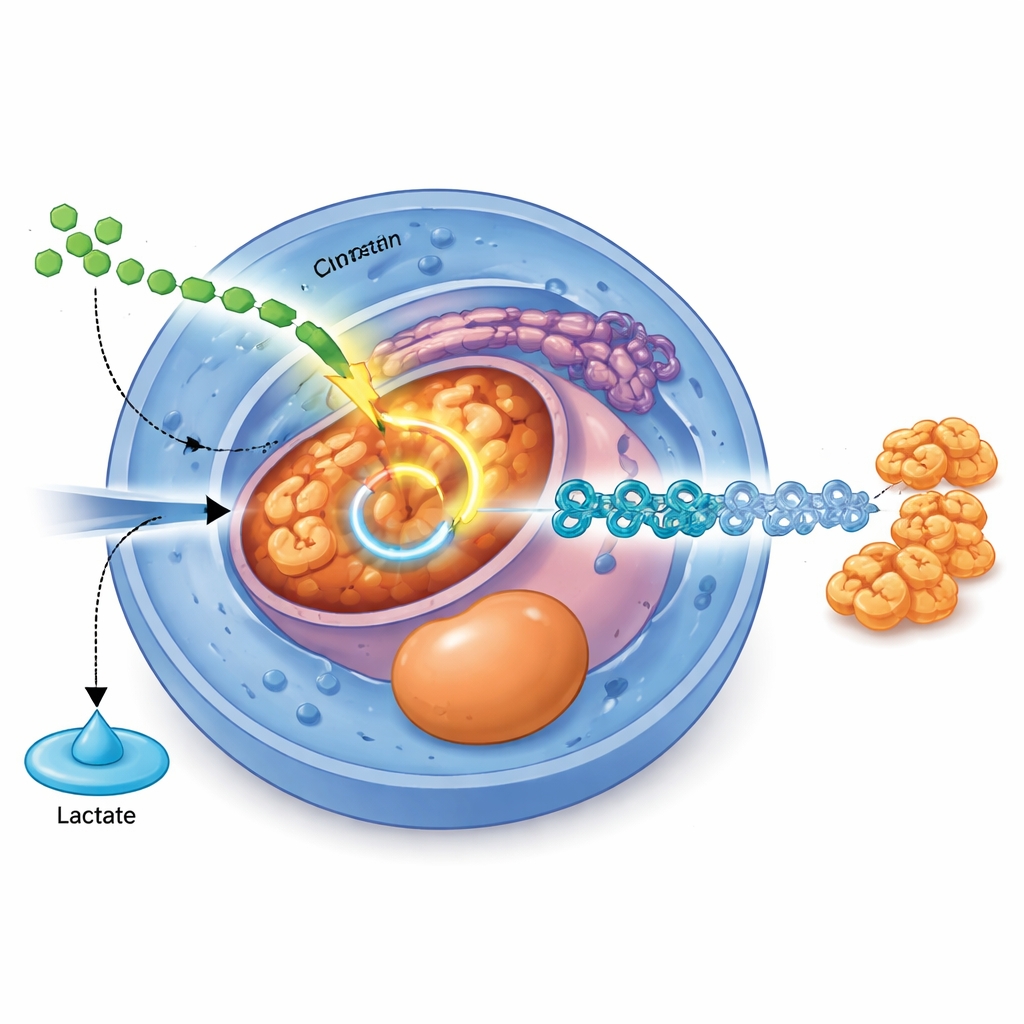
Ein Signalweg, der den Stoffwechsel umverdrahtet
Die Studie identifiziert einen spezifischen molekularen Schalter, der äußere Signale mit dieser inneren Brennstoffumleitung verbindet. Ein bekannter Wachstumsfaktor, TGFβ, wirkt über seine Botenproteine SMAD2 und SMAD3 und steigert direkt die Produktion von PDHB, einer Kernkomponente des Pyruvatdehydrogenase‑Komplexes, der Pyruvat in den TCA‑Zyklus einspeist. Werden PDHB‑Spiegel mittels CRISPR reduziert, produzieren die Zellen mehr Lactat, weniger Acetyl‑CoA und haben Schwierigkeiten, sich vom Stammzellzustand in Richtung Endoderm und späterer pankreatischer Stadien weiterzuentwickeln. Umgekehrt verbessert eine Erhöhung von PDHB die mitochondriale Aktivität, steigert die zelluläre Energie und erhöht die Effizienz der Endodermdifferenzierung, insbesondere wenn das TGFβ‑Signal selbst schwach ist.
Energieniveaus steuern den Zugang zum genetischen Skript
Warum ist diese Brennstoffwahl so wichtig für die Identität? Die Autor*innen führen den Effekt auf ATP zurück, die wichtigste Energiewährung der Zelle. Die Blockade des Glukoseabbaus oder des mitochondrialen Eintritts senkt die ATP‑Spiegel, und das bloße Zuführen von zusätzlichem ATP von außen kann in mehreren Fällen eine gescheiterte Endodermdifferenzierung retten. Der wichtigste ATP‑Verbraucher ist der BAF‑Komplex, eine große Chromatin‑Remodelling‑Maschinerie zentriert um das Protein BRG1, die ATP nutzt, um gefaltete DNA zu öffnen. Wenn BAF chemisch gehemmt oder BRG1 abgebaut oder so mutiert wird, dass sein ATP‑getriebener Motor nicht mehr arbeitet, stockt die Endodermbildung und zusätzliches ATP hilft nicht mehr. Genomweite Kartierungen der Chromatinzugänglichkeit zeigen, dass bei Reduktion von PDHB oder mitochondrialer Pyruvatnutzung viele Regionen in der Nähe endodermbezogener Gene weniger zugänglich werden, besonders Enhancer‑Regionen, an die BRG1 normalerweise bindet.
Was das für den Aufbau von Organen aus Zellen bedeutet
Zusammengefasst skizziert die Arbeit eine klare Ereigniskette: TGFβ‑Signale erhöhen die PDHB‑Spiegel, PDHB lenkt Pyruvat in die Mitochondrien, der mitochondriale Stoffwechsel erhöht ATP, und ATP treibt das BRG1‑abhängige Öffnen wichtiger DNA‑Regionen an, sodass Endodermgene angeschaltet werden können. Einfach gesagt bestimmt die Art, wie frühe menschliche Zellen Zucker verbrennen, wie viel „Energieetat“ ihnen zur Verfügung steht, um die Genomstellen freizuschalten, die nötig sind, damit sie Darm‑ und organbildendes Gewebe werden. Das Verständnis und die gezielte Steuerung dieses Brennstoffschalters könnte Methoden verbessern, bestimmte menschliche Gewebe aus Stammzellen für Forschung, Krankheitsmodellierung und zukünftige zellbasierte Therapien zu züchten.
Zitation: Meng, L., Lv, J., Yi, Y. et al. TGFβ-activated PDHB promotes mitochondrial pyruvate metabolism and contributes to human endoderm differentiation via ATP-dependent BRG1. Nat Commun 17, 2846 (2026). https://doi.org/10.1038/s41467-026-69510-0
Schlüsselwörter: Stammzellstoffwechsel, Endodermdifferenzierung, mitochondriales Pyruvat, Chromatin-Remodelling, TGF‑Beta‑Signalgebung