Clear Sky Science · ru
Активация PDHB через TGFβ усиливает митохондриальный метаболизм пирувата и способствует дифференцировке человеческого энтодерма через ATP-зависимый BRG1
Как использование топлива формирует раннее развитие человека
Наши тела начинаются как крошечные шарики стволовых клеток, которым нужно решить, в какие ткани превратиться. В этом исследовании задают на удивление приземлённый вопрос: как то, как эти ранние клетки «сжигают» сахар, влияет на их решение формировать органы, такие как печень, лёгкие и поджелудочная железа? Отслеживая использование энергии и регулирование ДНК параллельно, исследователи показывают, что специфический сдвиг в сахарном метаболизме — это не просто фон, а активный драйвер раннего развития человека.
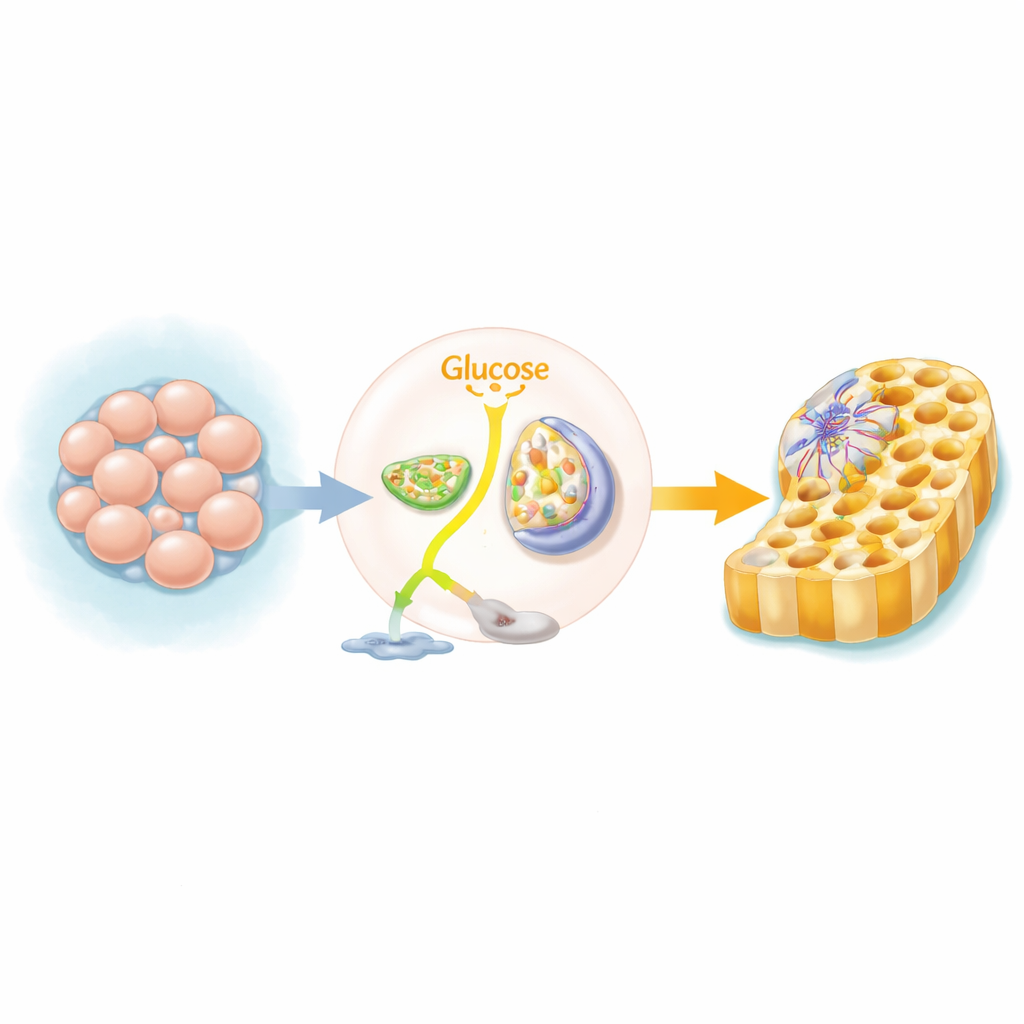
Метаболический переключатель в формирующихся тканях
Человеческие плюрипотентные стволовые клетки, которые могут дать начало почти любой ткани, обычно полагаются на быстрый, но неэффективный способ использования сахара, расщепляя глюкозу до лактата даже при наличии кислорода. По мере того как эти клетки начинают формировать «дефинитивный энтодерм» — предшественник кишечника, печени и поджелудочной — они переключают основной топливный путь. Вместо того чтобы направлять сахар в лактат, они отправляют больше его в митохондрии, «электростанции» клетки, чтобы запустить цикл трикарбоновых кислот (TCA) и окислительное фосфорилирование. Команда использовала геномные скрины CRISPR и набор химических блокаторов, чтобы показать, что при блокировке этого переключения значительно меньше клеток успешно приобретают идентичность энтодерма.
Преобразование сахара в митохондриальную энергию
В основе этого переключения лежит пируват, ключевой продукт расщепления глюкозы. Пируват может либо превращаться в лактат, либо импортироваться в митохондрии и превращаться в ацетил-CoA — «билет» в цикл TCA. Исследователи обнаружили, что направление пирувата в сторону митохондрий сильно благоприятствует формированию энтодерма. Препараты, ингибирующие ферменты, делающие лактат, «перекачивают» больше пирувата в митохондрии и усиливают дифференцировку, тогда как соединения, препятствующие попаданию пирувата в митохондрии или его обработке там, резко снижают маркеры энтодерма. Подкормка клеток пируватом или глутамином, ещё одним субстратом для цикла TCA, помогает восстановить этот путь развития, когда ранние шаги использования сахара заблокированы.
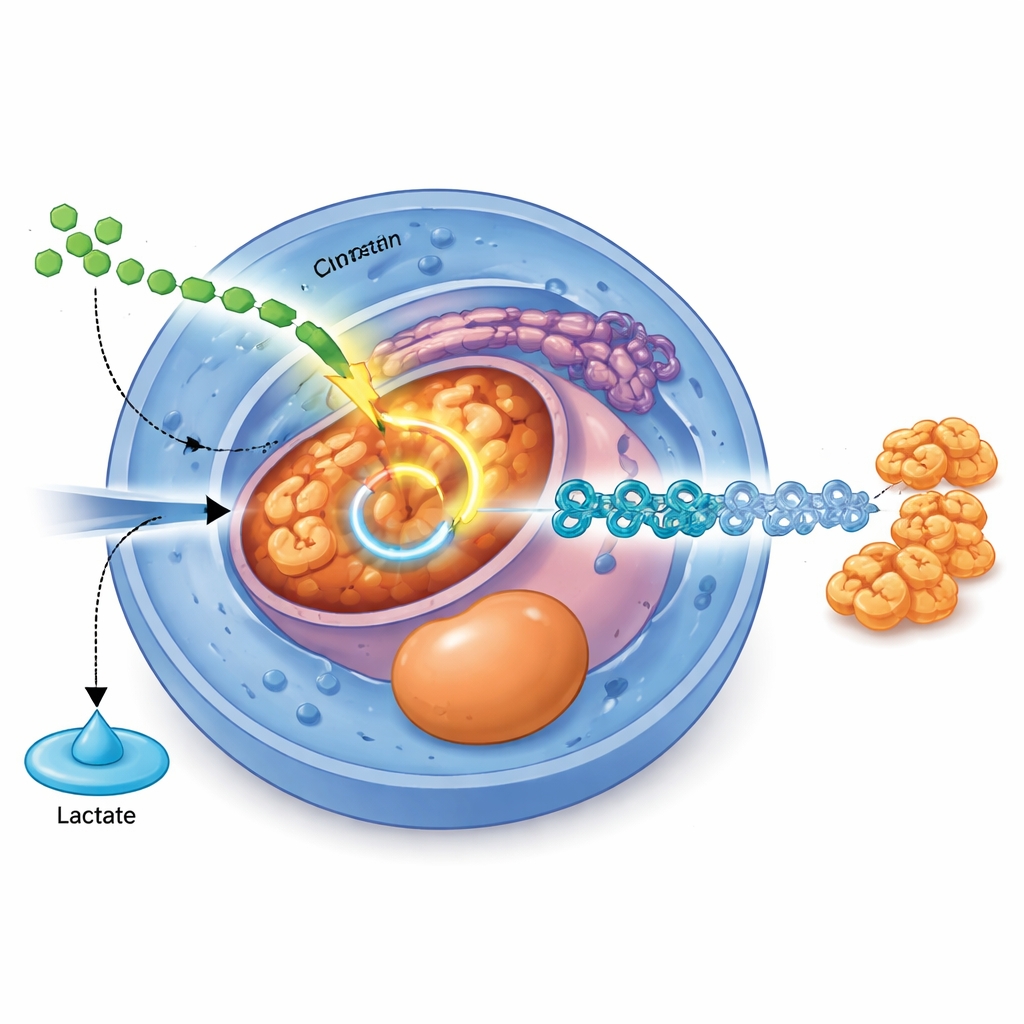
Сигнальный путь, который перенастраивает метаболизм
В исследовании идентифицирован конкретный молекулярный переключатель, связывающий внешние сигналы с внутренним перенаправлением топлива. Хорошо известный фактор роста TGFβ через свои медиаторы SMAD2 и SMAD3 прямо повышает продукцию PDHB, ключевого компонента комплекса пируватдегидрогеназы, который направляет пируват в цикл TCA. Когда уровни PDHB снижали с помощью редактирования CRISPR, клетки производили больше лактата, меньше ацетил-CoA и испытывали трудности с переходом от стволовых клеток к энтодерму и далее к панкреатическим стадиям. Наоборот, повышение уровня PDHB усиливает митохондриальную активность, увеличивает клеточную энергию и улучшает эффективность дифференцировки в энтодерм, особенно при слабом сигнале TGFβ.
Уровни энергии контролируют доступ к генетической программе
Почему выбор топлива так сильно влияет на идентичность? Авторы отнесли эффект к ATP, главной энергетической валюте клетки. Блокировка распада глюкозы или входа в митохондрии снижает уровни ATP, и простое внешнее добавление ATP может восстановить неудавшуюся дифференцировку в энтодерм в нескольких условиях. Главным потребителем ATP является комплекс BAF, большой механизм «ремоделирования хроматина», центрированный на белке BRG1, который использует ATP для раскрытия свернутой ДНК. Когда BAF химически ингибируют или BRG1 деградируется либо мутирован так, что его ATP-зависимый «мотор» больше не работает, формирование энтодерма нарушается и дополнительный ATP уже не помогает. Геномное картирование доступности хроматина показывает, что при снижении PDHB или митохондриального использования пирувата многие регионы рядом с генами, связанными с энтодермом, становятся менее доступными, особенно энхансеры, где обычно связывается BRG1.
Что это значит для создания органов из клеток
В сумме работа описывает чёткую цепочку событий: сигналы TGFβ повышают уровни PDHB, PDHB направляет пируват в митохондрии, митохондриальный метаболизм повышает ATP, а ATP питает BRG1-опосредованное раскрытие ключевых участков ДНК, чтобы гены энтодерма могли включиться. Проще говоря, то, как ранние человеческие клетки «сжигают» сахар, определяет, какой «энергетический бюджет» у них есть, чтобы открыть те участки генома, которые нужны для превращения в ткани, формирующие кишечник и органы. Понимание и контроль этого топливного переключателя может улучшить методы выращивания специфических человеческих тканей из стволовых клеток для исследований, моделирования болезней и потенциальных клеточных терапий.
Цитирование: Meng, L., Lv, J., Yi, Y. et al. TGFβ-activated PDHB promotes mitochondrial pyruvate metabolism and contributes to human endoderm differentiation via ATP-dependent BRG1. Nat Commun 17, 2846 (2026). https://doi.org/10.1038/s41467-026-69510-0
Ключевые слова: метаболизм стволовых клеток, дифференцировка энтодерма, митохондриальный пируват, ремоделирование хроматина, сигнализация TGF бета