Clear Sky Science · pl
TGFβ-aktywowany PDHB promuje mitochondrialny metabolizm pirogronianu i przyczynia się do różnicowania endodermy u człowieka poprzez ATP-zależny BRG1
Jak wykorzystanie paliwa kształtuje wczesny rozwój człowieka
Nasze ciała zaczynają się jako maleńkie kulki komórek macierzystych, które muszą zdecydować, w jaki rodzaj tkanek się przekształcić. W tym badaniu zadano pozornie przyziemne pytanie: w jaki sposób sposób, w jaki te wczesne komórki spalają cukier, wpływa na ich decyzję o tworzeniu narządów takich jak wątroba, płuca i trzustka? Śledząc równocześnie zużycie energii i regulację DNA, badacze pokazują, że specyficzna zmiana w metabolizmie cukru nie jest jedynie tłem, lecz aktywnym czynnikiem napędzającym wczesny rozwój człowieka.
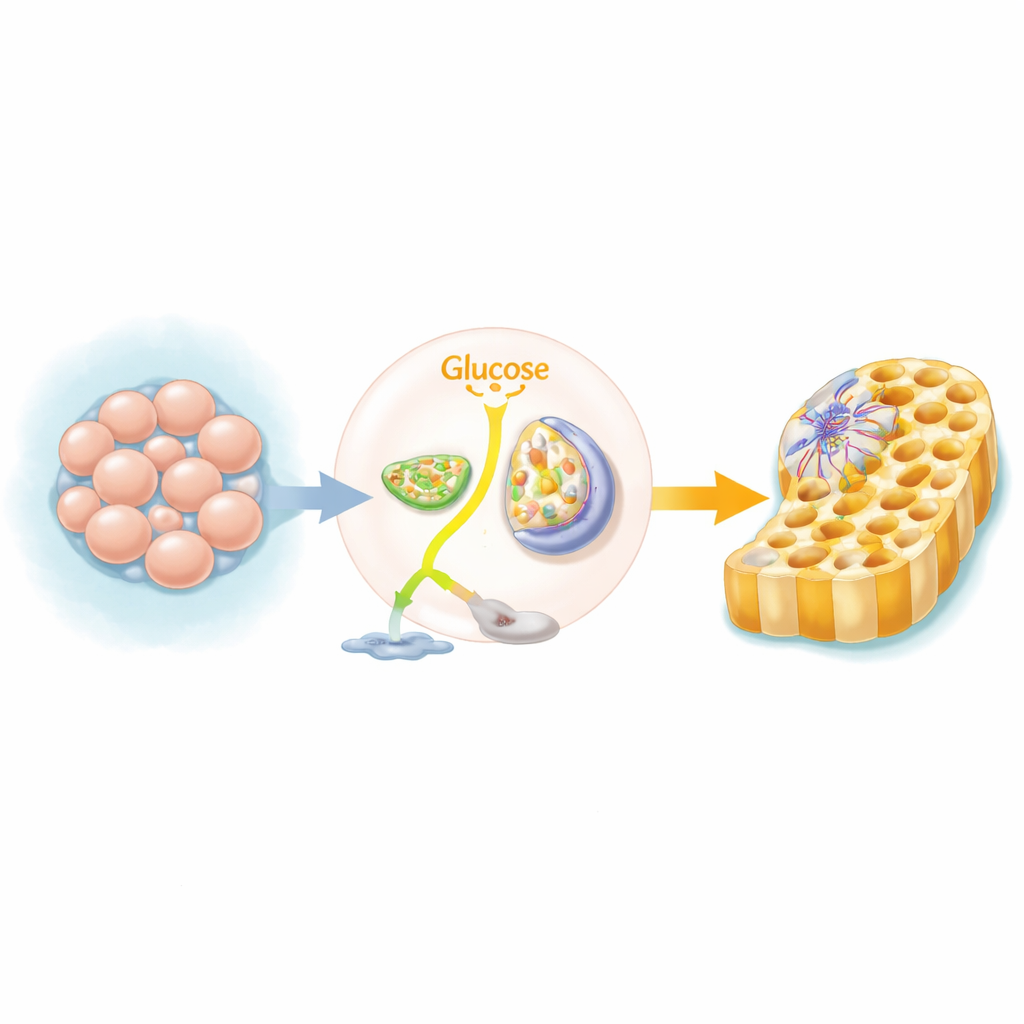
Przełączenie metaboliczne w kształtujących się tkankach
Ludzkie pluripotentne komórki macierzyste, które mogą dać początek niemal każdej tkance, zwykle polegają na szybkim, lecz mało wydajnym sposobie wykorzystania cukru, rozkładając glukozę do mleczanu nawet w obecności tlenu. Gdy te komórki zaczynają formować „definitywną endodermę” — prekursor jelita, wątroby i trzustki — zmieniają główną ścieżkę pozyskiwania paliwa. Zamiast odprowadzać cukier do mleczanu, wysyłają więcej jego pochodnych do mitochondriów, elektrowni komórkowych, aby zasilić cykl kwasów trikarboksylowych (TCA) i fosforylację oksydacyjną. Zespół wykorzystał przesiewy CRISPR obejmujące całe genomy oraz zestaw inhibitorów chemicznych, aby wykazać, że gdy to przełączenie zostaje zablokowane, znacznie mniej komórek pomyślnie przyjmuje tożsamość endodermalną.
Przekształcanie cukru w mitochondrialną moc
W centrum tego przełączenia znajduje się pirogronian, kluczowy produkt rozpadu glukozy. Pirogronian może być albo przekształcony do mleczanu, albo zaimportowany do mitochondriów i przekształcony w acetylo-CoA, bilecik wejścia do cyklu TCA. Badacze stwierdzili, że skierowanie pirogronianu w stronę mitochondriów zdecydowanie sprzyja powstawaniu endodermy. Leki hamujące enzymy tworzące mleczan powodują, że więcej pirogronianu trafia do mitochondriów i zwiększają różnicowanie, podczas gdy związki uniemożliwiające wejście pirogronianu do mitochondriów lub jego przetwarzanie tam gwałtownie zmniejszają markery endodermy. Suplementacja komórek pirogronianem lub glutaminą, innym paliwem dla cyklu TCA, pomaga przywrócić tę ścieżkę rozwojową, gdy wczesne etapy wykorzystania cukru są zablokowane.
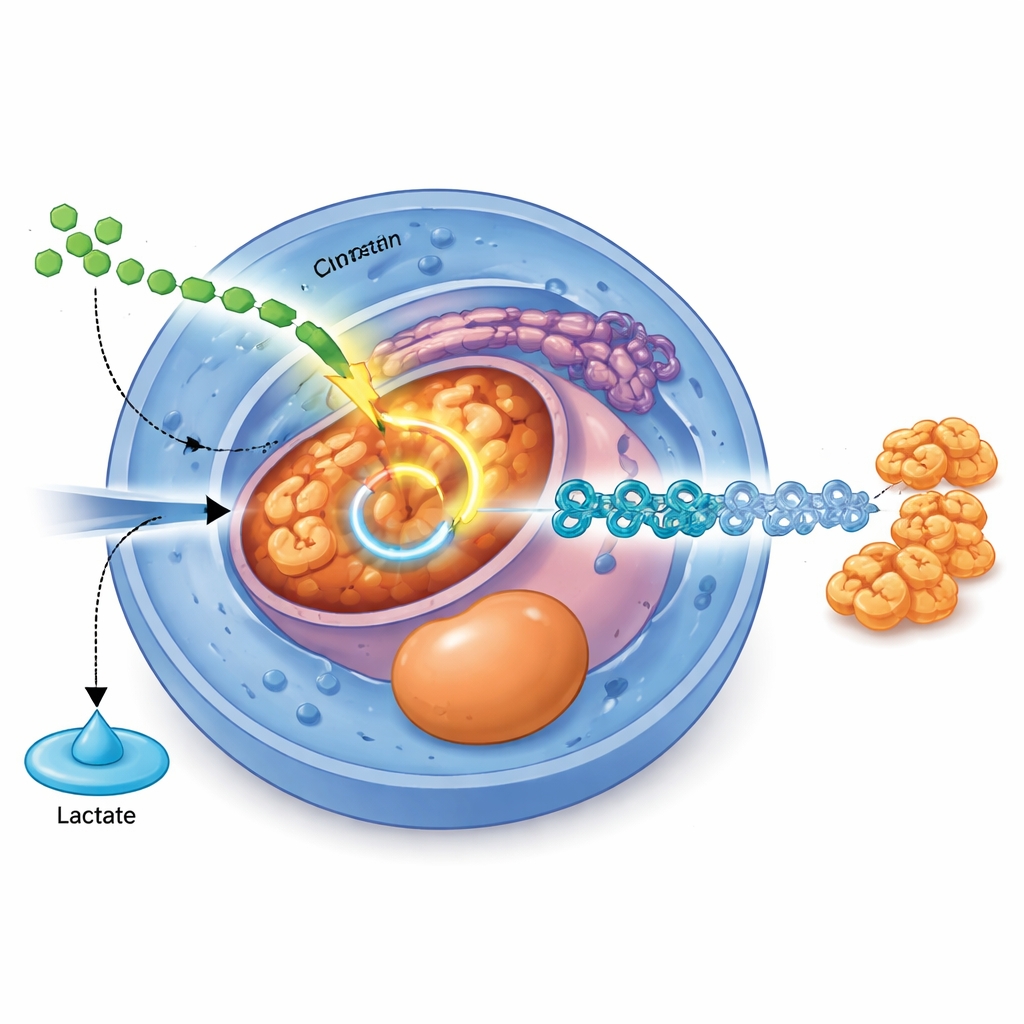
Szlak sygnałowy, który przepina metabolizm
Badanie identyfikuje konkretny przełącznik molekularny łączący sygnały z zewnątrz z wewnętrznym przekierowaniem paliwa. Znany sygnał wzrostu zwany TGFβ, działając przez białka przekaźnikowe SMAD2 i SMAD3, bezpośrednio zwiększa produkcję PDHB, kluczowego składnika kompleksu dehydrogenazy pirogronianowej, który kieruje pirogronian do cyklu TCA. Gdy poziomy PDHB są obniżane za pomocą edycji CRISPR, komórki produkują więcej mleczanu, mniej acetylo-CoA i mają trudności z przejściem od komórek macierzystych do endodermy, a później do stadiów trzustkowych. Odwrotnie, podniesienie poziomu PDHB zwiększa aktywność mitochondrialną, podnosi poziom energii w komórce i poprawia wydajność różnicowania endodermy, szczególnie gdy sam sygnał TGFβ jest słaby.
Poziomy energii kontrolują dostęp do zapisu genetycznego
Dlaczego wybór paliwa tak bardzo wpływa na tożsamość komórkową? Autorzy wiążą efekt z ATP, główną walutą energetyczną komórki. Blokowanie rozkładu glukozy lub wejścia do mitochondriów obniża poziomy ATP, a proste dostarczenie dodatkowego ATP z zewnątrz może uratować nieudane różnicowanie endodermy w kilku ustawieniach. Kluczowym konsumentem ATP jest kompleks BAF, duża maszyna „remodelingu chromatyny” skoncentrowana na białku BRG1, która wykorzystuje ATP do otwierania zwiniętego DNA. Gdy BAF jest chemicznie zahamowany lub BRG1 zostaje zdegradowany lub zmutowany tak, że jego napęd zależny od ATP przestaje działać, powstawanie endodermy słabnie i dodatkowy ATP przestaje pomagać. Mapowanie dostępności chromatyny w skali całego genomu pokazuje, że gdy PDHB lub mitochondrialne użycie pirogronianu są zmniejszone, wiele regionów w pobliżu genów związanych z endodermą staje się mniej dostępnych, zwłaszcza regiony wzmacniające, do których normalnie wiąże się BRG1.
Co to oznacza dla budowy narządów z komórek
Podsumowując, praca opisuje jasny łańcuch zdarzeń: sygnały TGFβ podnoszą poziom PDHB, PDHB kieruje pirogronian do mitochondriów, metabolizm mitochondrialny zwiększa ATP, a ATP napędza otwieranie kluczowych regionów DNA przez BRG1, dzięki czemu geny endodermy mogą się włączyć. Mówiąc prościej, sposób, w jaki wczesne komórki ludzkie spalają cukier, decyduje o tym, ile „budżetu energetycznego” mają, by odblokować części genomu niezbędne do stania się tkanką tworzącą jelita i narządy. Zrozumienie i kontrola tego przełączenia paliwowego mogą poprawić metody hodowli konkretnych ludzkich tkanek z komórek macierzystych do badań, modelowania chorób i przyszłych terapii komórkowych.
Cytowanie: Meng, L., Lv, J., Yi, Y. et al. TGFβ-activated PDHB promotes mitochondrial pyruvate metabolism and contributes to human endoderm differentiation via ATP-dependent BRG1. Nat Commun 17, 2846 (2026). https://doi.org/10.1038/s41467-026-69510-0
Słowa kluczowe: metabolizm komórek macierzystych, różnicowanie endodermy, mitochondrialny pirogronian, remodeling chromatyny, sygnalizacja TGF beta