Clear Sky Science · sv
TGFβ-aktiverat PDHB främjar mitokondriell pyruvatmetabolism och bidrar till mänsklig endodermdifferentiering via ATP-beroende BRG1
Hur bränsleanvändning formar tidig mänsklig utveckling
Våra kroppar börjar som små klot av stamceller som måste bestämma vilken typ av vävnad de ska bli. Den här studien ställer en överraskande jordnära fråga: hur påverkar sättet dessa tidiga celler förbränner socker deras beslut att bilda organ som levern, lungorna och bukspottkörteln? Genom att följa energianvändning och DNA-reglering parallellt visar forskarna att ett specifikt skift i sockeromvandlingen inte bara är en bakgrundsprocess utan en aktiv drivkraft i tidig mänsklig utveckling.
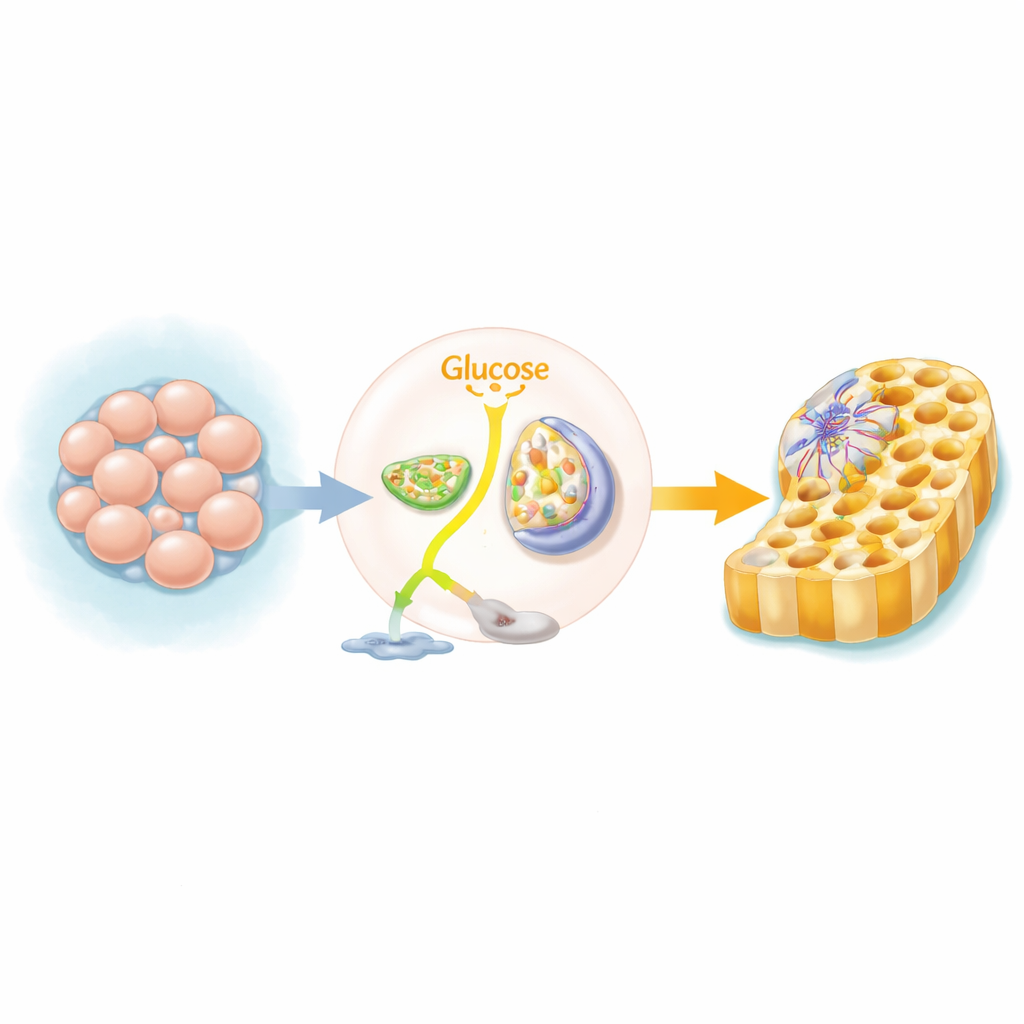
En metabolisk växel i blivande vävnader
Mänskliga pluripotenta stamceller, som kan bilda nästan alla vävnadstyper, förlitar sig normalt på ett snabbt men ineffektivt sätt att använda socker och bryter ner glukos till laktat även när syre finns tillgängligt. När dessa celler börjar bilda det så kallade “definitiva endodermet” — föregångaren till tarm, lever och pankreas — byter de sin huvudsakliga bränsleväg. Istället för att skicka socker till laktat skickar de mer av det in i mitokondrierna, cellens kraftverk, för att driva trikarboxylsyracykeln (TCA) och oxidativ fosforylering. Gruppen använde genomsnittliga CRISPR-skärmar över genomet och en uppsättning kemiska blockeringar för att visa att när denna växling hindras, antar långt färre celler endodermidentitet.
Att omvandla socker till mitokondriell kraft
I centrum för denna växling ligger pyruvat, en nyckelprodukt vid nedbrytning av glukos. Pyruvat kan antingen omvandlas till laktat eller importeras in i mitokondrierna och omvandlas till acetyl-CoA, inträdesbiljetten till TCA-cykeln. Forskarna fann att att styra pyruvat mot mitokondrierna starkt gynnar endodermbildning. Läkemedel som hämmar enzymer som bildar laktat skjuter mer pyruvat in i mitokondrierna och främjar differentiering, medan ämnen som förhindrar pyruvat från att komma in i mitokondrierna eller bearbetas där kraftigt minskar endodermmarkörer. Att tillsätta pyruvat eller glutamin, ett annat bränsle för TCA-cykeln, hjälper till att återställa denna utvecklingsväg när tidiga steg i sockeranvändningen är blockerade.
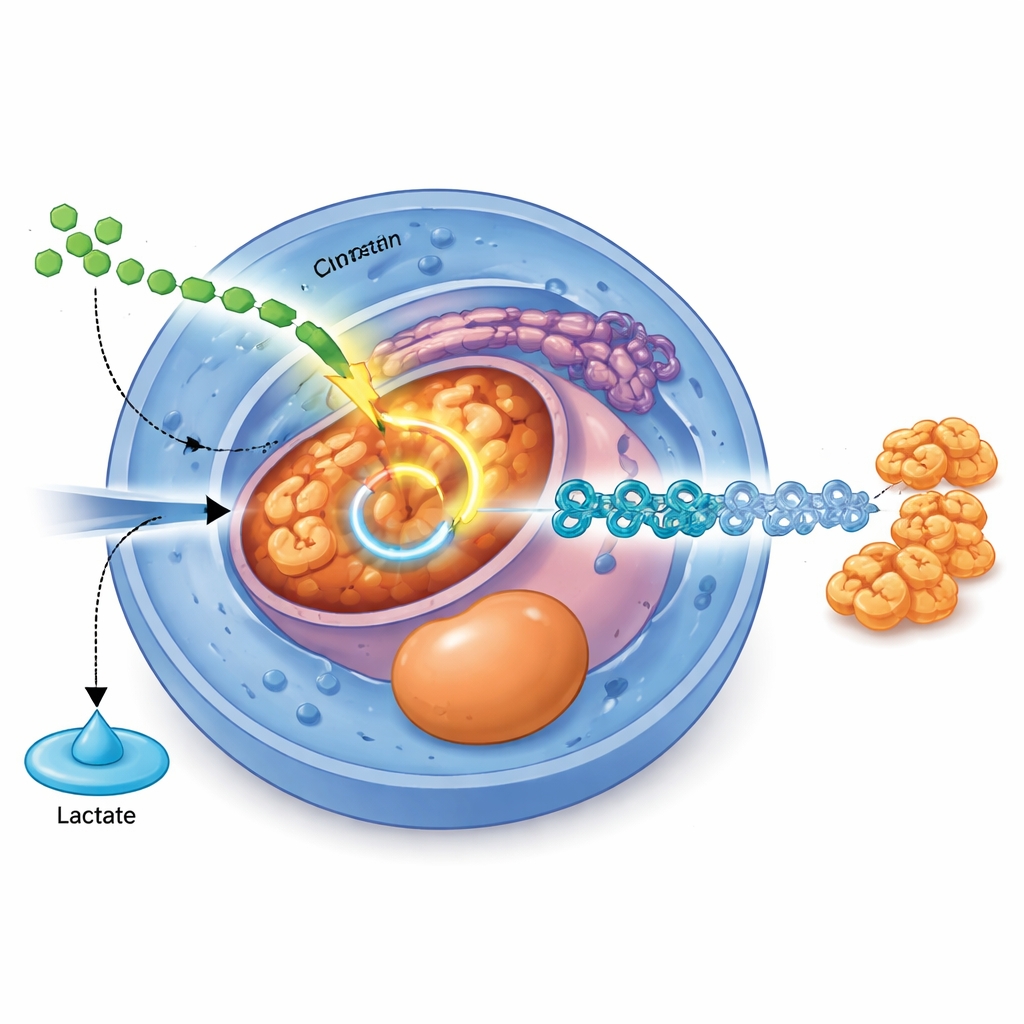
En signalväg som omkopplar metabolismen
Studien identifierar en specifik molekylär omkopplare som kopplar yttre signaler till denna interna bränsleomdirigering. En välkänd tillväxtsignal kallad TGFβ, som verkar via sina budbärarproteiner SMAD2 och SMAD3, ökar direkt produktionen av PDHB, en kärnkomponent i pyruvatdehydrogenaskomplexet som för in pyruvat i TCA-cykeln. När PDHB-nivåerna sänks med CRISPR-redigering producerar cellerna mer laktat, mindre acetyl-CoA och har svårt att gå från stamceller mot endoderm och senare pankreasstadier. Omvänt förbättrar höjda PDHB-nivåer mitokondriell aktivitet, ökar cellernas energi och förbättrar effektiviteten i endodermdifferentiation, särskilt när själva TGFβ-signalen är svag.
Energinivåer styr tillgången till det genetiska manuset
Varför spelar detta val av bränsle så stor roll för cellens identitet? Författarna härleder effekten till ATP, cellens huvudsakliga energivaluta. Att blockera glukosnedbrytning eller mitokondrieinträde sänker ATP-nivåerna, och att helt enkelt tillföra extra ATP utifrån kan rädda misslyckad endodermdifferentiation i flera situationer. Den viktigaste ATP-konsumenten är BAF-komplexet, en stor ”kromatinombyggnadsmaskin” centrerad kring proteinet BRG1 som använder ATP för att öppna upp veckad DNA. När BAF kemiskt hämmas eller BRG1 degraderas eller muteras så att dess ATP-drivna motor inte längre fungerar, sviktar endodermbildningen och extra ATP kan inte längre hjälpa. Genom omfattande kartläggning av kromatinåtkomlighet visar de att när PDHB eller mitokondriellt pyruvatbruk minskas blir många regioner nära endodermrelaterade gener mindre åtkomliga, särskilt förstärkarregioner där BRG1 normalt binder.
Vad detta betyder för att bygga organ från celler
Tillsammans beskriver arbetet en tydlig händelsekedja: TGFβ-signaler höjer PDHB-nivåerna, PDHB leder pyruvat in i mitokondrierna, mitokondriell metabolism ökar ATP, och ATP driver BRG1-beroende öppning av nyckelregioner i DNA så att endodermgener kan aktiveras. I enkla termer bestämmer sättet tidiga mänskliga celler förbränner socker hur stort ”energibudget” de har för att låsa upp de delar av genomet som behövs för att bli tarm- och organbildande vävnad. Att förstå och kontrollera denna bränsleväxling kan förbättra metoder för att odla specifika mänskliga vävnader från stamceller för forskning, sjukdomsmodellering och framtida cellbaserade terapier.
Citering: Meng, L., Lv, J., Yi, Y. et al. TGFβ-activated PDHB promotes mitochondrial pyruvate metabolism and contributes to human endoderm differentiation via ATP-dependent BRG1. Nat Commun 17, 2846 (2026). https://doi.org/10.1038/s41467-026-69510-0
Nyckelord: stamcellsmetabolism, endodermdifferentiation, mitokondriellt pyruvat, kromatinombyggnad, TGF beta-signalering