Clear Sky Science · es
PDHB activado por TGFβ promueve el metabolismo mitocondrial del piruvato y contribuye a la diferenciación del endodermo humano mediante BRG1 dependiente de ATP
Cómo el uso de combustible moldea el desarrollo humano temprano
Nuestros cuerpos comienzan como pequeñas bolas de células madre que deben decidir en qué tipos de tejidos convertirse. Este estudio plantea una pregunta sorprendentemente concreta: ¿cómo influye la forma en que estas células tempranas queman azúcar en su decisión de formar órganos como el hígado, los pulmones y el páncreas? Al seguir el uso de energía y la regulación del ADN en paralelo, los investigadores muestran que un cambio específico en el metabolismo de los azúcares no es solo un telón de fondo, sino un motor activo del desarrollo humano temprano.
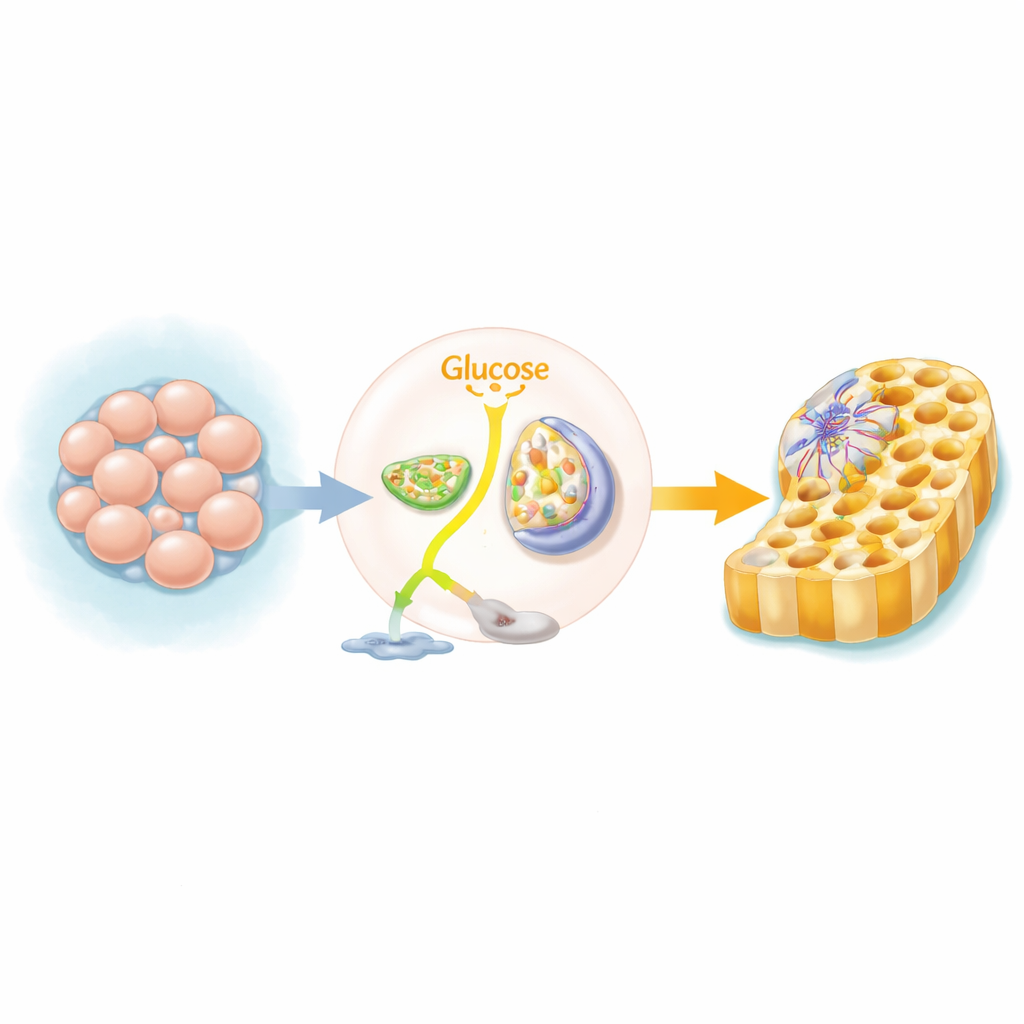
Un interruptor metabólico en tejidos en formación
Las células madre pluripotentes humanas, que pueden formar casi cualquier tejido, normalmente dependen de una vía rápida pero ineficiente para usar el azúcar, descomponiendo la glucosa hasta lactato incluso cuando hay oxígeno disponible. Cuando estas células empiezan a formar la capa de “endodermo definitivo”, el precursor del intestino, el hígado y el páncreas, cambian su ruta energética principal. En lugar de desviar el azúcar hacia el lactato, envían más de él a las mitocondrias, las centrales energéticas de la célula, para alimentar el ciclo del ácido tricarboxílico (TCA) y la fosforilación oxidativa. El equipo utilizó cribados CRISPR a escala del genoma y una batería de bloqueadores químicos para demostrar que cuando este cambio se bloquea, muchas menos células adoptan con éxito la identidad de endodermo.
Convertir el azúcar en potencia mitocondrial
En el centro de este cambio está el piruvato, un producto clave de la degradación de la glucosa. El piruvato puede convertirse en lactato o ser importado a las mitocondrias y transformarse en acetil-CoA, la entrada al ciclo TCA. Los investigadores encontraron que dirigir el piruvato hacia las mitocondrias favorece de forma contundente la formación del endodermo. Los fármacos que inhiben las enzimas que generan lactato empujan más piruvato hacia las mitocondrias y aumentan la diferenciación, mientras que los compuestos que impiden que el piruvato entre en las mitocondrias o se procese allí reducen drásticamente los marcadores de endodermo. Suplementar las células con piruvato o glutamina, otro combustible para el ciclo TCA, ayuda a restablecer esta vía de desarrollo cuando los pasos iniciales del uso de azúcares están bloqueados.
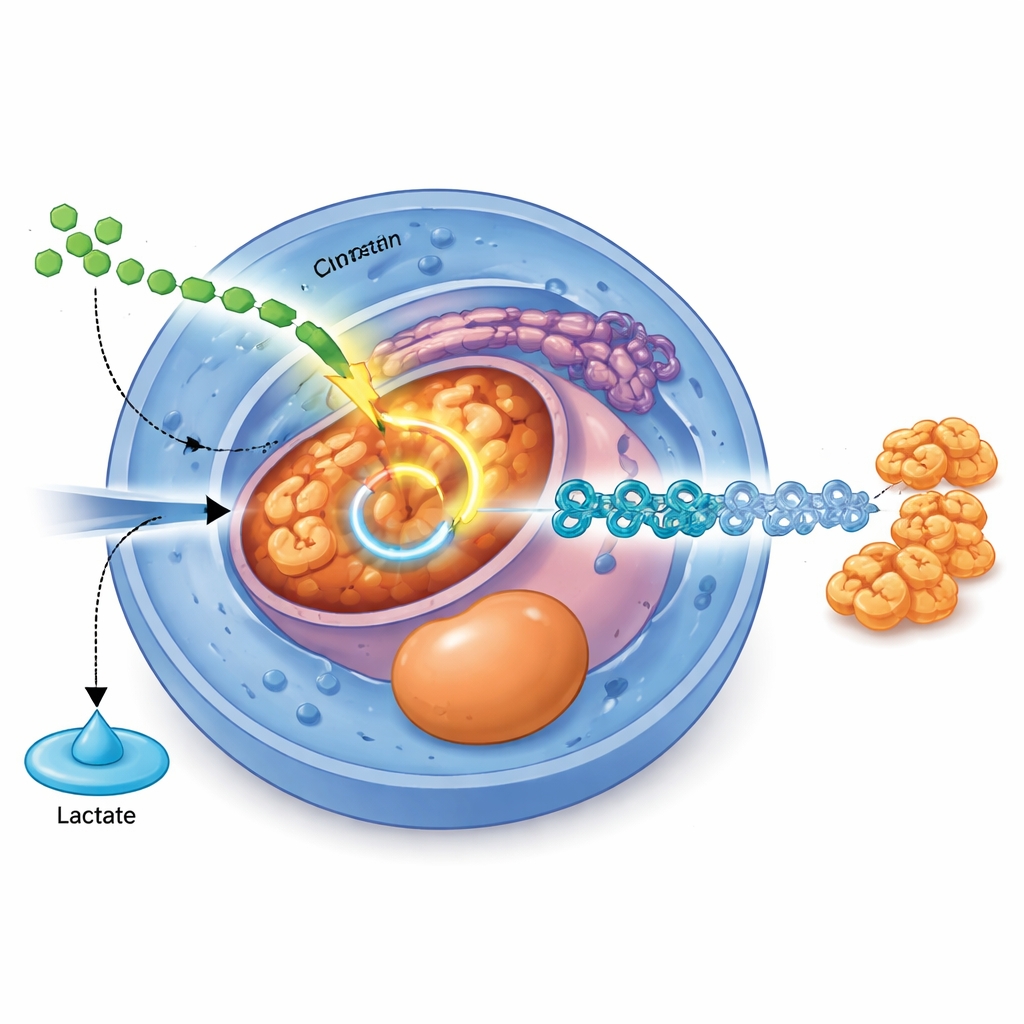
Una vía de señalización que reconfigura el metabolismo
El estudio identifica un interruptor molecular específico que vincula señales externas con este cambio interno en el uso de combustible. Una señal de crecimiento conocida como TGFβ, actuando a través de sus mensajeros SMAD2 y SMAD3, aumenta directamente la producción de PDHB, un componente central del complejo de la piruvato deshidrogenasa que canaliza el piruvato hacia el ciclo TCA. Cuando los niveles de PDHB se reducen mediante edición CRISPR, las células producen más lactato, menos acetil-CoA y tienen dificultades para avanzar desde las células madre hacia el endodermo y etapas pancreáticas posteriores. Por el contrario, aumentar los niveles de PDHB mejora la actividad mitocondrial, incrementa la energía celular y mejora la eficiencia de la diferenciación hacia endodermo, especialmente cuando la señal TGFβ en sí es débil.
Los niveles de energía controlan el acceso al guion genético
¿Por qué importa tanto esta elección de combustible para la identidad celular? Los autores rastrean el efecto hasta el ATP, la principal moneda energética de la célula. Bloquear la degradación de glucosa o la entrada mitocondrial reduce los niveles de ATP, y simplemente suministrar ATP adicional desde el exterior puede rescatar la diferenciación fallida del endodermo en varios contextos. El principal consumidor de ATP es el complejo BAF, una gran máquina de “remodelado de la cromatina” centrada en la proteína BRG1 que utiliza ATP para abrir el ADN plegado. Cuando BAF se inhibe químicamente o BRG1 se degrada o muta de modo que su motor dependiente de ATP deja de funcionar, la formación del endodermo se resiente y el ATP adicional ya no puede ayudar. Mapas genómicos de accesibilidad de la cromatina muestran que, cuando se reduce PDHB o el uso mitocondrial del piruvato, muchas regiones cercanas a genes relacionados con el endodermo se vuelven menos accesibles, especialmente regiones potenciadoras donde normalmente se une BRG1.
Qué significa esto para construir órganos a partir de células
En conjunto, el trabajo describe una cadena de eventos clara: las señales TGFβ elevan los niveles de PDHB, PDHB dirige el piruvato hacia las mitocondrias, el metabolismo mitocondrial aumenta el ATP y el ATP impulsa la apertura de regiones clave del ADN por BRG1 para que los genes del endodermo puedan activarse. En términos sencillos, la forma en que las células humanas tempranas queman azúcar determina cuánto “presupuesto energético” tienen para desbloquear las partes del genoma necesarias para convertirse en tejido formador de intestino y órganos. Entender y controlar este interruptor metabólico podría mejorar los métodos para cultivar tejidos humanos específicos a partir de células madre para investigación, modelos de enfermedad y, en última instancia, terapias celulares.
Cita: Meng, L., Lv, J., Yi, Y. et al. TGFβ-activated PDHB promotes mitochondrial pyruvate metabolism and contributes to human endoderm differentiation via ATP-dependent BRG1. Nat Commun 17, 2846 (2026). https://doi.org/10.1038/s41467-026-69510-0
Palabras clave: metabolismo de células madre, diferenciación del endodermo, piruvato mitocondrial, remodelado de la cromatina, señalización TGF beta