Clear Sky Science · he
PDHB שמופעל על-ידי TGFβ מקדם מטבוליזם מיצטונדריאלי של פירובט ותורם להבחנת האנדודרם האנושי דרך BRG1 התלוי ב-ATP
כיצד שימוש בדלק מעצב את ההתפתחות האנושית המוקדמת
גופנו מתחיל ככדורים זעירים של תאי גזע שצריכים להחליט לאילו רקמות להתפתח. המחקר הזה שואל שאלה מפתיעה ופשוטה: כיצד הדרך שבה תאים מוקדמים אלה “שרופים” את הסוכר משפיעה על החלטתם ליצור איברים כמו כבד, ריאות ולבלב? באמצעות מעקב מקביל אחרי שימוש באנרגיה ורגולציה של ה-DNA, החוקרים מראים שמעבר מטבולי ספציפי בסוכר אינו רק רקע אלא גורם פעיל בהתפתחות האנושית המוקדמת.
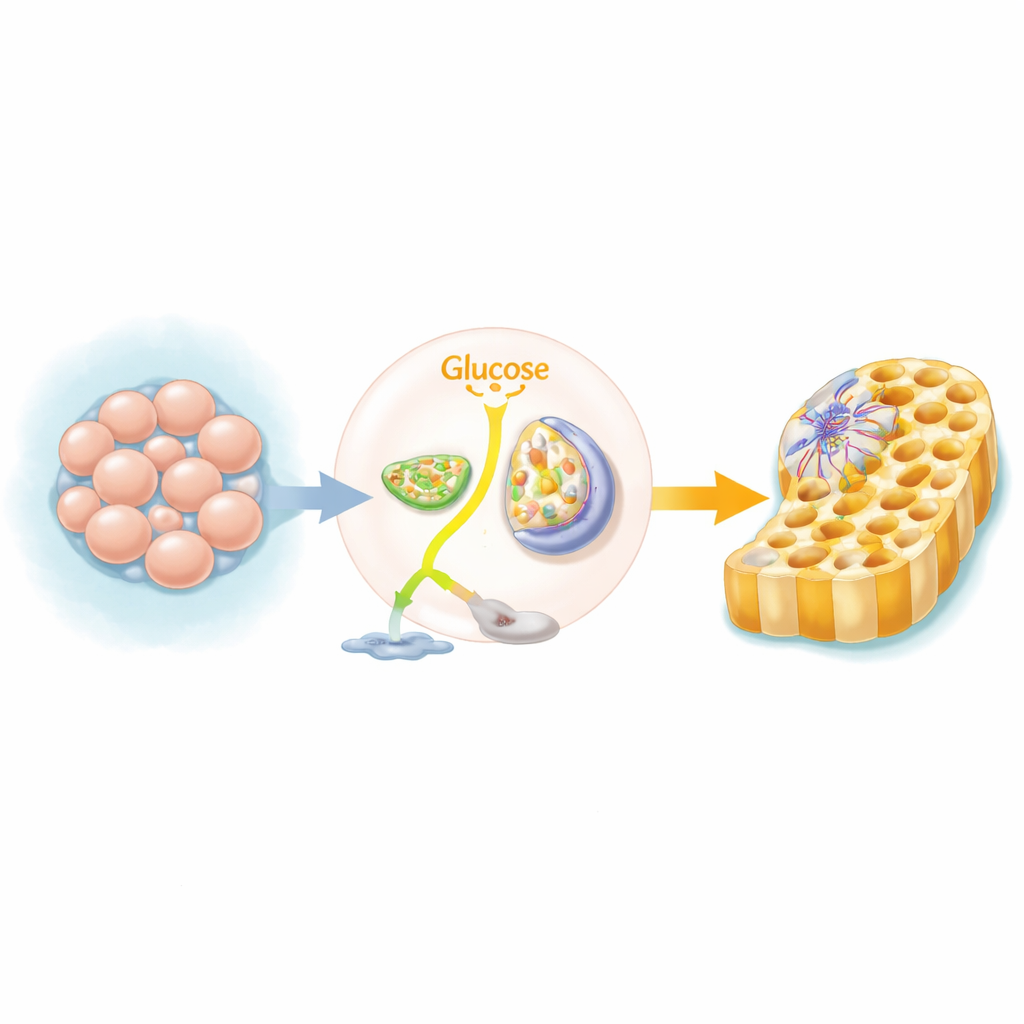
מתג מטבולי ברקמות הנביטות
תאי גזע פלוריפוטנטיים אנושיים, היכולים ליצור כמעט כל רקמה, בדרך כלל מסתמכים על דרך מהירה אך לא יעילה של עיבוד סוכר, המפרקת גלוקוז ללקטט גם בנוכחות חמצן. כאשר תאים אלה מתחילים ליצור את שכבת ה"אנדודרם הדפיניטיבי"—השלד המוקדם של המעי, הכבד והלבלב—הם מחליפים את מסלול הדלק העיקרי שלהם. במקום לשגר סוכר ללקטט הם שולחים יותר ממנו למיטוכונדריה, תחנות הכוח של התא, כדי להזין את מעגל ה-TCA ופוספורילציה חמצונית. הצוות השתמש בסקרי CRISPR ברמת הגנום ובמגוון חוסמים כימיים כדי להראות שכאשר המעבר הזה נחסם, מספר התאים שמפתחי זהות אנדודרמלית קטן משמעותית.
מהפיכת הסוכר לכוח מיטוכונדריאלי
לב המעבר הזה הוא פירובט, תוצר פירוק מפתח של גלוקוז. פירובט יכול או להיות מומת ללקטט או להיכנס למיטוכונדריה ולהיות מומר לאצטיל-CoA, הכרטיס הכניסה למעגל ה-TCA. החוקרים מצאו שכיוון פירובט למיטוכונדריה תומך בעוצמה ביצירת אנדודרם. תרופות המעכבות אנזימים היוצרים לקטט דוחפות יותר פירובט למיטוכונדריה ומשפרות את ההבחנה, בעוד תרכובות המונעות את כניסת הפירובט למיטוכונדריה או את עיבודו שם מפחיתות בחדות סמני אנדודרם. תוספת פירובט או גלוטמין, דלק נוסף למעגל ה-TCA, עוזרת לשחזר את מסלול ההתפתחות הזה כאשר צעדים מוקדמים של עיבוד סוכר נחסמים.
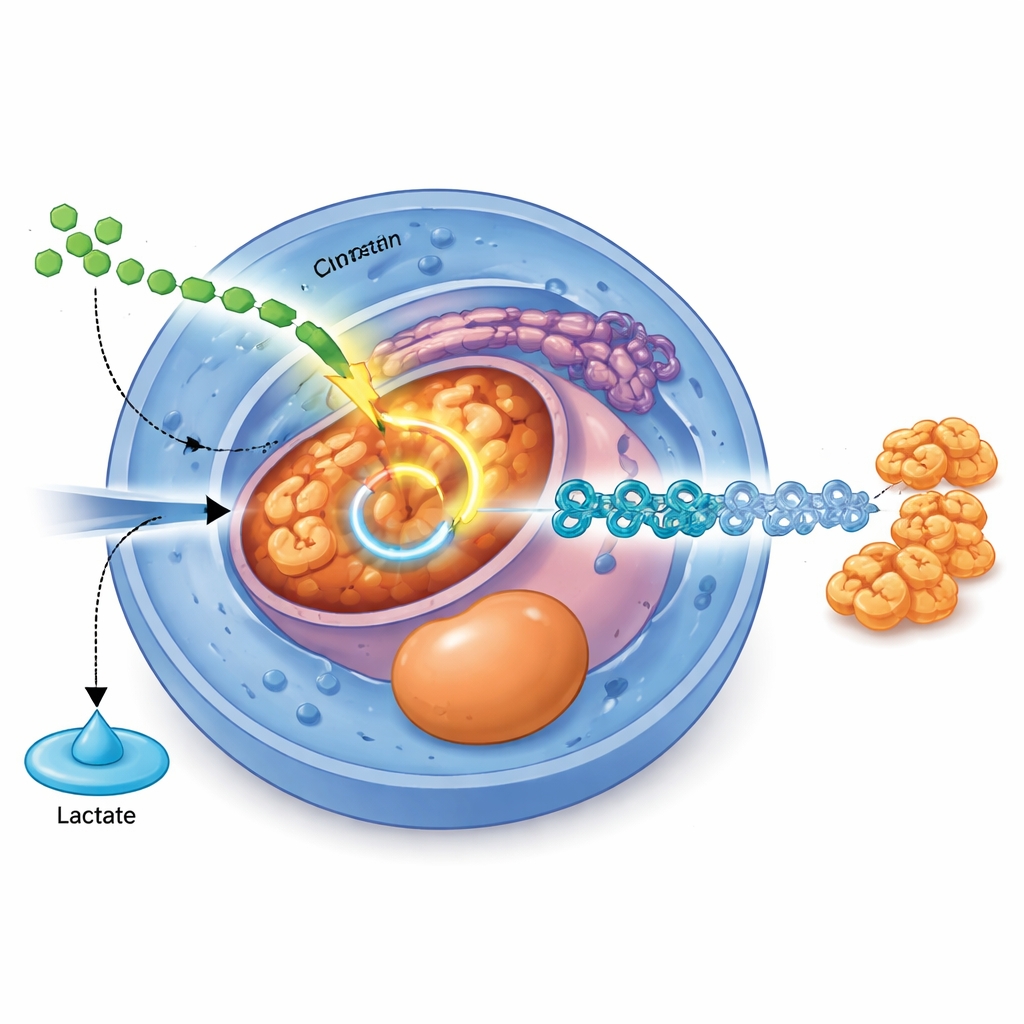
מסלול איתות שמעצב מחדש את המטבוליזם
המחקר מזהה מתג מולקולרי ספציפי המקשר אותות חיצוניים להסטה פנימית של האספקת הדלק. אות גדילה ידוע בשם TGFβ, הפועל דרך חלבוני שליח SMAD2 ו-SMAD3, מגביר ישירות את הייצור של PDHB, מרכיב מרכזי של קומפלקס פירובט דהידרוגנאז שמזין את הפירובט למעגל ה-TCA. כאשר רמות PDHB מוקטנות בעזרת עריכת CRISPR, תאים מייצרים יותר לקטט, פחות אצטיל-CoA, ונאבקים להתקדם מתאי גזע לכיוון האנדודרם ושלבים מואחרים של התפתחות הלבלב. מנגד, העלאת רמות PDHB משפרת את פעילות המיטוכונדריה, מעלה את רמת האנרגיה התאית ומשפרת את יעילות ההבחנה לאנדודרם, במיוחד כשהאות של TGFβ עצמו חלש.
רמות האנרגיה שולטות בנגישות לסקריפט הגנטי
מדוע בחירת דלק זו כה קריטית לזהות התא? המחברים מתחקים אחר האפקט עד ל-ATP, מטבע האנרגיה המרכזי של התא. חסימת פירוק הגלוקוז או כניסת המיטוכונדריה מורידים את רמות ה-ATP, ואספקת ATP חיצונית פשוטה יכולה להציל כישלון בהבחנת אנדודרם במצבים שונים. הצרכן העיקרי של ATP הוא קומפלקס BAF, מכונה גדולה של "עיבוד כרומטין" שמבוססת על החלבון BRG1 ומשתמשת ב-ATP כדי לפתוח DNA מקופל. כאשר BAF מעוכב כימית או ש-BRG1 מפורק או מוטנטי כך שמנוע ה-ATP שלו לא פועל, יצירת האנדודרם נחלשת ולא ניתן עוד להציל זאת בעזרת ATP חיצוני. מיפוי נגישות הכרומטין ברמת הגנום מראה שכאשר PDHB או השימוש הפירובט המיטוכונדריאלי מצומצמים, אזורים רבים הסמוכים לגנים הקשורים לאנדודרם נהיים פחות נגישים, במיוחד אזורי מאיצים שבהם BRG1 בדרך כלל נקשר.
מה המשמעות של זה לבניית איברים מתאים
במבט כולל, העבודה משרטטת שרשרת אירועים ברורה: אותות TGFβ מעלים רמות PDHB, PDHB מנתב פירובט למיטוכונדריה, מטבוליזם מיטוכונדריאלי מעלה ATP, ו-ATP מפעיל את פתיחת אזורי ה-DNA באמצעות BRG1 כך שגני אנדודרם יוכלו להידלק. במונחים פשוטים, האופן שבו תאים אנושיים מוקדמים צורכים סוכר קובע כמה "תקציב אנרגיה" יש להם כדי לשחרר את חלקי הגנום הנחוצים להפוך לרקמות מכילות מעי ואיברים. הבנת השליטה במתג הדלק הזה ושליטתו עשויה לשפר שיטות לגידול רקמות אנושיות ספציפיות מתאי גזע למטרות מחקר, דגמי מחלה ובסופו של דבר טיפולים תאיים.
ציטוט: Meng, L., Lv, J., Yi, Y. et al. TGFβ-activated PDHB promotes mitochondrial pyruvate metabolism and contributes to human endoderm differentiation via ATP-dependent BRG1. Nat Commun 17, 2846 (2026). https://doi.org/10.1038/s41467-026-69510-0
מילות מפתח: מטבוליזם של תאי גזע, הבחנת אנדודרם, פירובט מיטוכונדריאלי, עיבוד כרומטין, אותות TGF בטא