Clear Sky Science · zh
Ank3/ankyrin-G 中的神经元类型特异性微外显子调节钙活动和神经元兴奋性
微小的基因编辑如何塑造脑细胞行为
大脑依赖于兴奋神经元与抑制神经元之间的精细平衡来维持电路功能。本研究表明,一个极小的遗传片段——仅九个氨基酸——能帮助决定某些抑制性脑细胞的发放强度以及它们处理钙信号的方式。由于同一基因与躁郁症及其他脑病相关,理解这个微观开关有助于说明微小分子改动如何逐层放大影响行为和疾病风险。
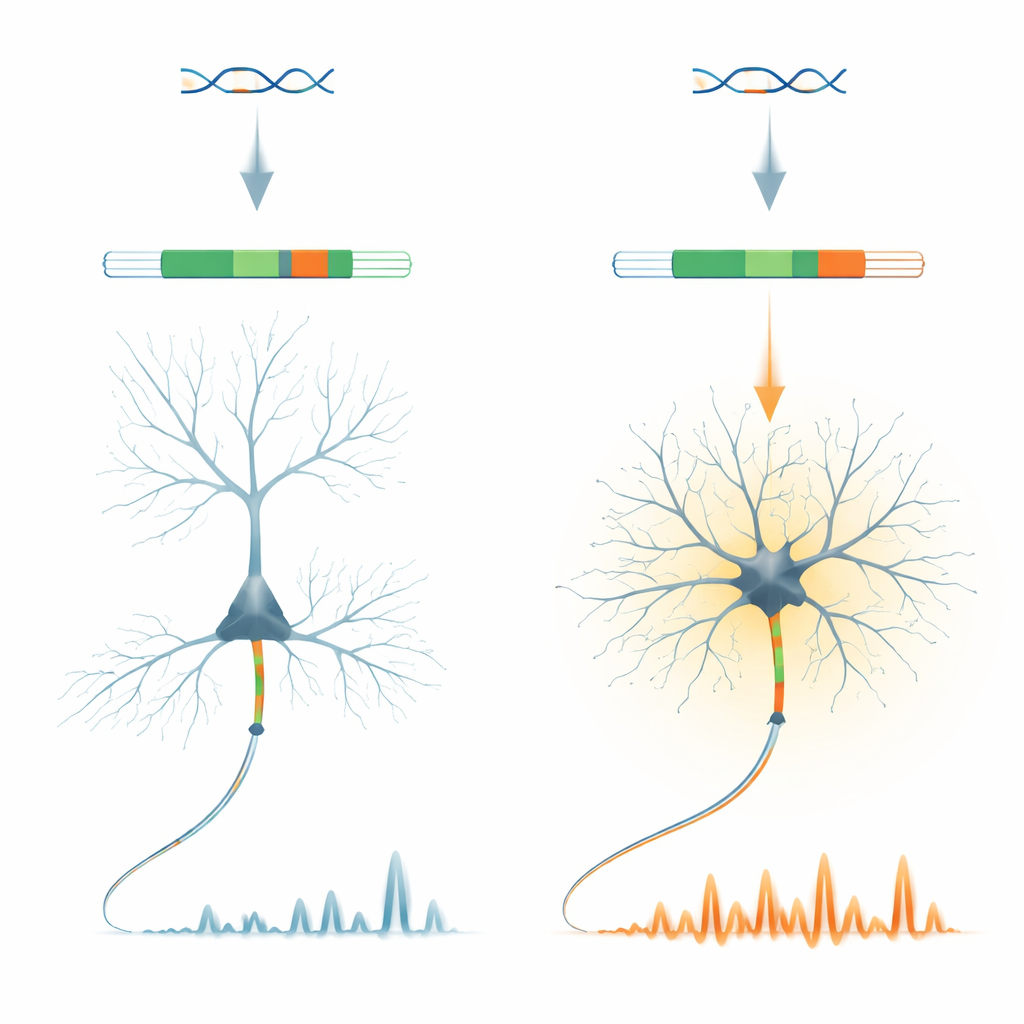
一个小型遗传开关却承担重大任务
研究者聚焦于一种名为 ankyrin-G 的蛋白,它是轴突起始段(神经信号首次生成的区域)的关键组织因子。在编码 ankyrin-G 的 Ank3 基因中,他们鉴定出一个非常短的“微外显子”称为 E35a。该片段在不同神经元类型中的使用差异显著:在皮质的兴奋性锥体神经元中多半被跳过,而在许多产生 GABA 的抑制性神经元以及小脑神经元中常常被包括进来。值得注意的是,这种模式在脊椎动物中得以保守,表明进化上强烈保留了这个神经元类型特异性的开/关开关。
不同脑细胞作出不同的剪接选择
细胞通过一组协调作用的 RNA 结合蛋白决定是否包含 E35a,从而控制原始 RNA 的切割与拼接。通过重新分析大规模数据集并在细胞中测试简化的“迷你基因”报告子,作者表明若干调控因子要么促进要么抑制 E35a 的被包含。其中一些调控因子在兴奋性神经元中更活跃,另一些在抑制性神经元中更突出,它们的综合作用产生了典型模式:许多抑制性细胞中包含率高,而大多数兴奋性细胞中包含率低。包含水平也可随神经元活动而变化,表明这一微小片段是一个对活动有响应的程序的一部分,可在电路成熟与放电过程中调整蛋白变体。
去除微外显子改变发放和钙信号
为探测 E35a 的实际作用,团队构建了删除该微外显子的转基因小鼠,使所有 ankyrin-G 分子都呈“短”型。这些动物生长和外表大体正常,但其抑制性神经元显示出显著变化。在脑切片中,前额皮层的快发放中间神经元发放更容易且频率更高,尽管轴突起始段的基本结构保持完整。在清醒小鼠中,双光子成像显示抑制性神经元的胞体钙活动大约是对照组的两倍,而邻近的兴奋性神经元仅有轻微变化。这表明该微外显子对某些抑制性细胞整合输入和调控胞内钙水平具有微调作用。
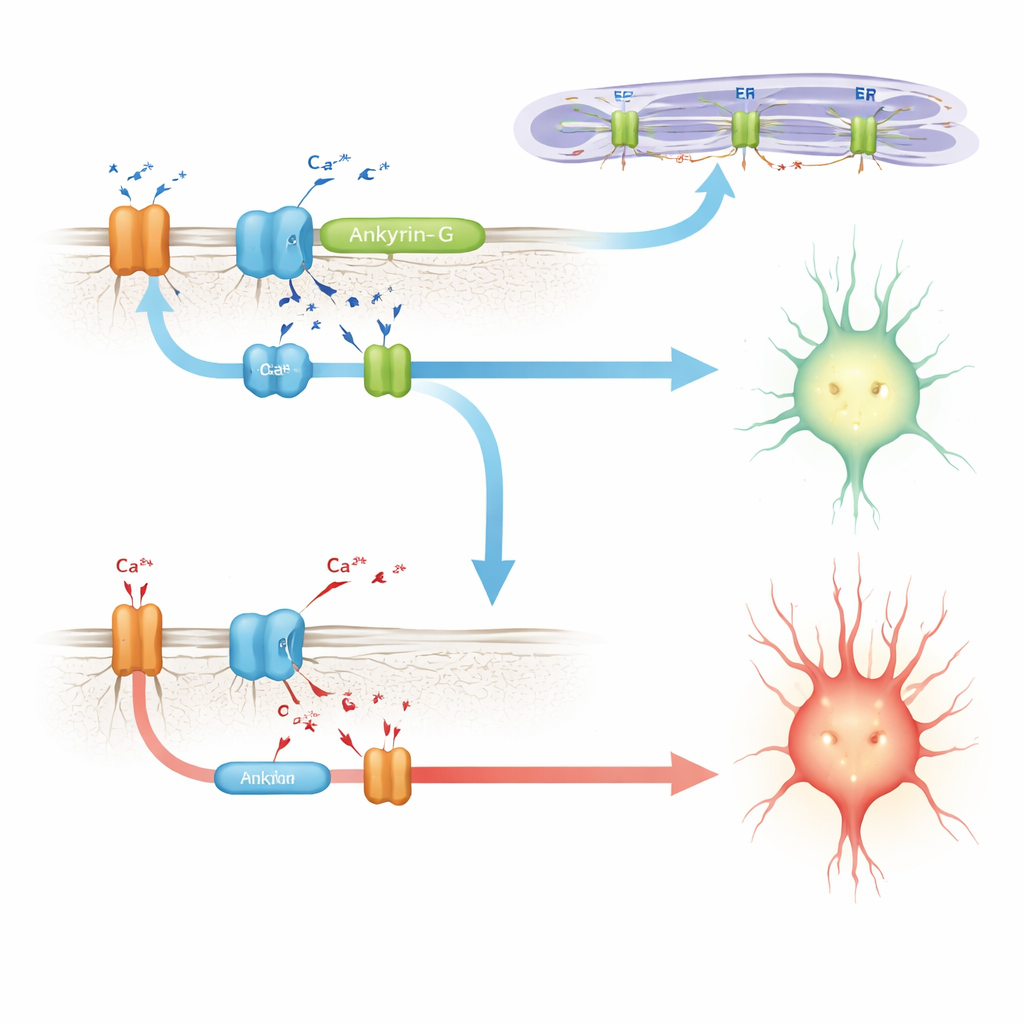
将 ankyrin-G 与钙处理机制联系起来
为寻找机制,作者参考了心肌细胞的早期工作:在心脏中,与之相关的蛋白 ankyrin-B 有助于组装一组钙处理组分的簇:钠钾泵、钠钙交换体以及内膜上的钙释放通道。该区域的病变会破坏该复合体并改变心脏钙节律。在这里,科学家们显示包含 E35a 的 ankyrin-G 会增强其与大脑中一组类似伙伴的相互作用,包括肌醇三磷酸受体和钠钾泵。在缺失 E35a 的小鼠中,这些相互作用明显减弱。在培养细胞中,包含 E35a 编码肽段的 ankyrin-G 变体比缺失该片段的变体能拉下更多的钙释放受体,支持了这样一种假设:该微外显子有助于在神经元中创建或稳定调控钙的微域。
从分子微调到行为
尽管在细胞水平上有明显变化,突变小鼠的行为影响却较为微妙。它们在协调性、焦虑样行为、简单记忆测试或社会交互上没有出现明显缺陷。然而,步态分析和活动量测量显示它们的运动略显更快、精力更充沛。作者提出更广泛的大脑网络可能对抑制性神经元兴奋性的改变进行补偿,从而在所用的行为学测试中掩盖了更明显的行为效应。即便如此,这些发现说明了一个小而神经元类型特异性的外显子如何在 ankyrin-G 的一般结构作用之外增加一层额外控制,调节特定回路中抑制和钙动力学的微调。
这对理解大脑为何重要
对非专业读者而言,关键信息是:大脑的多样性不仅在于哪些基因存在,还在于这些基因如何被灵活地在不同细胞中编辑为略有差异的版本。本研究表明,ankyrin-G 中的一个九个氨基酸插入充当了某些抑制性神经元兴奋性和钙信号的精密调节旋钮,而不会干扰它们发动信号区域的核心结构。由于 Ank3 基因与包括躁郁症在内的精神疾病有关,这些结果提供了一个机制性的线索,说明微小的 RNA 剪接变化如何可能改变回路平衡并影响疾病易感性,同时也强调了在心肌中已见到的钙调控策略在进化上的重复利用。
引用: Alam, S., Dermentzaki, G., Cabrera-Garcia, D. et al. A neuron type-specific microexon in Ank3/ankyrin-G modulates calcium activity and neuronal excitability. Nat Commun 17, 3173 (2026). https://doi.org/10.1038/s41467-026-69486-x
关键词: 可变剪接, ankyrin-G, GABA 能抑制性中间神经元, 钙信号, 神经元兴奋性