Clear Sky Science · es
Un microexón específico de tipo neuronal en Ank3/ankyrin-G modula la actividad del calcio y la excitabilidad neuronal
Cómo pequeñas ediciones genéticas moldean el comportamiento de las células cerebrales
El cerebro depende de un equilibrio delicado entre neuronas que excitaban los circuitos y otras que los calman. Este estudio muestra que un fragmento genético diminuto—apenas nueve bloques de construcción en una sola proteína—ayuda a determinar con qué intensidad disparan algunas células inhibidoras y cómo manejan las señales de calcio. Dado que el mismo gen está vinculado al trastorno bipolar y otras afecciones cerebrales, comprender este interruptor microscópico ofrece pistas sobre cómo ajustes moleculares sutiles pueden propagarse hasta afectar el comportamiento y el riesgo de enfermedad.
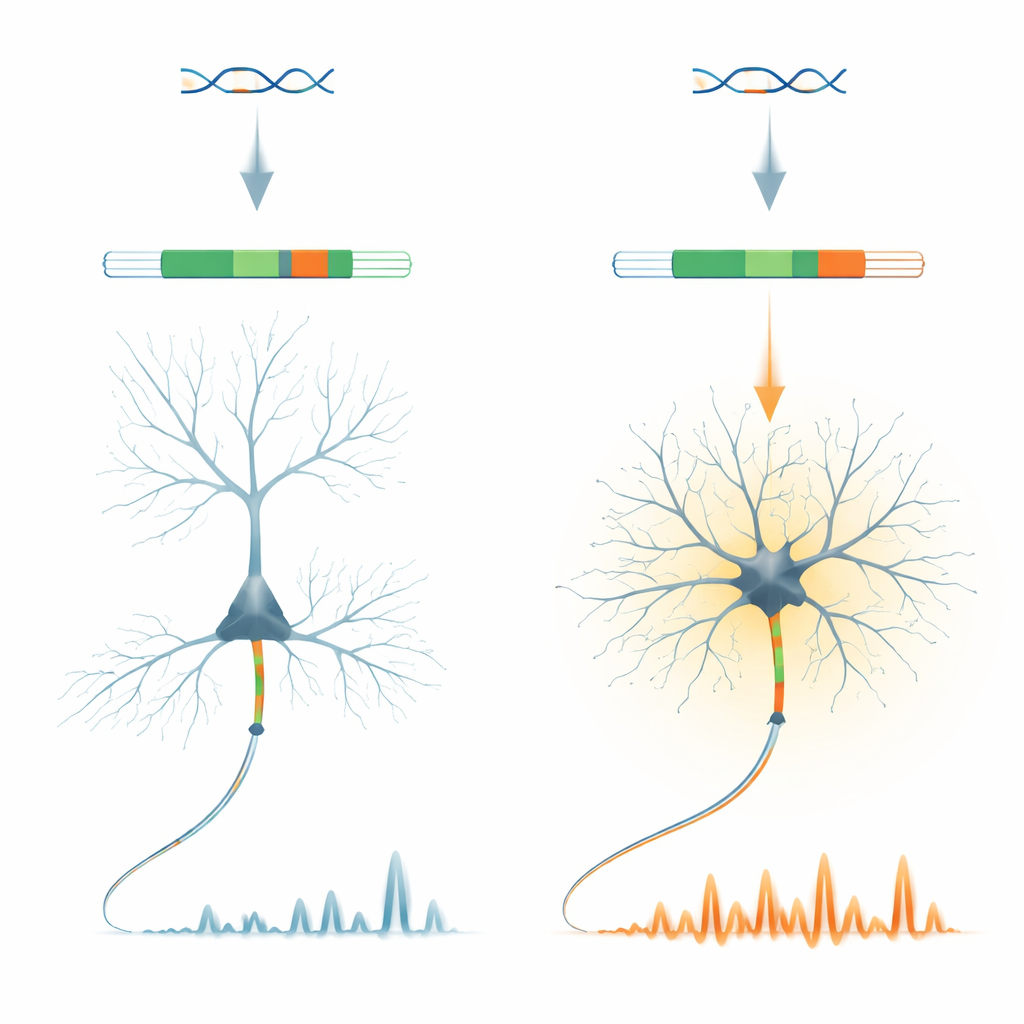
Un pequeño interruptor genético con una gran función
Los investigadores se centran en una proteína llamada ankyrin-G, un organizador clave de la región donde las señales nerviosas se generan por primera vez en un axón. Dentro del gen Ank3 que codifica la ankyrin-G, identifican un «microexón» muy corto denominado E35a. Este fragmento se usa de manera muy distinta según el tipo de neurona: suele excluirse en las neuronas piramidales excitadoras de la corteza, pero suele incluirse en muchas neuronas inhibitorias productoras de GABA y en neuronas cerebelosas. De forma notable, este patrón se conserva entre vertebrados, lo que sugiere que la evolución ha preservado fuertemente este interruptor on/off específico de tipo neuronal.
Diferentes células cerebrales, diferentes decisiones de empalme
Las células deciden si incluir E35a mediante una red coordinada de proteínas que se unen al ARN y controlan cómo se corta y se empalma el ARN primario. Al reanalizar grandes conjuntos de datos y probar un reportero simplificado de «minigen» en células, los autores muestran que varios reguladores promueven o bloquean la inclusión de E35a. Algunos de estos reguladores son más activos en neuronas excitadoras, otros en neuronas inhibidoras, y su acción combinada produce el patrón característico: alta inclusión en muchas células inhibitorias y baja inclusión en la mayoría de las excitadoras. El nivel de inclusión también puede cambiar con la actividad neuronal, lo que indica que este segmento minúsculo forma parte de un programa sensible a la actividad que ajusta las variantes proteicas a medida que los circuitos maduran y se activan.
Eliminar el microexón cambia el disparo y las señales de calcio
Para indagar qué hace realmente E35a, el equipo diseñó ratones en los que este microexón se elimina por completo, forzando a todas las moléculas de ankyrin-G a adoptar la forma «corta». Estos animales crecen y parecen generalmente normales, pero sus neuronas inhibitorias muestran cambios llamativos. En cortes cerebrales, las interneuronas de disparo rápido en la corteza frontal activan con más facilidad y a tasas más altas, aunque la arquitectura básica del segmento inicial del axón permanece intacta. En ratones despiertos, la imagen por dos fotones revela que las neuronas inhibitorias presentan aproximadamente el doble de actividad de calcio somática en comparación con los controles, mientras que las neuronas excitadoras cercanas muestran solo cambios menores. Esto indica que el microexón ajusta finamente cómo ciertas células inhibitorias integran entradas y controlan sus niveles internos de calcio.
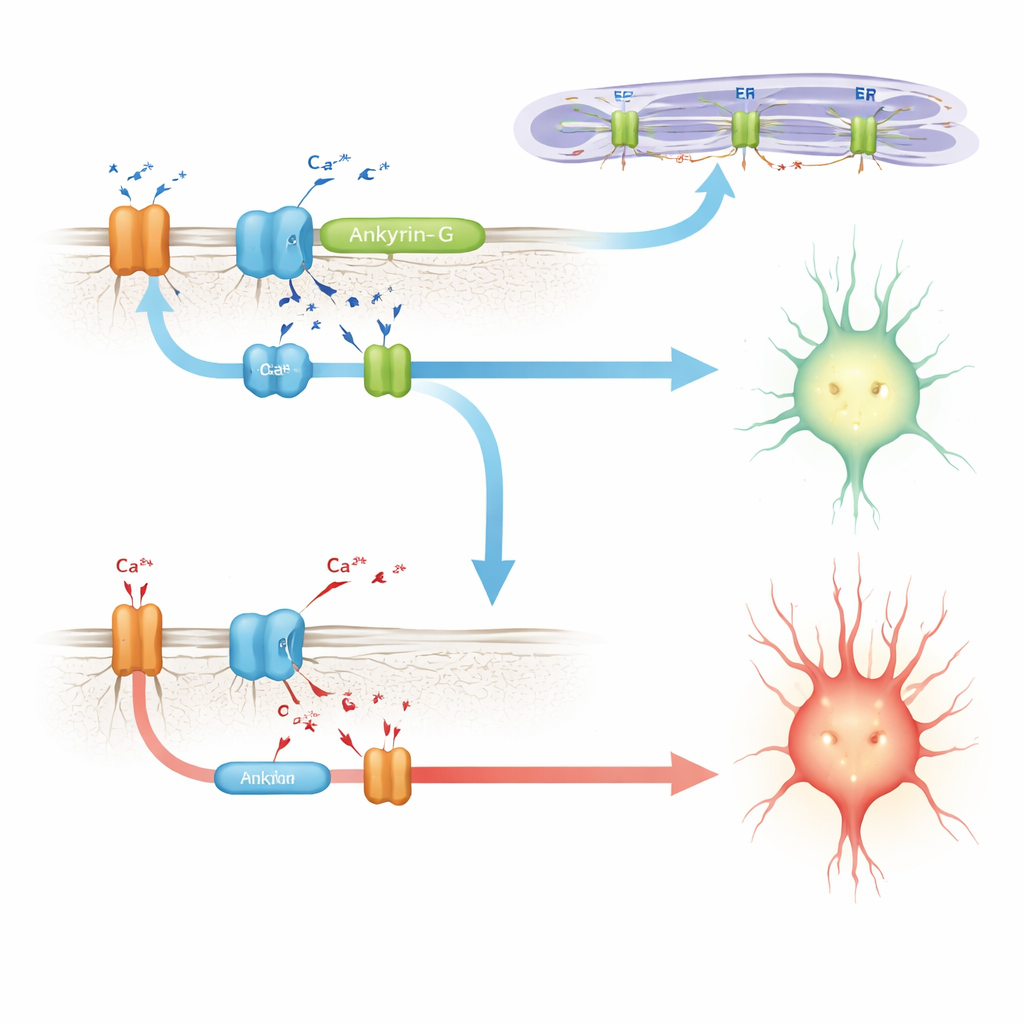
Conectando ankyrin-G con la maquinaria de manejo del calcio
Buscando un mecanismo, los autores recurren a trabajos previos en células cardíacas, donde una proteína relacionada, ankyrin-B, ayuda a ensamblar un conjunto de componentes que manejan el calcio: la bomba sodio–potasio, el intercambiador sodio–calcio y canales de liberación de calcio en membranas internas. Una mutación patológica en esa región desestabiliza el complejo y altera los ritmos de calcio cardíaco. Aquí, los científicos muestran que incluir E35a en ankyrin-G fortalece su interacción con un conjunto similar de asociados en el cerebro, incluido un receptor de inositol trifosfato y la bomba sodio–potasio. En ratones sin E35a, estas interacciones son notablemente más débiles. En células en cultivo, una versión de ankyrin-G que contiene el péptido codificado por E35a captura mucha más cantidad del receptor de liberación de calcio que una versión que carece de él, lo que apoya la idea de que este microexón ayuda a crear o estabilizar microdominios reguladores del calcio en las neuronas.
Del ajuste molecular fino al comportamiento
A pesar de los cambios claros a nivel celular, el impacto conductual en los ratones mutantes es sutil. No muestran déficits importantes en coordinación, comportamientos con rasgos ansiosos, memoria en pruebas simples o interacción social. Sin embargo, el análisis de la marcha y las medidas de actividad sugieren un movimiento levemente más rápido y enérgico. Los autores proponen que redes cerebrales más amplias pueden compensar la alterada excitabilidad de las neuronas inhibitorias, enmascarando efectos conductuales más dramáticos en los ensayos utilizados. Aun así, los hallazgos ilustran cómo un exón pequeño y específico de tipo neuronal puede añadir una capa extra de control sobre el papel estructural general de ankyrin-G, ajustando cómo se regulan la inhibición y la dinámica del calcio en circuitos concretos.
Por qué esto importa para entender el cerebro
Para no especialistas, el mensaje clave es que la diversidad del cerebro no depende solo de qué genes están presentes, sino también de cuán flexiblemente esos genes se editan en versiones ligeramente diferentes en distintas células. Este estudio muestra que una inserción de nueve aminoácidos en ankyrin-G actúa como un dial de precisión para la excitabilidad y la señalización del calcio de neuronas inhibitorias específicas, sin alterar la arquitectura central de su región de inicio de señales. Dado que el gen Ank3 está vinculado a condiciones psiquiátricas como el trastorno bipolar, estos resultados ofrecen una visión mecanicista de cómo cambios mínimos en el empalme del ARN podrían alterar el equilibrio de los circuitos e influir en la vulnerabilidad a la enfermedad, al tiempo que destacan la reutilización evolutiva de una estrategia de control del calcio ya observada previamente en el músculo cardíaco.
Cita: Alam, S., Dermentzaki, G., Cabrera-Garcia, D. et al. A neuron type-specific microexon in Ank3/ankyrin-G modulates calcium activity and neuronal excitability. Nat Commun 17, 3173 (2026). https://doi.org/10.1038/s41467-026-69486-x
Palabras clave: splicing alternativo, ankyrin-G, interneuronas GABAérgicas, señalización del calcio, excitabilidad neuronal