Clear Sky Science · ar
مُيكرواكسون خاص بنوع خلية عصبية في Ank3/أنكرين-G يعدّل نشاط الكالسيوم وقابلية إثارة الخلايا العصبية
كيف تشكّل تعديلات جينية ضئيلة سلوك خلية الدماغ
تعتمد الأدمغة على توازن دقيق بين الخلايا العصبية التي تثير الدوائر وتلك التي تهدئها. تُظهر هذه الدراسة أن شظية جينية صغيرة — مكوّنة من تسعة وحدات بناء فقط في بروتين واحد — تساعد في ضبط مدى شدة إطلاق بعض الخلايا المثبطة وكيفية تعاملها مع إشارات الكالسيوم. وبما أن نفس الجين مرتبط بالاضطراب ثنائي القطب وحالات دماغية أخرى، فإن فهم هذا المفتاح الميكروسكوبي يوفر دلائل على كيف يمكن لتعديلات جزيئية طفيفة أن تتصاعد لتؤثر على السلوك ومخاطر المرض.
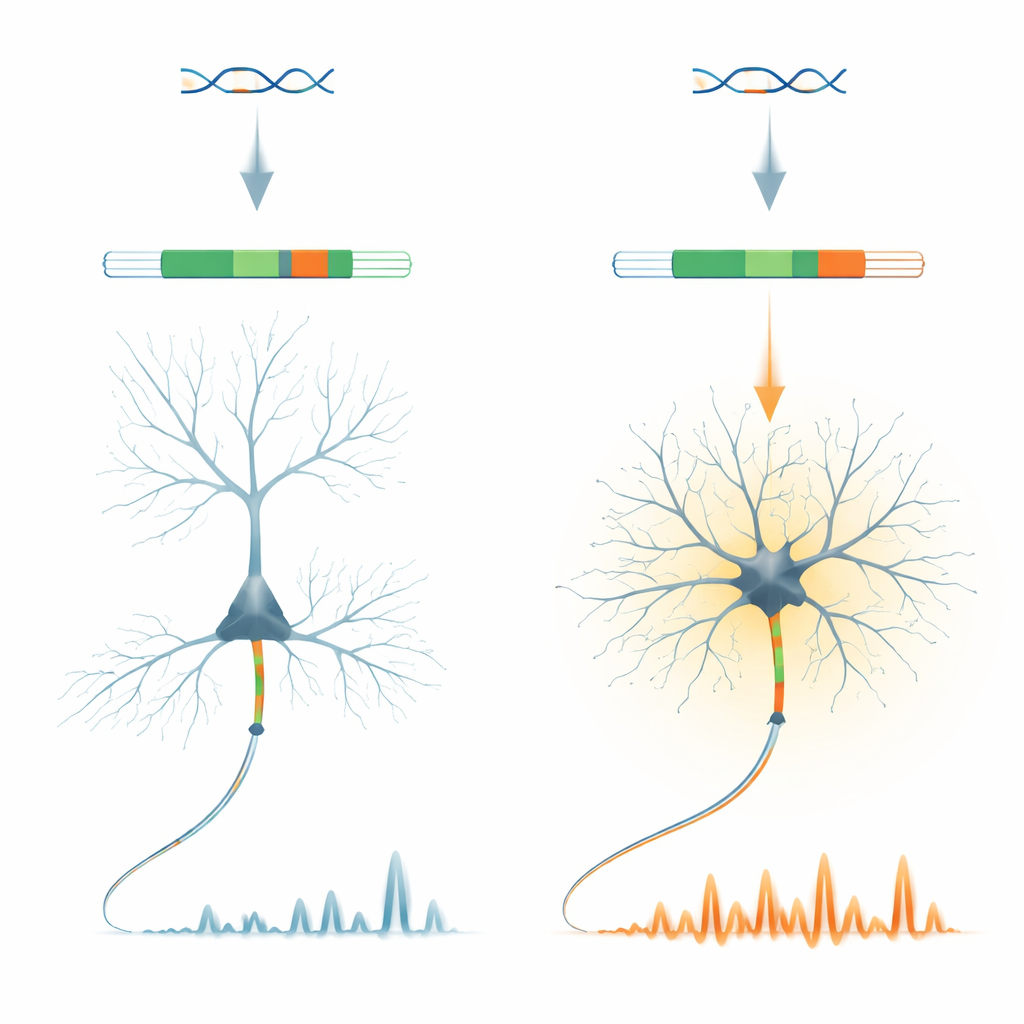
مفتاح جيني صغير لوظيفة كبيرة
يركّز الباحثون على بروتين يُدعى أنكرين-G، منظم رئيسي للمنطقة التي تُولد فيها الإشارات العصبية أولاً في المحور العصبي. داخل الجين Ank3 الذي يُشفّر أنكرين-G، حدّدوا «ميكرواكسون» قصير جداً يُسمى E35a. تُستخدم هذه الشريحة بشكل مختلف بشكل ملحوظ عبر أنواع الخلايا العصبية: فهي تُحذف في الغالب في الخلايا الهرمية المثيرة في القشرة، لكنها تُضمَّن عادةً في العديد من الخلايا المثبطة المنتجة لـ GABA وفي خلايا المخيخ. ومن اللافت أن هذا النمط محفوظ عبر الفقاريات، ما يشير إلى أن التطور حفظ هذا المفتاح التشغيلي النوعي للخلايا بقوة.
خلايا دماغية مختلفة، اختيارات معالجة بديلة مختلفة
تقرّر الخلايا ما إذا كانت ستضمّ E35a عبر شبكة من بروتينات ربط الرنا التي تتحكم في كيفية قطع وربط الحمض النووي الريبي الخام. من خلال تحليل مجموعات بيانات كبيرة وإجراء اختبارات باستخدام ناقل «مينيجين» مبسّط في الخلايا، يبيّن المؤلفون أن عدداً من المنظِّمات إما تعزّز أو تمنع إدراج E35a. بعض هذه المنظّمات أكثر نشاطاً في الخلايا المثيرة، وأخرى في الخلايا المثبطة، ويؤدي تراكب نشاطها إلى النمط المميز: إدراج مرتفع في العديد من الخلايا المثبطة، وإدراج منخفض في معظم الخلايا المثيرة. ويمكن أيضاً أن يتغير مستوى الإدراج مع نشاط العصبون، مما يدل على أن هذه الشريحة الصغيرة تُعد جزءاً من برنامج يستجيب للنشاط يضبط نسخ البروتين مع نضج وتيار دارات الشبكات.
حذف الميكرواكسون يغيّر الإطلاق وإشارات الكالسيوم
للبحث عما تفعله E35a عملياً، مهندس الفريق فئران حُذِف فيها هذا الميكرواكسون تماماً، مما اضطر جميع جزيئات أنكرين-G إلى الشكل «القصير». تنمو هذه الحيوانات وتبدو عموماً طبيعية، لكن خلاياها المثبطة تظهر تغييرات لافتة. في شرائح الدماغ، تطلق الخلايا البينية سريعة الإطلاق في القشرة الأمامية نبضات أسهل وبمعدلات أعلى، على الرغم من أن البنية الأساسية لقطاع بداية المحور العصبي تظل سليمة. في فئران يقظة، تكشف صور ثنائية الفوتون أن الخلايا المثبطة تُظهر نشاط كالسيوم جسدي تقريباً مضاعفاً مقارنةً بالمقاييس، بينما تُظهر الخلايا المثيرة المجاورة تغييرات طفيفة فقط. يشير هذا إلى أن الميكرواكسون يضبط بدقة كيفية تكامل مدخلات بعض الخلايا المثبطة وكيفية تحكمها في مستويات الكالسيوم الداخلية.
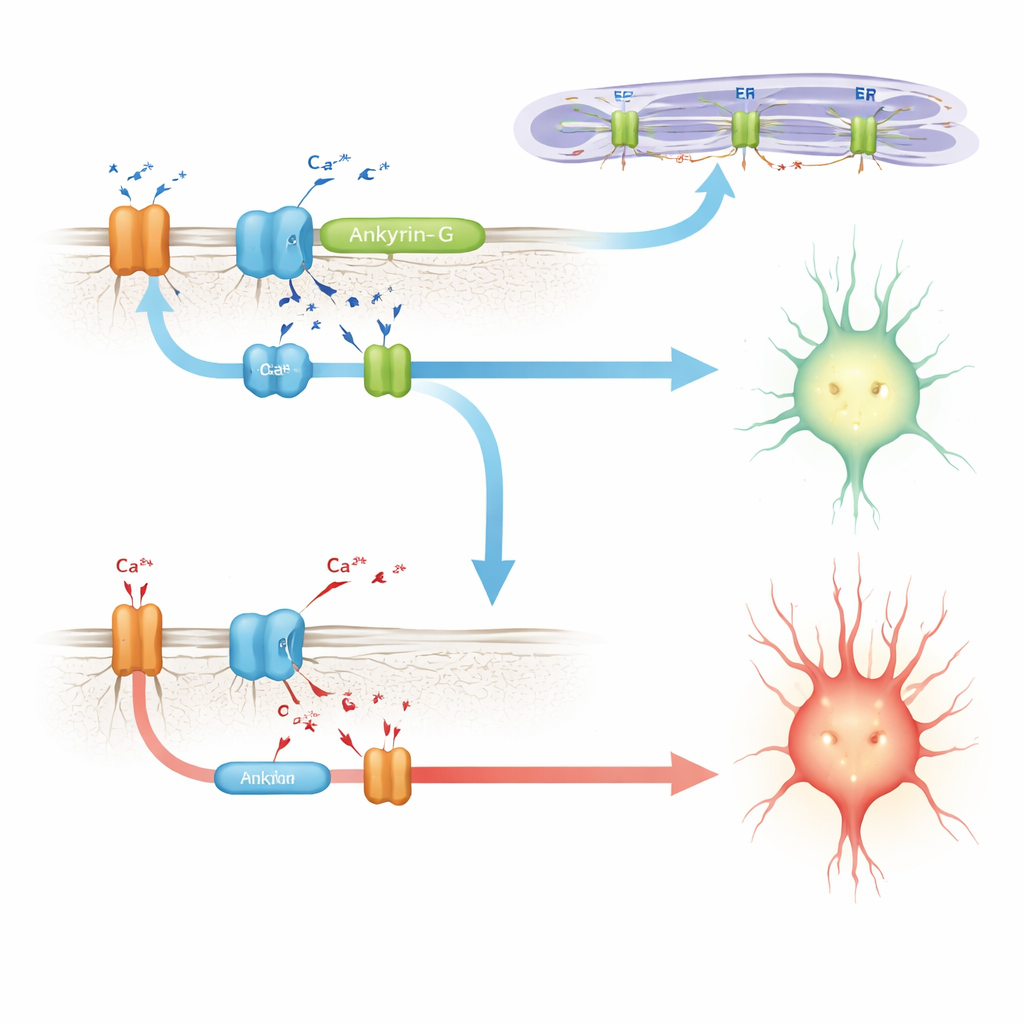
ربط أنكرين-G بآلات إدارة الكالسيوم
باحثين يبحثون عن آلية يتجهون إلى أعمال سابقة في خلايا القلب، حيث يساعد بروتين شبيه، أنكرين-B، في تجميع مجموعة من مكونات إدارة الكالسيوم: مضخة الصوديوم–البوتاسيوم، مبادل الصوديوم–الكالسيوم، وقنوات إطلاق الكالسيوم على الأغشية الداخلية. طفرة مرضية في تلك المنطقة تعطل هذا المجمع وتغيّر إيقاعات الكالسيوم القلبية. هنا، يُظهر العلماء أن إدراج E35a في أنكرين-G يقوّي تفاعله مع مجموعة مشابهة من الشركاء في الدماغ، بما في ذلك مستقبل ثلاثي فوسفات الإينوزيتول ومضخة الصوديوم–البوتاسيوم. في الفئران التي تفتقر إلى E35a، تكون هذه التفاعلات أضعف بشكل ملحوظ. في خلايا مزروعة، نسخة من أنكرين-G تحتوي على الببتيد المشفّر بواسطة E35a تسحب كمية أكبر بكثير من مستقبل إطلاق الكالسيوم مقارنةً بنسخة تفتقر إليه، مما يدعم الفكرة أن هذا الميكرواكسون يساعد في إنشاء أو استقرار ميكروفواصل تنظيم الكالسيوم في الخلايا العصبية.
من الضبط الجزيئي إلى السلوك
على الرغم من التغييرات الواضحة على مستوى الخلايا، فإن التأثير السلوكي في الفئران الطافرة طفيف. فهي لا تظهر عجزاً كبيراً في التناسق، أو سلوك يشبه القلق، أو ذاكرة في اختبارات بسيطة، أو تفاعل اجتماعي ملحوظ. ومع ذلك، تشير تحليلات المشية ومقاييس النشاط إلى حركة أسرع وخالية أكثر نشاطاً بشكل طفيف. يقترح المؤلفون أن الشبكات الدماغية الأوسع قد تعوّض عن قابلية إثارة الخلايا المثبطة المتغيرة، ما يخفي تأثيرات سلوكية أكثر دراماتيكية في الاختبارات المستخدمة. ومع ذلك، توضح النتائج كيف يمكن لواكسون صغير، نوعي للخلايا العصبية، أن يضيف طبقة تحكّم إضافية فوق الدور البنيوي العام لأنكرين-G، مضبطاً كيفية تهيئة التثبيط وديناميكيات الكالسيوم في دوائر معينة.
لماذا يهم هذا لفهم الدماغ
للغير متخصصين، الرسالة الأساسية هي أن تنوّع الدماغ لا يتعلق فقط بوجود جينات معينة، بل أيضاً بمدى مرونة تحرير تلك الجينات إلى نسخ متباينة قليلاً في خلايا مختلفة. تُظهر هذه الدراسة أن إدراج تسعة أحماض أمينية في أنكرين-G يعمل كقرص دقيق لقابلية الإثارة وإشارات الكالسيوم في خلايا مثبطة محددة، من دون أن يزعزع البنية الأساسية لمنطقة إطلاق الإشارة. وبما أن جين Ank3 مرتبط بحالات نفسية مثل الاضطراب ثنائي القطب، تقدّم هذه النتائج لمحة آلية عن كيف يمكن لتغييرات طفيفة في تطعيم الرنا أن تحوّل توازن الدوائر وتؤثر في القابلية للمرض، مع إبراز إعادة استخدام تطوري لاستراتيجية ضبط الكالسيوم شوهدت سابقاً في عضلة القلب.
الاستشهاد: Alam, S., Dermentzaki, G., Cabrera-Garcia, D. et al. A neuron type-specific microexon in Ank3/ankyrin-G modulates calcium activity and neuronal excitability. Nat Commun 17, 3173 (2026). https://doi.org/10.1038/s41467-026-69486-x
الكلمات المفتاحية: التطعيم البديل للنسخ, أنكرين-G, الخلايا العصبية البينية المفرِزة لـ GABA, إشارة الكالسيوم, قابلية إثارة العصبون