Clear Sky Science · pt
Um microéxon específico de tipo neuronal em Ank3/ankyrin-G modula a atividade de cálcio e a excitabilidade neuronal
Como pequenas edições genéticas moldam o comportamento das células cerebrais
Os cérebros dependem de um equilíbrio delicado entre células nervosas que excitam os circuitos e aquelas que os acalmam. Este estudo mostra que um fragmento genético minúsculo — apenas nove blocos de construção em uma única proteína — ajuda a definir com que intensidade algumas células cerebrais inibitórias disparam e como elas gerenciam sinais de cálcio. Como o mesmo gene está associado ao transtorno bipolar e outras condições cerebrais, entender esse interruptor microscópico oferece pistas de como ajustes moleculares sutis podem repercutir no comportamento e no risco de doença.
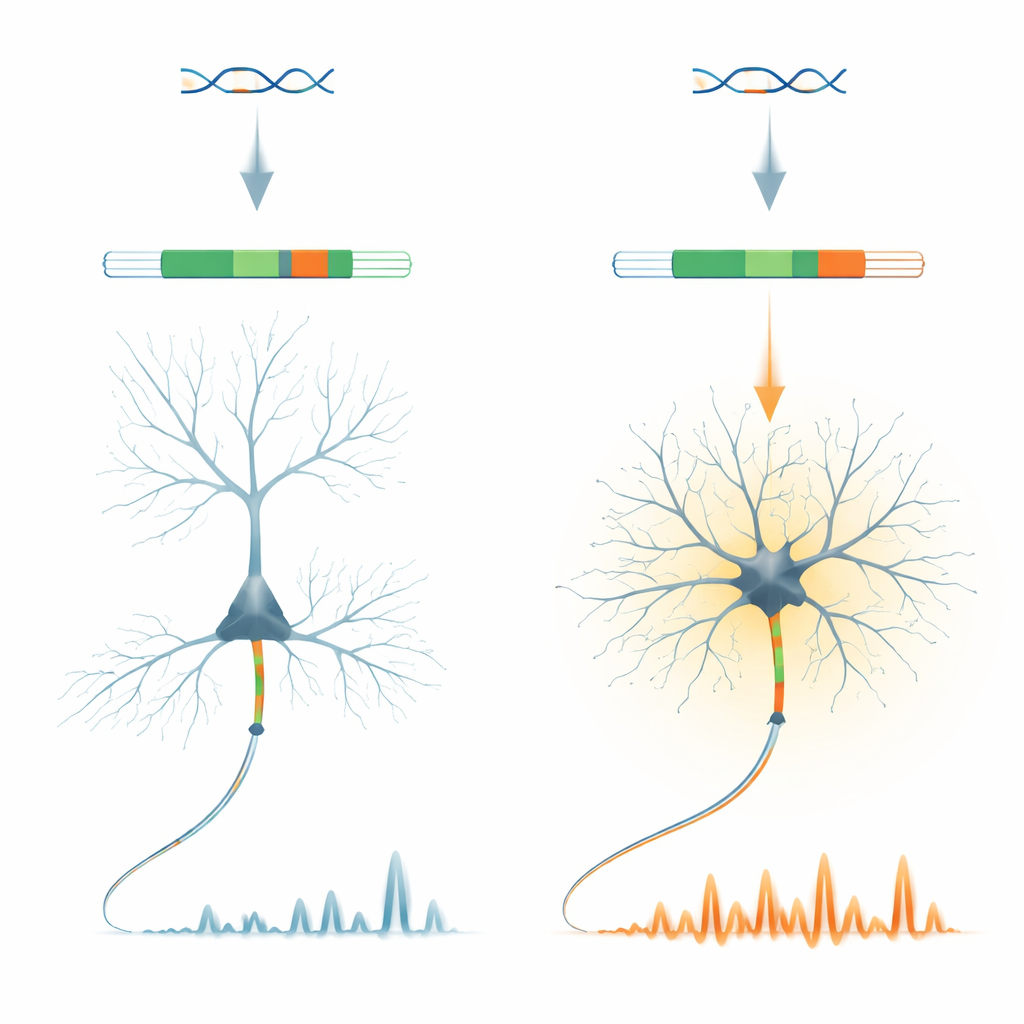
Um pequeno interruptor genético com grande função
Os pesquisadores focam em uma proteína chamada ankyrin-G, um organizador chave da região onde os sinais nervosos são gerados pela primeira vez em um axônio. No gene Ank3 que codifica a ankyrin-G, eles identificam um "microéxon" muito curto chamado E35a. Esse trecho é usado de maneiras bem distintas entre tipos de neurônios: é majoritariamente excluído em neurônios piramidais excitatórios do córtex, mas comumente incluído em muitos neurônios inibitórios produtores de GABA e em neurônios do cerebelo. Notavelmente, esse padrão é conservado entre vertebrados, sugerindo que a evolução preservou fortemente esse interruptor ligado ao tipo celular.
Diferentes células cerebrais, escolhas de splicing diferentes
As células decidem incluir ou não E35a por meio de uma rede coordenada de proteínas ligadoras de RNA que controlam como o RNA primário é cortado e emendado. Ao reanalisar grandes conjuntos de dados e testar um repórter “minigene” simplificado em células, os autores mostram que vários reguladores promovem ou bloqueiam a inclusão de E35a. Alguns desses reguladores são mais ativos em neurônios excitatórios, outros em inibitórios, e a ação combinada deles produz o padrão característico: alta inclusão em muitos neurônios inibitórios e baixa inclusão na maioria dos neurônios excitatórios. O nível de inclusão também pode mudar com a atividade neuronal, indicando que esse segmento minúsculo faz parte de um programa sensível à atividade que ajusta variantes proteicas à medida que os circuitos amadurecem e disparam.
Remover o microéxon altera disparos e sinais de cálcio
Para investigar o que E35a realmente faz, a equipe criou camundongos nos quais esse microéxon foi completamente deletado, forçando todas as moléculas de ankyrin-G para a forma "curta". Esses animais crescem e parecem, de modo geral, normais, mas seus neurônios inibitórios exibem mudanças marcantes. Em fatias cerebrais, interneurônios de disparo rápido no córtex frontal disparam mais facilmente e em taxas mais altas, apesar de a arquitetura básica do segmento inicial do axônio permanecer intacta. Em camundongos acordados, imagem por dois fótons revela que os neurônios inibitórios têm aproximadamente o dobro da atividade de cálcio somático em comparação com controles, enquanto neurônios excitatórios próximos mostram apenas mudanças pequenas. Isso indica que o microéxon ajusta com precisão como certos neurônios inibitórios integram entradas e regulam seus níveis internos de cálcio.
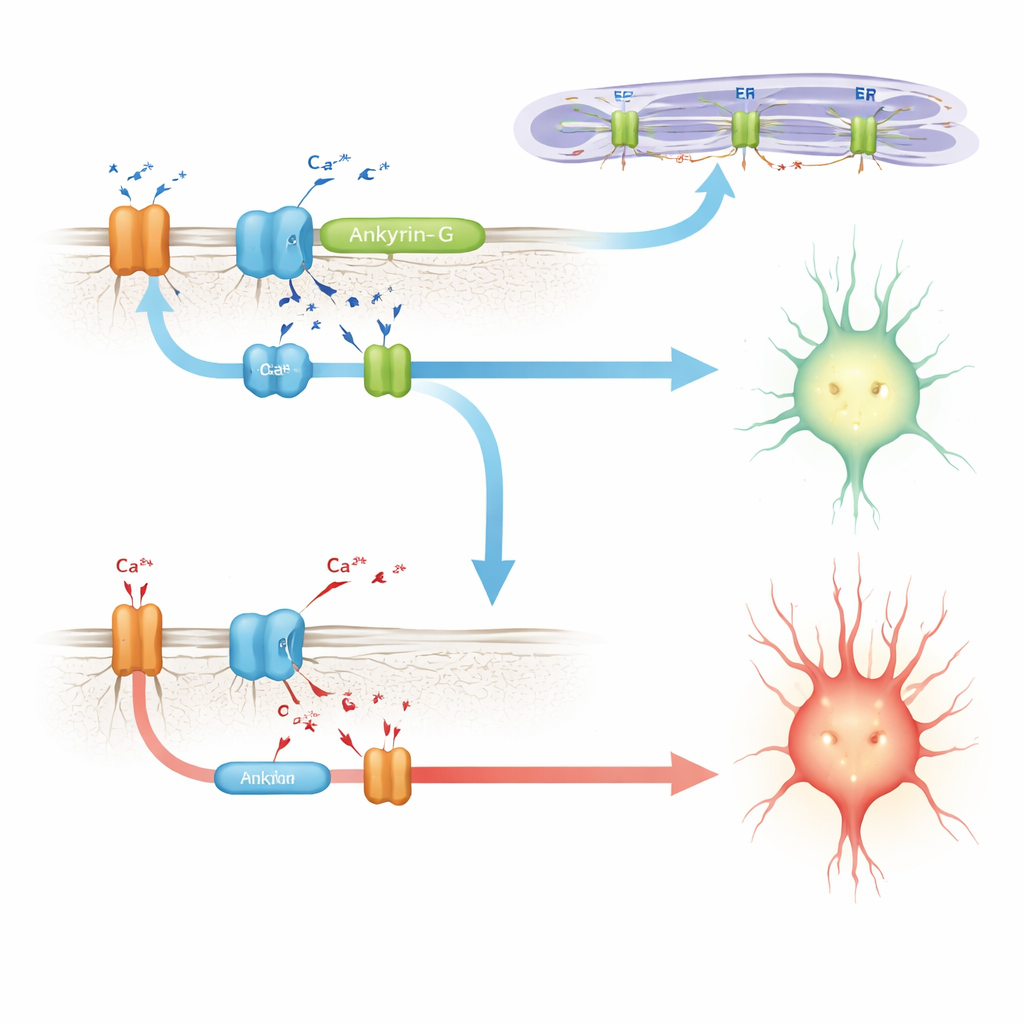
Ligando a ankyrin-G à maquinaria de manejo do cálcio
Buscando um mecanismo, os autores recorrem a trabalhos anteriores em células cardíacas, onde uma proteína relacionada, a ankyrin-B, ajuda a montar um conjunto de componentes de manejo do cálcio: a bomba sódio–potássio, o trocador sódio–cálcio e canais de liberação de cálcio em membranas internas. Uma mutação dessa região em doenças desorganiza o complexo e altera os ritmos de cálcio cardíacos. Aqui, os cientistas mostram que a inclusão de E35a na ankyrin-G fortalece sua interação com um conjunto semelhante de parceiros no cérebro, incluindo um receptor de inositol trifosfato e a bomba sódio–potássio. Em camundongos sem E35a, essas interações são visivelmente mais fracas. Em células em cultura, uma versão da ankyrin-G que contém o peptídeo codificado por E35a puxa muito mais do receptor de liberação de cálcio do que uma versão que o omite, sustentando a ideia de que esse microéxon ajuda a criar ou estabilizar microdomínios reguladores de cálcio em neurônios.
Do ajuste molecular ao comportamento
Apesar das mudanças claras no nível celular, o impacto comportamental nos camundongos mutantes é sutil. Eles não apresentam déficits importantes em coordenação, comportamentos análogos à ansiedade, memória em testes simples ou interação social. No entanto, análises de marcha e medidas de atividade sugerem movimentos levemente mais rápidos e enérgicos. Os autores propõem que redes cerebrais mais amplas podem compensar a excitabilidade alterada dos neurônios inibitórios, mascarando efeitos comportamentais mais dramáticos nos testes utilizados. Ainda assim, os achados ilustram como um pequeno éxon específico de tipo neuronal pode adicionar uma camada extra de controle além do papel estrutural geral da ankyrin-G, ajustando como a inibição e a dinâmica do cálcio são reguladas em circuitos particulares.
Por que isso importa para entender o cérebro
Para não especialistas, a mensagem principal é que a diversidade do cérebro não se resume apenas a quais genes estão presentes, mas também a quão flexivelmente esses genes são editados em versões ligeiramente diferentes em células distintas. Este estudo mostra que uma inserção de nove aminoácidos na ankyrin-G age como um botão de precisão para a excitabilidade e a sinalização por cálcio de neurônios inibitórios específicos, sem perturbar a arquitetura central de sua região de disparo de sinais. Como o gene Ank3 está ligado a condições psiquiátricas como o transtorno bipolar, esses resultados oferecem um vislumbre mecanístico de como mudanças minúsculas no splicing de RNA podem deslocar o equilíbrio dos circuitos e influenciar a vulnerabilidade à doença, ao mesmo tempo em que destacam o reaproveitamento evolutivo de uma estratégia de controle do cálcio já observada em músculo cardíaco.
Citação: Alam, S., Dermentzaki, G., Cabrera-Garcia, D. et al. A neuron type-specific microexon in Ank3/ankyrin-G modulates calcium activity and neuronal excitability. Nat Commun 17, 3173 (2026). https://doi.org/10.1038/s41467-026-69486-x
Palavras-chave: emparelhamento alternativo, ankyrin-G, interneurônios GABAérgicos, sinalização por cálcio, excitabilidade neuronal