Clear Sky Science · pl
Neuronowy typ-specyficzny microekson w Ank3/ankyrin-G modyfikuje aktywność wapniową i pobudliwość neuronów
Jak drobne genetyczne korekty kształtują zachowanie komórek mózgu
Mózg opiera się na delikatnej równowadze między komórkami nerwowymi, które pobudzają obwody, a tymi, które je hamują. Badanie pokazuje, że maleńki fragment genetyczny — zaledwie dziewięć aminokwasów w pojedynczym białku — pomaga ustawić, jak silnie niektóre komórki hamujące się aktywują i jak radzą sobie z sygnałami wapniowymi. Ponieważ ten sam gen jest powiązany z chorobami psychicznymi, takimi jak zaburzenie dwubiegunowe, zrozumienie tego mikroskopijnego przełącznika daje wskazówki, jak subtelne modyfikacje molekularne mogą rozlewać się na poziom zachowania i ryzyka choroby.
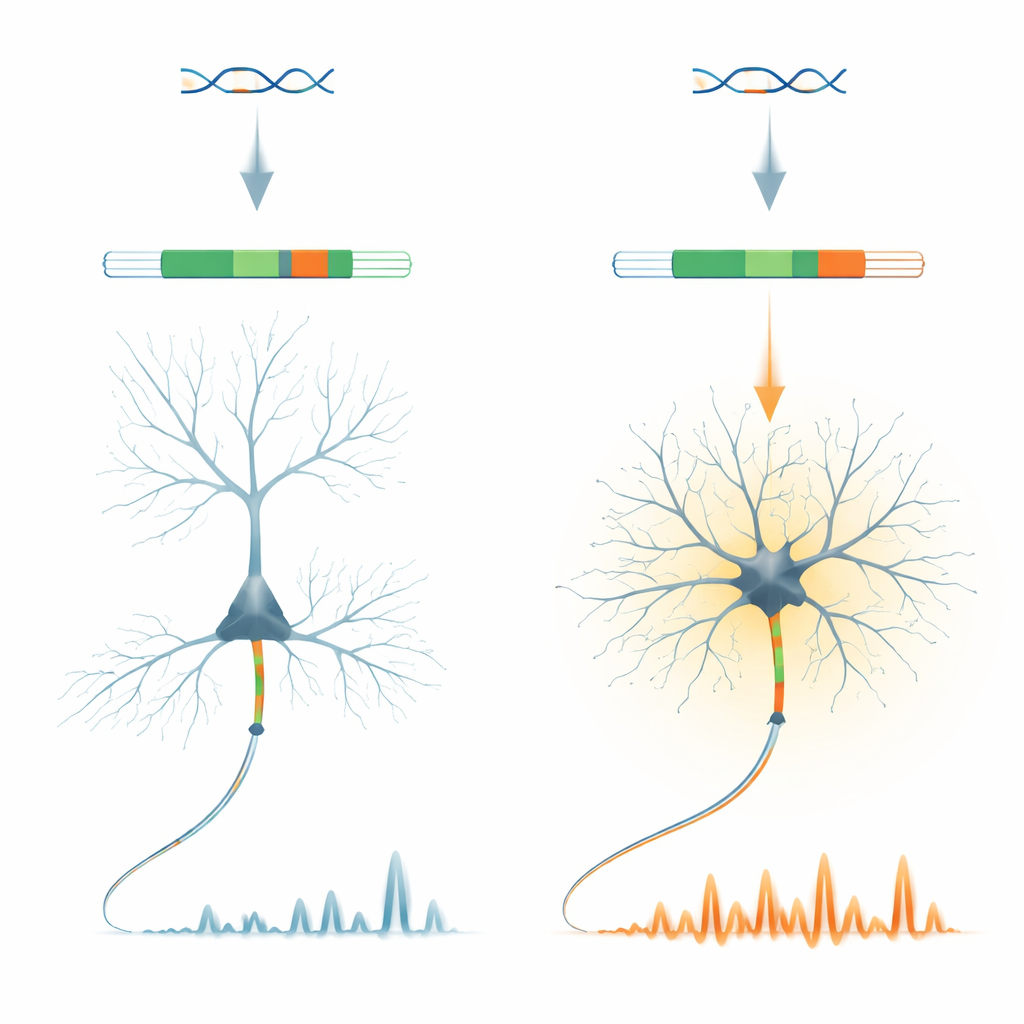
Mały genetyczny przełącznik o dużym zadaniu
Naukowcy koncentrują się na białku zwanym ankyrin-G, kluczowym organizatorze rejonu, gdzie w aksonie generowane są sygnały nerwowe. W genie Ank3 kodującym ankyrin-G identyfikują bardzo krótki „microekson” nazwany E35a. Ten fragment jest wykorzystywany bardzo różnie w różnych typach neuronów: przeważnie pomijany w pobudzających neuronach piramidowych kory, ale często włączany w wielu hamujących neuronach produkujących GABA oraz w komórkach móżdżku. Co istotne, ten wzorzec jest zachowany u kręgowców, co sugeruje, że ewolucja silnie utrwaliła ten neuronowy, typowo-specyficzny przełącznik on/off.
Różne komórki mózgu, różne wybory splicingu
Komórki decydują, czy włączyć E35a, dzięki skoordynowanej sieci białek wiążących RNA, które kontrolują cięcie i składanie surowego RNA. Poprzez ponowną analizę dużych zestawów danych i testowanie uproszczonego „minigenu” w komórkach, autorzy pokazują, że kilka regulatorów promuje lub blokuje włączenie E35a. Niektóre z tych regulatorów są bardziej aktywne w neuronach pobudzających, inne w hamujących, a ich skumulowane działanie daje charakterystyczny wzorzec: wysokie włączenie w wielu komórkach hamujących, niskie w większości komórek pobudzających. Poziom włączenia może również zmieniać się wraz z aktywnością neuronów, co wskazuje, że ten malutki segment jest częścią programu reagującego na aktywność, który dostraja warianty białek w miarę dojrzewania i aktywowania obwodów.
Usunięcie microeksonu zmienia wyładowania i sygnały wapniowe
Aby zbadać, co E35a rzeczywiście robi, zespół stworzył myszy, u których microekson jest całkowicie usunięty, zmuszając wszystkie cząsteczki ankyrin-G do „krótkiej” formy. Zwierzęta te rozwijają się i wyglądają na ogół normalnie, ale ich neurony hamujące wykazują uderzające zmiany. W preparatach mózgu interneurony szybko wyładowujące w korze przedczołowej wyładowują się łatwiej i z większą częstotliwością, mimo że podstawowa architektura początkowego segmentu aksonu pozostaje nienaruszona. U czujnych myszy obrazowanie dwufotonowe pokazuje, że neurony hamujące mają około dwukrotnie wyższą aktywność wapniową somy w porównaniu z kontrolami, podczas gdy pobliskie neurony pobudzające wykazują jedynie drobne zmiany. To wskazuje, że microekson dostraja sposób, w jaki konkretne neurony hamujące integrują sygnały i regulują swoje wewnętrzne poziomy wapnia.
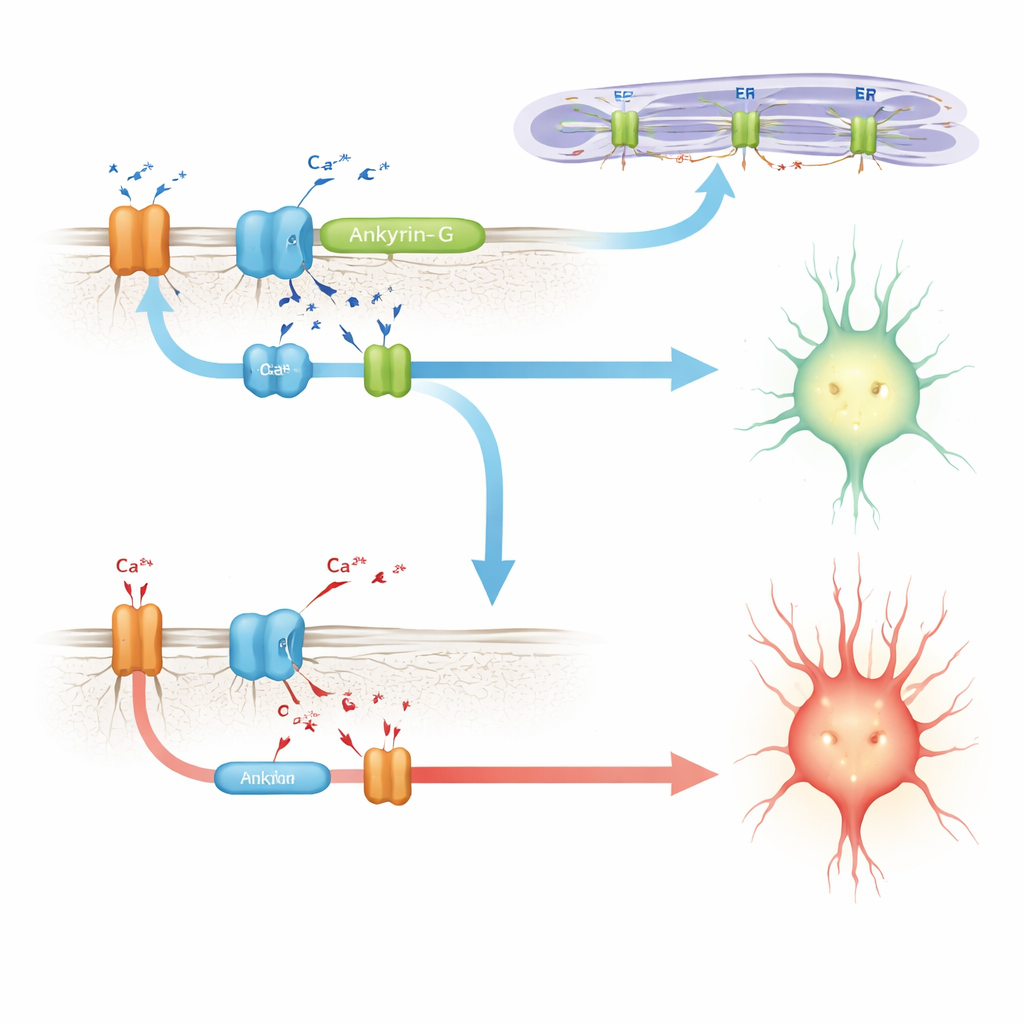
Łączenie ankyrin-G z aparatem obsługi wapnia
Szukając mechanizmu, autorzy odwołują się do wcześniejszych badań w komórkach serca, gdzie pokrewne białko, ankyrin-B, pomaga zmontować kompleks komponentów obsługujących wapń: pompę sodowo-potasową, wymiennik sodowo-wapniowy oraz kanały uwalniające wapń na błonach wewnętrznych. Mutacja związana z chorobą w tym regionie zaburza kompleks i zmienia rytmy wapniowe serca. Tutaj naukowcy pokazują, że włączenie E35a do ankyrin-G wzmacnia jej interakcję z podobnym zestawem partnerów w mózgu, w tym z receptorem inozytolu-trisfosforanowym i pompą sodowo-potasową. U myszy pozbawionych E35a te interakcje są wyraźnie słabsze. W hodowlach komórkowych wersja ankyrin-G zawierająca peptyd kodowany przez E35a wyłapuje znacznie więcej receptora uwalniającego wapń niż wersja bez niego, co wspiera tezę, że ten microekson pomaga tworzyć lub stabilizować mikroobszary regulujące wapń w neuronach.
Od molekularnego dostrajania do zachowania
Pomimo wyraźnych zmian na poziomie komórkowym, wpływ behawioralny u mutantów jest subtelny. Nie wykazują one poważnych deficytów w koordynacji, zachowaniach lękowych, pamięci w prostych testach ani w interakcjach społecznych. Jednak analiza chodu i pomiary aktywności sugerują nieco szybszy, bardziej energiczny ruch. Autorzy proponują, że szersze sieci mózgowe mogą kompensować zmienioną pobudliwość neuronów hamujących, maskując bardziej dramatyczne skutki w zastosowanych testach behawioralnych. Mimo to wyniki ilustrują, jak mały, neuronowo-specyficzny ekson może dorzucić dodatkową warstwę kontroli ponad ogólną strukturalną rolą ankyrin-G, dostrajając, jak hamowanie i dynamika wapniowa są regulowane w konkretnych obwodach.
Dlaczego to ma znaczenie dla zrozumienia mózgu
Dla osób nietechnicznych kluczowy wniosek jest taki, że różnorodność mózgu to nie tylko zestaw obecnych genów, ale także elastyczność ich edycji na nieco różne wersje w różnych komórkach. Badanie pokazuje, że wstawka dziewięciu aminokwasów w ankyrin-G działa jak precyzyjny regulator pobudliwości i sygnalizacji wapniowej specyficznych neuronów hamujących, nie zaburzając przy tym podstawowej architektury miejsca uruchamiania sygnału. Ponieważ gen Ank3 wiąże się ze schorzeniami psychicznymi, takimi jak zaburzenie dwubiegunowe, rezultaty te dają mechanistyczny wgląd w to, jak drobne zmiany w splicingu RNA mogą przesunąć równowagę obwodów i wpływać na podatność na choroby, a także podkreślają ewolucyjne wykorzystanie strategii kontroli wapnia wcześniej obserwowanej w mięśniu sercowym.
Cytowanie: Alam, S., Dermentzaki, G., Cabrera-Garcia, D. et al. A neuron type-specific microexon in Ank3/ankyrin-G modulates calcium activity and neuronal excitability. Nat Commun 17, 3173 (2026). https://doi.org/10.1038/s41467-026-69486-x
Słowa kluczowe: splicing alternatywny, ankyrin-G, interneurony GABA-ergiczne, sygnalizacja wapniowa, pobudliwość neuronów