Clear Sky Science · ru
Микроэкзон, специфичный для типа нейронов, в Ank3/анкирине-G модулирует активность кальция и возбудимость нейронов
Как крошечные генетические правки формируют поведение клеток мозга
Работа мозга опирается на тонкий баланс между нейронами, которые возбуждают цепи, и теми, которые их тормозят. В этом исследовании показано, что крошечный генетический фрагмент — всего девять аминокислот в одном белке — помогает задать, насколько активно стреляют некоторые тормозные клетки мозга и как они обрабатывают кальциевые сигналы. Поскольку тот же ген связан с биполярным расстройством и другими неврологическими состояниями, понимание этого микроскопического переключателя даёт подсказки о том, как тонкие молекулярные изменения могут распространяться вплоть до поведения и риска заболевания.
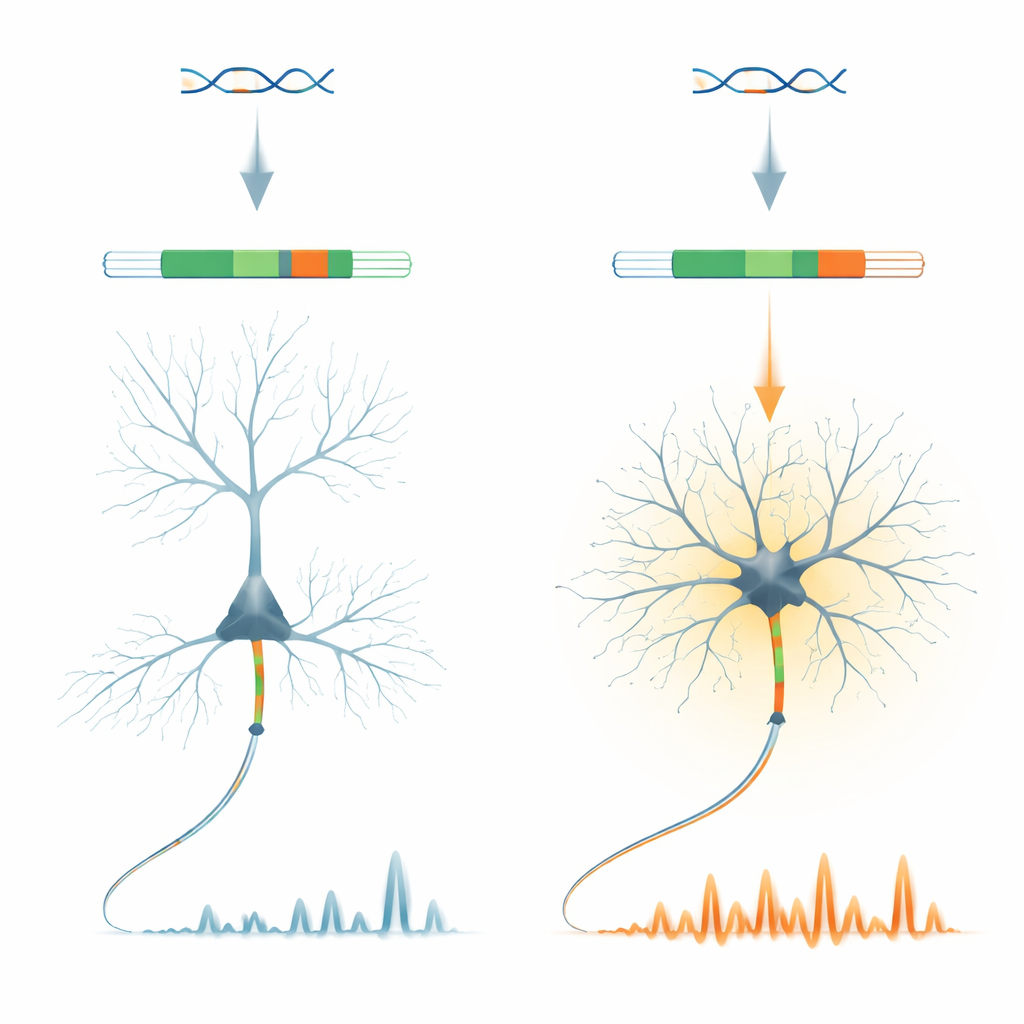
Маленький генетический переключатель с большой ролью
Исследователи сосредотачиваются на белке анкирине‑G, ключевом организаторе участка, где в аксоне генерируются нервные сигналы. В гене Ank3, кодирующем анкиринг‑G, они обнаружили очень короткий «микроэкзон», названный E35a. Этот фрагмент используется по‑разному в различных типах нейронов: он в основном исключается в возбуждающих пирамидальных нейронах коры, но часто включается во многих тормозных ГАМК‑образующих нейронах и в нейронах мозжечка. Примечательно, что этот паттерн сохранён у позвоночных, что указывает на сильную эволюционную консервацию этого тип‑специфического выключателя.
Разные клетки мозга — разные решения по сплайсингу
Клетки решают, включать ли E35a, с помощью скоординированной сети РНК‑связывающих белков, которые контролируют, как необработанная РНК разрезается и сшивается. Переанализировав большие наборы данных и протестировав упрощённый «минигенный» репортер в клетках, авторы показывают, что несколько регуляторов либо способствуют включению E35a, либо блокируют его. Некоторые из этих регуляторов более активны в возбуждающих нейронах, другие — в тормозных, и их совместное действие даёт характерный паттерн: высокое включение во многих тормозных клетках и низкое — в большинстве возбуждающих. Уровень включения также может сдвигаться в зависимости от активности нейронов, что указывает на то, что этот крошечный сегмент является частью программы, реагирующей на активность и корректирующей варианты белка по мере созревания и работы цепей.
Удаление микроэкзона меняет разряд и кальциевые сигналы
Чтобы выяснить функцию E35a, команда создала мышей, у которых этот микроэкзон полностью удалён, заставив все молекулы анкиринг‑G принимать «короткую» форму. Эти животные растут и выглядят в целом нормально, но их тормозные нейроны демонстрируют заметные изменения. В срезах мозга быстро‑стреляющие интернейроны фронтальной коры легче инициируют разряды и делают это с более высокой частотой, хотя базовая архитектура их начального сегмента аксона остаётся неизменной. У бодрствующих мышей двухфотонная визуализация показывает, что у тормозных нейронов соматическая кальциевая активность примерно вдвое выше по сравнению с контрольными животными, тогда как соседние возбуждающие нейроны демонстрируют лишь незначительные изменения. Это указывает на то, что микроэкзон тонко настраивает то, как определённые тормозные клетки интегрируют входы и контролируют внутриклеточный кальций.
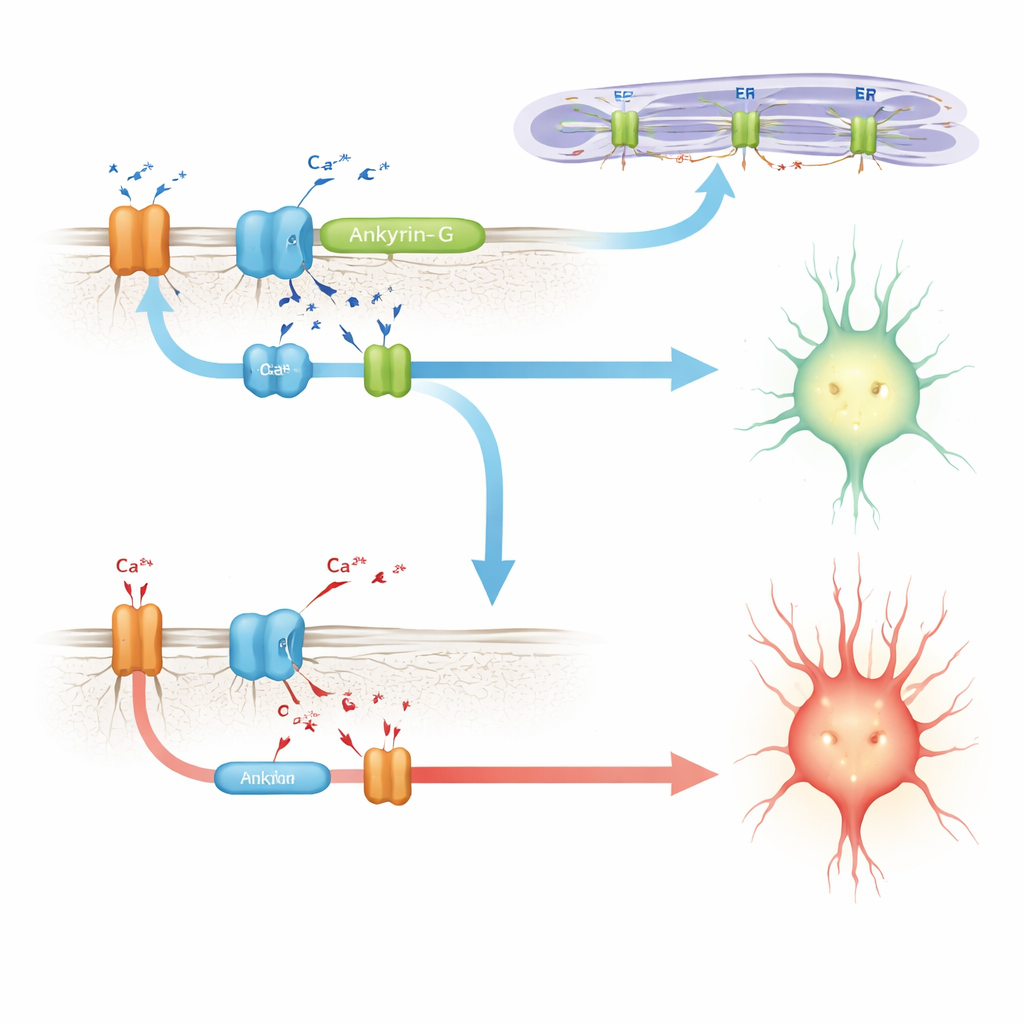
Связь анкиринг‑G с механизмами обращения с кальцием
Ища механизм, авторы обращаются к более ранним работам на сердечных клетках, где родственный белок анкиринг‑B помогает собирать кластер компонентов, управляющих кальцием: натрий‑калиевый насос, натрий‑кальциевый обменник и каналы высвобождения кальция на внутренних мембранах. Мутация в этой области нарушает комплекс и меняет сердечные кальциевые ритмы. Здесь учёные показывают, что включение E35a в анкиринг‑G усиливает его взаимодействие с похожим набором партнёров в мозге, включая рецептор инозитол‑трифосфата и натрий‑калиевый насос. У мышей без E35a эти взаимодействия заметно слабее. В культивируемых клетках версия анкиринг‑G, содержащая пептид, кодируемый E35a, связывает гораздо больше рецептора высвобождения кальция, чем версия без него, что поддерживает идею о том, что этот микроэкзон помогает создавать или стабилизировать кальцие‑регулирующие микродомены в нейронах.
От молекулярной тонкой настройки к поведению
Несмотря на явные клеточные изменения, поведенческий эффект у мутантных мышей тонкий. Они не демонстрируют серьёзных нарушений координации, тревожного поведения, памяти в простых тестах или социального взаимодействия. Тем не менее анализ походки и показатели активности указывают на слегка более быстрое и энергичное движение. Авторы предполагают, что более широкие мозговые сети могут компенсировать изменённую возбудимость тормозных нейронов, скрывая более драматические поведенческие эффекты в применённых тестах. Даже так, результаты показывают, как небольшой, тип‑специфичный экзон может добавить дополнительный уровень контроля сверх общей структурной роли анкиринг‑G, настраивая торможение и кальциевую динамику в отдельных цепях.
Почему это важно для понимания мозга
Для неспециалистов ключевая мысль в том, что разнообразие мозга определяется не только набором присутствующих генов, но и тем, насколько гибко эти гены редактируются в слегка разные варианты в разных клетках. Исследование демонстрирует, что вставка из девяти аминокислот в анкиринг‑G действует как точный регулятор возбудимости и кальциевой сигнализации специфических тормозных нейронов, не нарушая основной архитектуры их участка запуска сигналов. Поскольку ген Ank3 связан с психиатрическими состояниями, такими как биполярное расстройство, эти результаты дают механистическое представление о том, как крошечные изменения в сплайсинге РНК могут смещать баланс цепей и влиять на уязвимость к заболеваниям, а также подчёркивают эволюционное повторное использование стратегии контроля кальция, ранее обнаруженной в сердечной мышце.
Цитирование: Alam, S., Dermentzaki, G., Cabrera-Garcia, D. et al. A neuron type-specific microexon in Ank3/ankyrin-G modulates calcium activity and neuronal excitability. Nat Commun 17, 3173 (2026). https://doi.org/10.1038/s41467-026-69486-x
Ключевые слова: альтернативный сплайсинг, анкиринг-G, ГАМКергические интернейроны, кальциевая сигнализация, возбудимость нейронов