Clear Sky Science · it
Un microesone specifico per tipo neuronale in Ank3/ankyrin‑G modula l’attività del calcio e l’eccitabilità neuronale
Come piccole modifiche genetiche plasmano il comportamento delle cellule cerebrali
I cervelli dipendono da un delicato equilibrio tra neuroni che eccitano i circuiti e quelli che li inibiscono. Questo studio mostra che un frammento genetico minuscolo — appena nove mattoni amminoacidici in una singola proteina — contribuisce a determinare quanto intensamente alcuni neuroni inibitori sparano e come gestiscono i segnali di calcio. Poiché lo stesso gene è associato al disturbo bipolare e ad altre patologie cerebrali, comprendere questo interruttore microscopico offre indizi su come sottili modifiche molecolari possano riverberare fino al comportamento e al rischio di malattia.
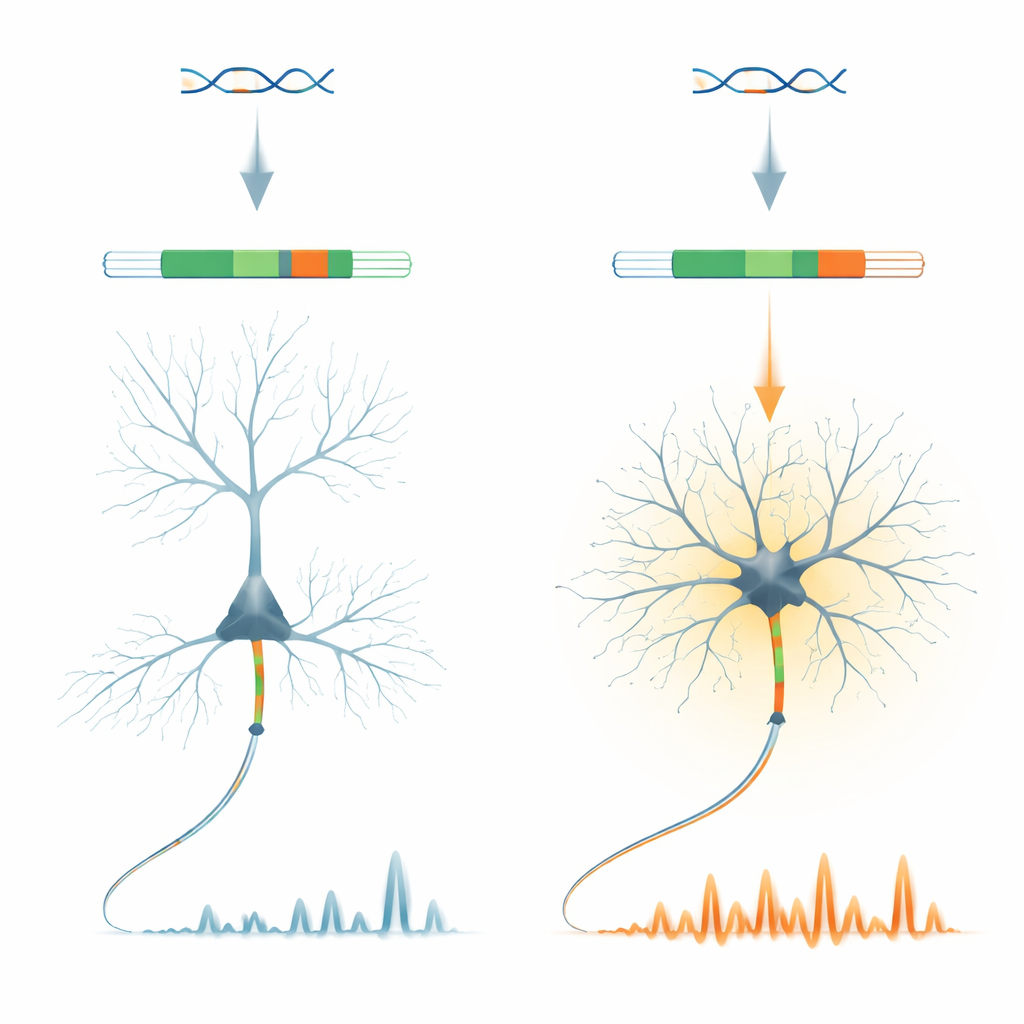
Un piccolo interruttore genetico con un grande compito
I ricercatori si concentrano su una proteina chiamata ankyrin‑G, un organizzatore chiave della regione dove i segnali neuronali vengono generati per la prima volta nell’assone. All’interno del gene Ank3 che codifica ankyrin‑G, identificano un «microesone» molto breve denominato E35a. Questo frammento viene usato in modo molto diverso a seconda del tipo neuronale: viene per lo più escluso nei neuroni piramidali eccitatori della corteccia, ma è comunemente incluso in molti neuroni inibitori produttori di GABA e nei neuroni del cervelletto. Sorprendentemente, questo schema è conservato tra i vertebrati, suggerendo che l’evoluzione ha fortemente preservato questo interruttore on/off specifico per tipo neuronale.
Cellule cerebrali diverse, scelte di splicing diverse
Le cellule decidono se includere E35a tramite una rete coordinata di proteine leganti l’RNA che controllano come l’RNA grezzo viene tagliato e ricucito. Rianalizzando grandi dataset e testando un reporter semplificato «minigene» in cellule, gli autori mostrano che diversi regolatori o promuovono o bloccano l’inclusione di E35a. Alcuni di questi regolatori sono più attivi nei neuroni eccitatori, altri negli inibitori, e la loro azione combinata produce il pattern caratteristico: alta inclusione in molti neuroni inibitori, bassa inclusione nella maggior parte dei neuroni eccitatori. Il livello di inclusione può anche variare con l’attività neuronale, indicando che questo piccolo segmento fa parte di un programma sensibile all’attività che aggiusta le varianti proteiche man mano che i circuiti maturano e si attivano.
Rimuovere il microesone modifica il firing e i segnali di calcio
Per sondare cosa faccia effettivamente E35a, il gruppo ha creato topi in cui questo microesone è completamente eliminato, costringendo tutte le molecole di ankyrin‑G nella forma «corta». Questi animali crescono e appaiono generalmente normali, ma i loro neuroni inibitori mostrano cambiamenti evidenti. In sezioni di cervello, gli interneuroni a sparo veloce nella corteccia frontale si attivano più facilmente e a frequenze maggiori, nonostante l’architettura di base del segmento iniziale dell’assone rimanga intatta. In topi svegli, immagini a due fotoni rivelano che i neuroni inibitori presentano circa il doppio dell’attività di calcio somatica rispetto ai controlli, mentre i neuroni eccitatori vicini mostrano solo cambiamenti minori. Ciò indica che il microesone regola finemente come alcuni neuroni inibitori integrano gli input e controllano i loro livelli interni di calcio.
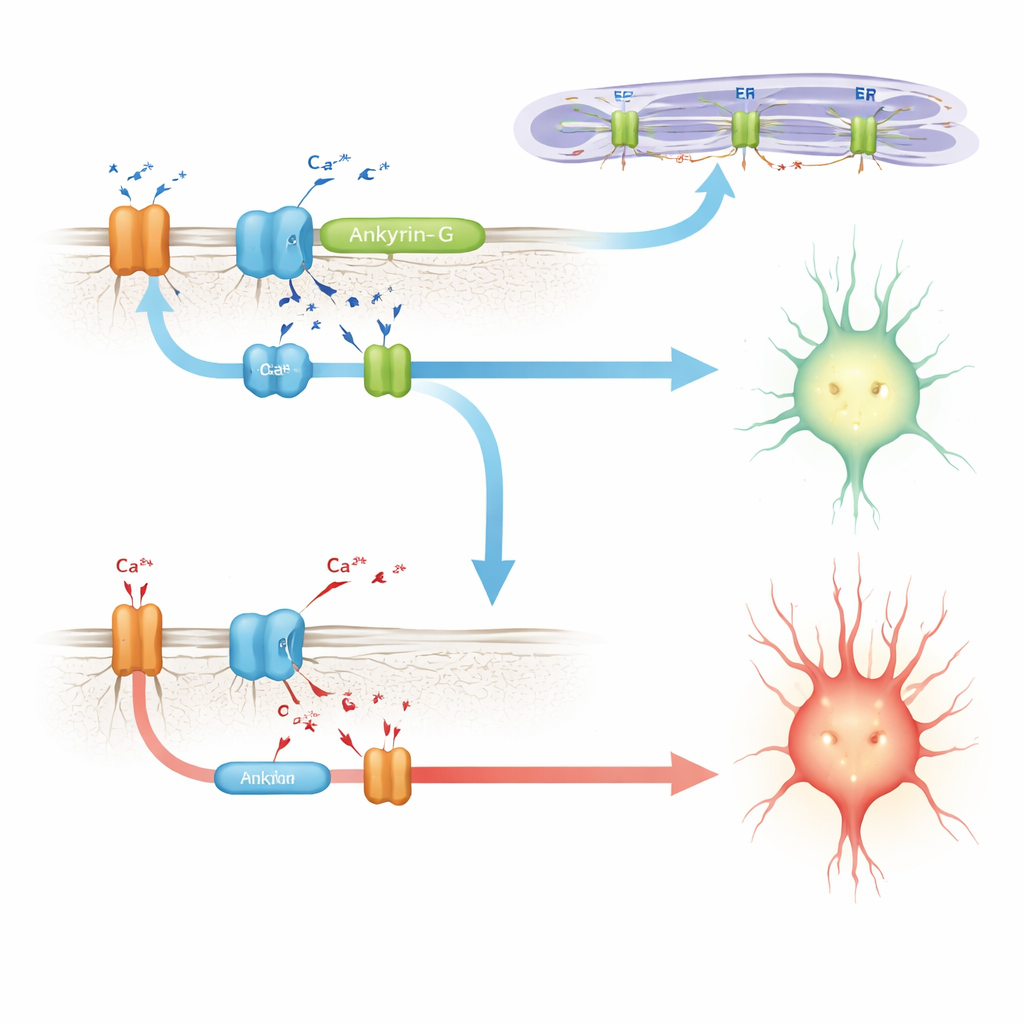
Collegare ankyrin‑G alla macchina che gestisce il calcio
Cercando un meccanismo, gli autori si rifanno a lavori precedenti nelle cellule cardiache, dove una proteina correlata, ankyrin‑B, aiuta ad assemblare un complesso di componenti che regolano il calcio: la pompa sodio‑potassio, lo scambiatore sodio‑calcio e i canali di rilascio del calcio sulle membrane interne. Una mutazione patologica in quella regione interrompe il complesso e altera i ritmi di calcio cardiaci. Qui, gli scienziati mostrano che l’inclusione di E35a in ankyrin‑G rafforza la sua interazione con un insieme simile di partner nel cervello, inclusi un recettore inositolo trifosfato e la pompa sodio‑potassio. Nei topi privi di E35a, queste interazioni risultano marcatamente più deboli. In cellule in coltura, una versione di ankyrin‑G che contiene il peptide codificato da E35a lega molto più recettore di rilascio del calcio rispetto a una versione che lo esclude, sostenendo l’idea che questo microesone aiuti a creare o stabilizzare microdomini che regolano il calcio nei neuroni.
Dalla messa a punto molecolare al comportamento
Nonostante cambiamenti chiari a livello cellulare, l’impatto comportamentale nei topi mutanti è sottile. Non mostrano deficit importanti nella coordinazione, nel comportamento ansioso, nella memoria nei test semplici o nelle interazioni sociali. Tuttavia, l’analisi del passo e le misure di attività suggeriscono un movimento lievemente più rapido e vivace. Gli autori propongono che reti cerebrali più ampie possano compensare l’aumentata eccitabilità dei neuroni inibitori, mascherando effetti comportamentali più drammatici negli assay utilizzati. Anche così, i risultati illustrano come un piccolo esone specifico per tipo neuronale possa aggiungere un ulteriore livello di controllo oltre al ruolo strutturale generale di ankyrin‑G, modulando come l’inibizione e la dinamica del calcio sono tarate in circuiti particolari.
Perché è importante per comprendere il cervello
Per il lettore non specialista, il messaggio chiave è che la diversità cerebrale non dipende solo da quali geni sono presenti, ma anche da quanto flessibilmente quei geni vengono editati in versioni leggermente differenti nelle diverse cellule. Questo studio mostra che un inserto di nove amminoacidi in ankyrin‑G agisce come una manopola di precisione per l’eccitabilità e la segnalazione del calcio di specifici neuroni inibitori, senza alterare l’architettura di base della loro regione di inizio del segnale. Poiché il gene Ank3 è collegato a condizioni psichiatriche come il disturbo bipolare, questi risultati offrono uno scorcio meccanicistico di come cambiamenti minuti nello splicing dell’RNA possano spostare l’equilibrio dei circuiti e influenzare la vulnerabilità alla malattia, evidenziando al contempo il riutilizzo evolutivo di una strategia di controllo del calcio già osservata nel muscolo cardiaco.
Citazione: Alam, S., Dermentzaki, G., Cabrera-Garcia, D. et al. A neuron type-specific microexon in Ank3/ankyrin-G modulates calcium activity and neuronal excitability. Nat Commun 17, 3173 (2026). https://doi.org/10.1038/s41467-026-69486-x
Parole chiave: splicing alternativo, ankyrin‑G, interneuroni gabaergici, segnalazione del calcio, eccitabilità neuronale