Clear Sky Science · sv
En neuronspecifik mikroexon i Ank3/ankyrin‑G påverkar kalciumaktivitet och neuronal excitabilitet
Hur små genetiska ändringar formar hjärncellers beteende
Hjärnan förlitar sig på en känslig balans mellan nervceller som exciterar kretsar och de som dämpar dem. Denna studie visar att en liten genetisk fragment—bara nio byggstenar i ett enda protein—hjälper bestämma hur kraftigt vissa inhibitoriska hjärnceller avfyrar och hur de hanterar kalciumsignaler. Eftersom samma gen är kopplad till bipolär sjukdom och andra hjärntillstånd, ger förståelsen av denna mikroskopiska strömbrytare ledtrådar till hur subtila molekylära justeringar kan få genomslag på beteende och sjukdomsrisk.
En liten genetisk strömbrytare med ett stort jobb
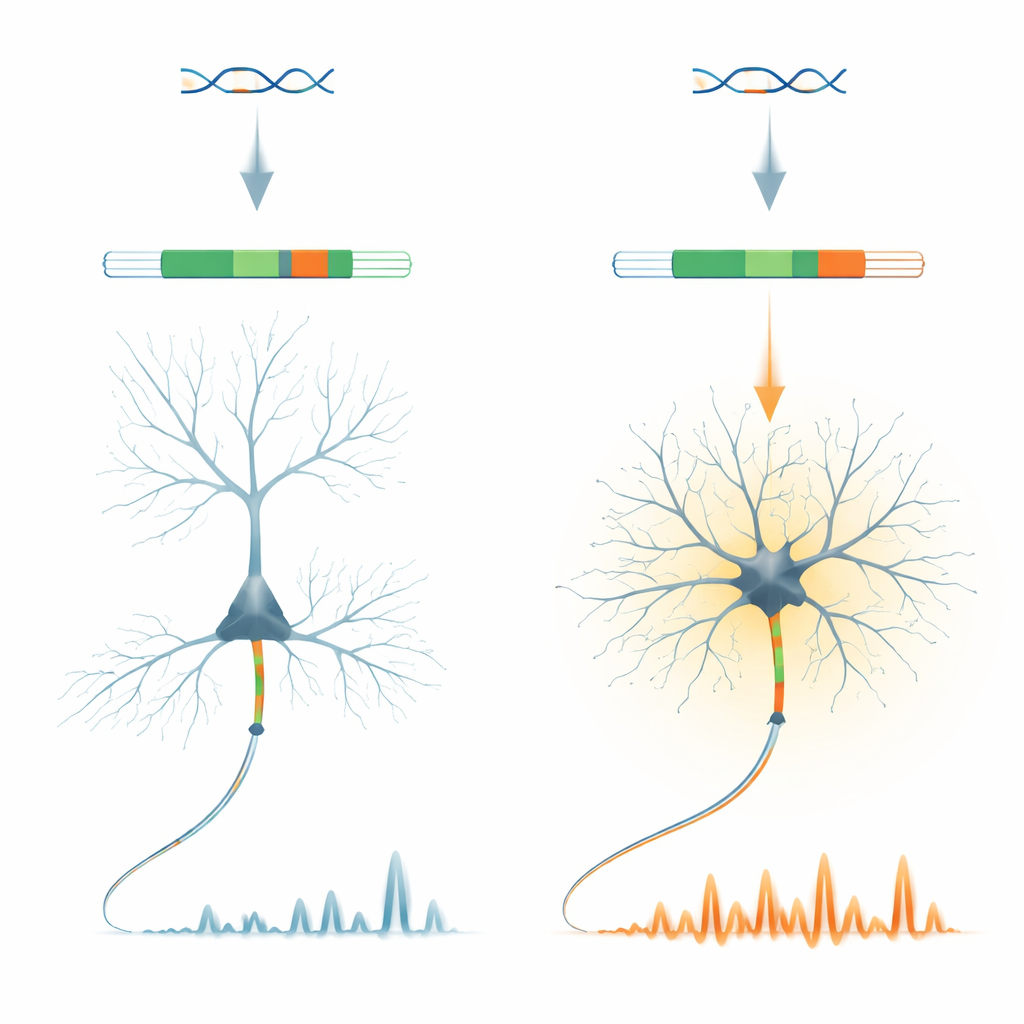
Forskarna fokuserar på ett protein kallat ankyrin‑G, en nyckelorganisatör av den region där nervsignaler först genereras i ett axon. Inom Ank3‑genen som kodar för ankyrin‑G identifierar de en mycket kort "microexon" kallad E35a. Detta snutt används mycket olika mellan neurontyper: den utesluts i huvudsak i excitatoriska pyramidceller i cortex, men inkluderas ofta i många inhibitoriska GABA‑producerande neuroner och i cerebellära neuroner. Anmärkningsvärt nog är detta mönster bevarat över ryggsträngsdjur, vilket tyder på att evolutionen starkt har bevarat denna neuronspecifika av/på‑strömbrytare.
Olika hjärnceller, olika splitsningsval
Celler bestämmer om E35a ska inkluderas genom ett koordinerat nätverk av RNA‑bindande proteiner som kontrollerar hur rå‑RNA skärs och sys ihop. Genom att omanalysera stora dataset och testa en förenklad "minigen"‑reporter i celler visar författarna att flera regulatorer antingen främjar eller blockerar inkludering av E35a. Några av dessa regulatorer är mer aktiva i excitatoriska neuroner, andra i inhibitoriska neuroner, och deras samlade verkan ger det karakteristiska mönstret: hög inklusion i många inhibitoriska celler, låg inklusion i de flesta excitatoriska celler. Inklusionsnivån kan också skifta med neuronal aktivitet, vilket indikerar att detta lilla segment är del av ett aktivitetsresponsivt program som justerar proteinvarianter när kretsar mognar och avfyrar.
Borttagning av microexonet ändrar avfyrning och kalciumsignaler
För att undersöka vad E35a faktiskt gör konstruerade gruppen möss där detta microexon är helt borttaget, vilket tvingar alla ankyrin‑G‑molekyler till den "kortare" formen. Dessa djur växer upp och verkar i stort sett normala, men deras inhibitoriska neuroner visar slående förändringar. I hjärnskivor avfyrar snabbavfyrande interneuroner i frontala cortex lättare och med högre frekvens, trots att den grundläggande arkitekturen i axonens initialsegment förblir intakt. Hos vakna möss visar tvåfotonavbildning att inhibitoriska neuroner har ungefär dubbelt så hög somatisk kalciumaktivitet jämfört med kontrollgrupper, medan närliggande excitatoriska neuroner bara visar mindre förändringar. Detta tyder på att microexonet finjusterar hur vissa inhibitoriska celler integrerar insignalering och reglerar sina interna kalciumnivåer.
Koppla ankyrin‑G till kalciumhanterande maskineri
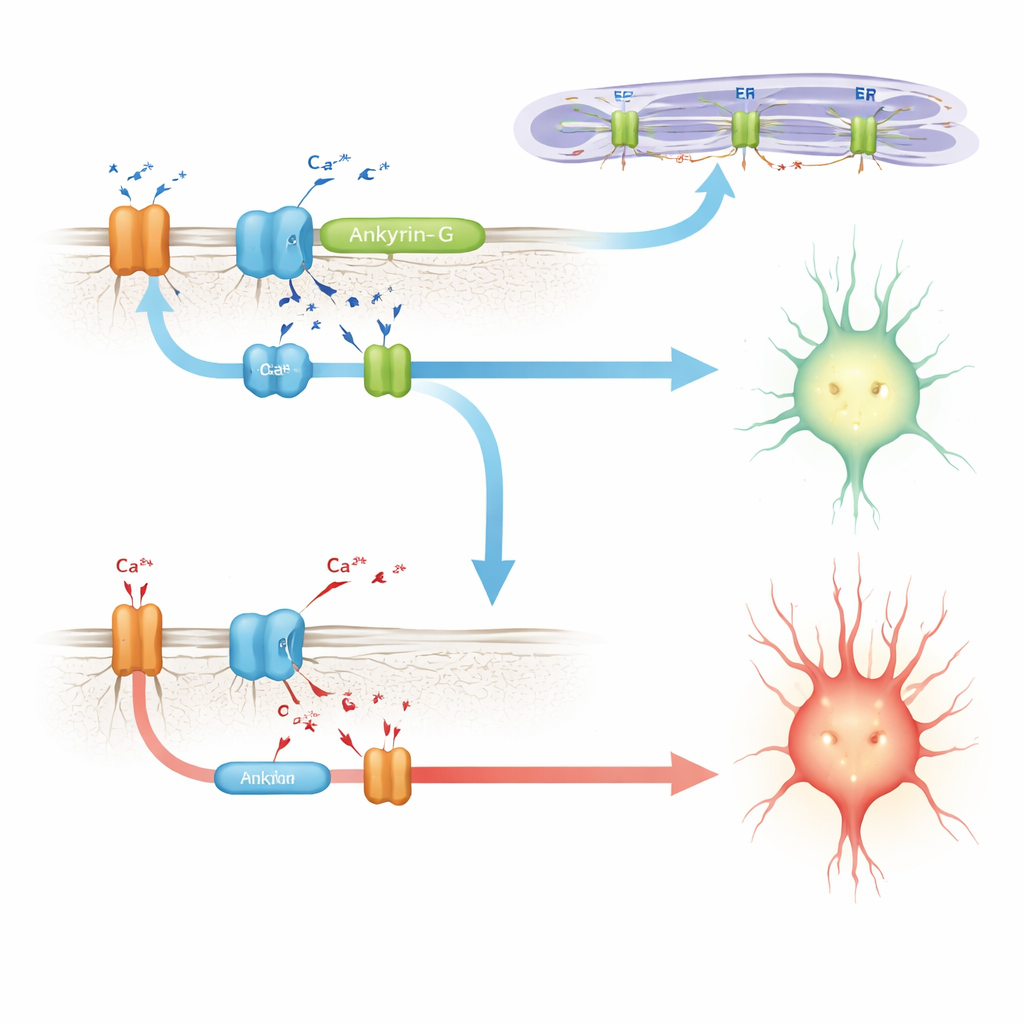
I jakten på en mekanism vänder författarna sig till tidigare arbete i hjärtceller, där ett närbesläktat protein, ankyrin‑B, hjälper till att montera ett kluster av kalciumhanterande komponenter: natrium‑kaliumpumpen, natrium‑kalcium‑växlaren och kalcium‑frisättningskanaler på interna membran. En sjukdomsvariant i det området stör komplexet och ändrar hjärtats kalciumrytmik. Här visar forskarna att inkludering av E35a i ankyrin‑G stärker dess interaktion med en liknande uppsättning partners i hjärnan, inklusive en inositoltrisfosfatreceptor och natrium‑kaliumpumpen. Hos möss utan E35a är dessa interaktioner markant svagare. I odlade celler drar en version av ankyrin‑G som innehåller det E35a‑kodade peptidet ner betydligt mer av kalcium‑frisättningsreceptorn än en version som saknar det, vilket stöder idén att detta microexon bidrar till att skapa eller stabilisera kalciumreglerande mikrodoman i neuroner.
Från molekylär finjustering till beteende
Trots tydliga förändringar på cellnivå är beteendepåverkan hos de mutanta mössen diskret. De visar inga stora brister i koordination, ångestliknande beteende, minne i enkla tester eller social interaktion. Gånganalys och aktivitetsmätningar antyder dock något snabbare, mer energiskt rörelsemönster. Författarna föreslår att bredare hjärnnätverk kan kompensera för den förändrade excitabiliteten hos inhibitoriska neuroner och därigenom dölja mer dramatiska beteendeeffekter i de använda testerna. Ändå illustrerar fynden hur en liten, neuronspecifik exon kan lägga till ett extra kontrollskikt ovanpå ankyrin‑G:s generella strukturella roll och justera hur inhibition och kalciumdynamik fininställs i specifika kretsar.
Varför detta är viktigt för förståelsen av hjärnan
För icke‑specialister är huvudbudskapet att hjärnans mångfald inte bara handlar om vilka gener som finns, utan också om hur flexibelt dessa gener redigeras till något olika varianter i olika celler. Denna studie visar att en nio‑aminosyra‑insats i ankyrin‑G fungerar som en precisionsratt för excitabilitet och kalciumsignalering i specifika inhibitoriska neuroner, utan att rubba den grundläggande arkitekturen i deras signal‑startregion. Eftersom Ank3‑genen är kopplad till psykiatriska tillstånd som bipolär sjukdom ger dessa resultat en mekanistisk inblick i hur minutiösa förändringar i RNA‑splitsning kan förskjuta kretsbalansen och påverka sårbarhet för sjukdom, samtidigt som de lyfter fram den evolutionära återanvändningen av en kalciumkontrollstrategi som tidigare observerats i hjärtmuskel.»
Citering: Alam, S., Dermentzaki, G., Cabrera-Garcia, D. et al. A neuron type-specific microexon in Ank3/ankyrin-G modulates calcium activity and neuronal excitability. Nat Commun 17, 3173 (2026). https://doi.org/10.1038/s41467-026-69486-x
Nyckelord: alternativ splitsning, ankyrin‑G, GABAerga interneuroner, kalciumsignalering, neuronal excitabilitet