Clear Sky Science · nl
Een neurontype-specifieke microexon in Ank3/ankyrin‑G moduleert calciumactiviteit en neuronale prikkelbaarheid
Hoe kleine genetische aanpassingen het gedrag van hersencellen sturen
Hersenen vertrouwen op een fijn uitgebalanceerde verhouding tussen zenuwcellen die circuits opwekken en cellen die ze tot rust brengen. Deze studie toont dat een klein genetisch fragment—slechts negen bouwstenen in een enkel eiwit—mee bepaalt hoe sterk sommige remmende hersencellen vuren en hoe ze omgaan met calciumsignalen. Omdat hetzelfde gen in verband is gebracht met bipolaire stoornis en andere hersenaandoeningen, biedt inzicht in deze microscopische schakel aanwijzingen voor hoe subtiele moleculaire aanpassingen zich kunnen uiten in gedrag en ziekterisico.
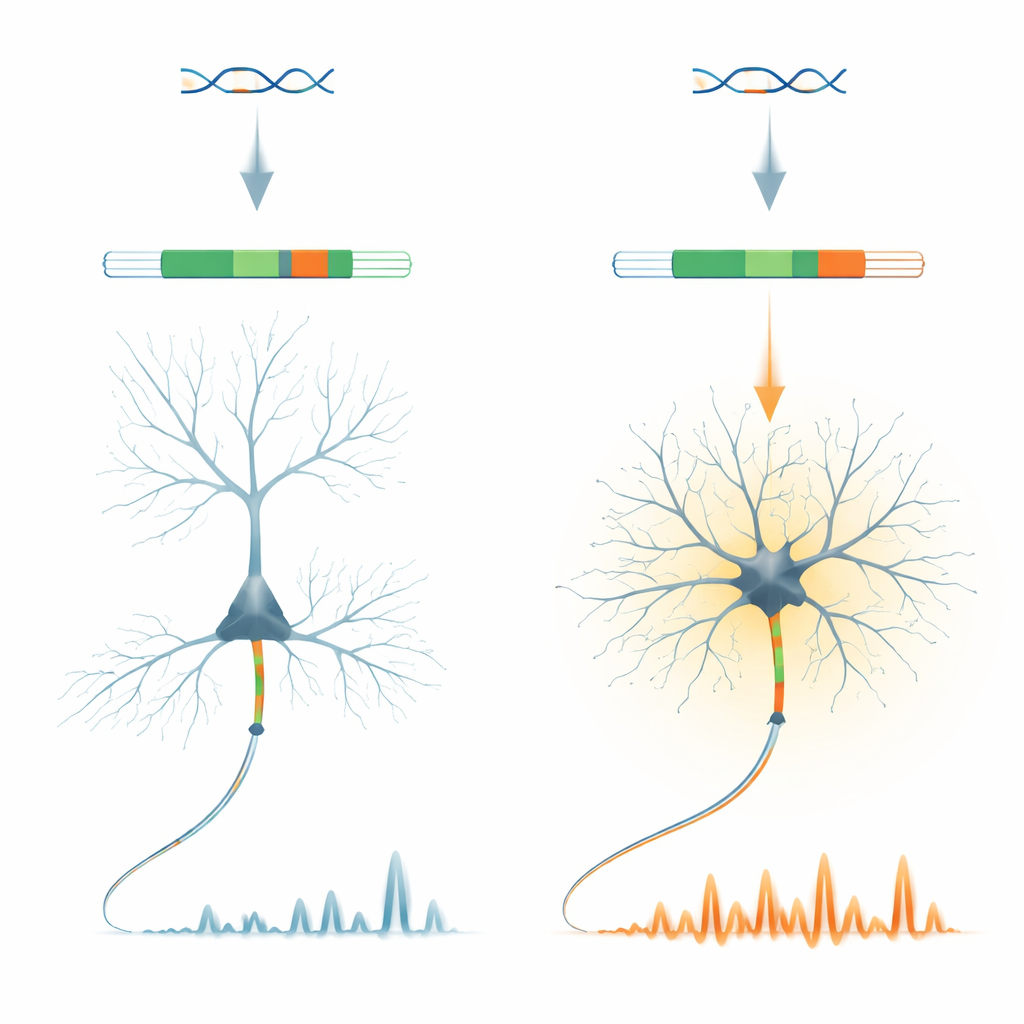
Een kleine genetische schakel met een grote taak
De onderzoekers richten zich op een eiwit genaamd ankyrin‑G, een belangrijke organisator van de regio waar zenuwsignalen voor het eerst worden gegenereerd in een axon. Binnen het Ank3‑gen dat ankyrin‑G codeert, identificeren ze een zeer korte "microexon" genaamd E35a. Dit stukje wordt heel verschillend gebruikt tussen neurontypes: het wordt meestal weggelaten in exciterende piramidale neuronen van de cortex, maar vaak opgenomen in veel remmende GABA‑producerende neuronen en in cerebellaire neuronen. Opmerkelijk is dat dit patroon behouden is bij gewervelden, wat erop wijst dat de evolutie deze neurontype‑specifieke aan/uit‑schakelaar sterk heeft geconserveerd.
Verschillende hersencellen, verschillende splicing‑keuzes
Cellen beslissen of ze E35a opnemen door een gecoördineerd netwerk van RNA‑bindende eiwitten dat bepaalt hoe het ruwe RNA wordt geknipt en gelijmd. Door grote datasets te heranalyseren en een vereenvoudigde "minigen"‑reporter in cellen te testen, tonen de auteurs aan dat meerdere regulatoren E35a‑opname stimuleren of blokkeren. Sommige van deze regulatoren zijn actiever in exciterende neuronen, andere in remmende neuronen, en hun gecombineerde werking levert het kenmerkende patroon op: hoge opname in veel remmende cellen, lage opname in de meeste exciterende cellen. Het opname‑niveau kan ook verschuiven met neuronale activiteit, wat aangeeft dat dit tiny segment deel uitmaakt van een activiteitsreactief programma dat eiwitvarianten bijstelt terwijl circuits rijpen en vuren.
Het verwijderen van de microexon verandert vuren en calciumsignalen
Om te onderzoeken wat E35a daadwerkelijk doet, maakten de onderzoekers muizen waarin deze microexon volledig is verwijderd, waardoor alle ankyrin‑G‑moleculen in de "korte" vorm gedwongen worden. Deze dieren groeien op en lijken over het algemeen normaal, maar hun remmende neuronen vertonen opvallende veranderingen. In hersenplakken vuren snelvurende interneuronen in de frontale cortex gemakkelijker en op hogere frequenties, ook al blijft de basisarchitectuur van hun axoninitiatiesegment intact. Bij ontwakende muizen laat twee‑fotonenbeeldvorming zien dat remmende neuronen ongeveer dubbel zoveel somatische calciumactiviteit hebben vergeleken met controles, terwijl nabijgelegen exciterende neuronen slechts kleine veranderingen tonen. Dit wijst erop dat de microexon fijn afstemt hoe bepaalde remmende cellen inputs integreren en hun interne calciumniveaus regelen.
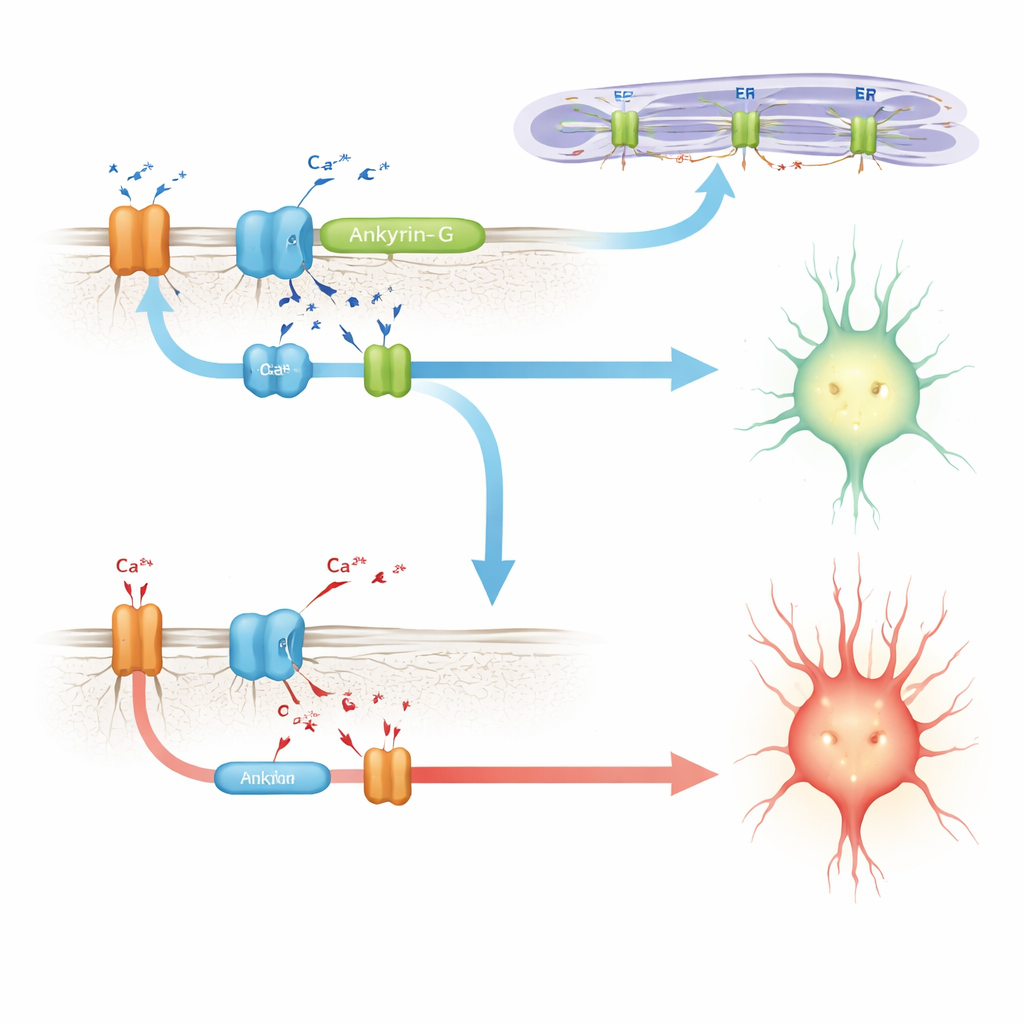
Ankyrin‑G verbinden met calciumbeheersingsmachinerie
Op zoek naar een mechanisme wenden de auteurs zich tot eerder werk in hartcellen, waar een verwant eiwit, ankyrin‑B, helpt bij het samenbrengen van een cluster calciumbeheersende componenten: de natrium‑kalium‑pomp, de natrium‑calcium‑uitwisselaar en calcium‑releasekanalen op interne membranen. Een ziekte‑mutatie in dat gebied verstoort het complex en verandert de cardiale calciumritmes. Hier laten de onderzoekers zien dat opname van E35a in ankyrin‑G de interactie met een vergelijkbare set partners in de hersenen versterkt, waaronder een inositoltrisfosfaatreceptor en de natrium‑kalium‑pomp. Bij muizen zonder E35a zijn deze interacties duidelijk verzwakt. In gekweekte cellen trekt een versie van ankyrin‑G die het door E35a gecodeerde peptiden bevat veel meer van de calcium‑releasereceptor aan dan een versie zonder, wat de idee ondersteunt dat deze microexon helpt bij het creëren of stabiliseren van calcium‑regulerende microdomeinen in neuronen.
Van moleculaire bijsturing naar gedrag
Ondanks duidelijke veranderingen op cellulair niveau is de gedragsimpact bij de gemuteerde muizen subtiel. Ze vertonen geen grote tekorten in coördinatie, angstachtig gedrag, geheugen in eenvoudige tests of sociale interactie. Wel suggereren gangbeeldanalyse en activiteitsmetingen licht snellere, energiekere bewegingen. De auteurs stellen voor dat bredere hersennetwerken mogelijk compenseren voor de gewijzigde prikkelbaarheid van remmende neuronen, waardoor meer dramatische gedragseffecten in de gebruikte tests worden verborgen. Desalniettemin illustreren de bevindingen hoe een klein, neurontype‑specifiek exon een extra regelingslaag kan toevoegen bovenop de algemene structurele rol van ankyrin‑G, waarmee wordt bijgestuurd hoe remming en calciumdynamiek in specifieke circuits getuned worden.
Waarom dit belangrijk is voor het begrijpen van de hersenen
Voor niet‑specialisten is de kernboodschap dat de diversiteit van de hersenen niet alleen draait om welke genen aanwezig zijn, maar ook om hoe flexibel die genen in verschillende cellen tot licht verschillende versies worden bewerkt. Deze studie toont aan dat een negen‑aminozuurinsertie in ankyrin‑G fungeert als een precisieknop voor de prikkelbaarheid en calcium‑signaalgeving van specifieke remmende neuronen, zonder de kernarchitectuur van hun signaal‑lancerende gebied te verstoren. Omdat het Ank3‑gen gekoppeld is aan psychiatrische aandoeningen zoals bipolaire stoornis, bieden deze resultaten een mechanistisch kijkje in hoe kleine veranderingen in RNA‑splicing de balans van circuits kunnen verschuiven en de kwetsbaarheid voor ziekte kunnen beïnvloeden, terwijl ze ook de evolutionaire hergebruik van een calcium‑controlestrategie benadrukken die eerder in hartspier werd gezien.
Bronvermelding: Alam, S., Dermentzaki, G., Cabrera-Garcia, D. et al. A neuron type-specific microexon in Ank3/ankyrin-G modulates calcium activity and neuronal excitability. Nat Commun 17, 3173 (2026). https://doi.org/10.1038/s41467-026-69486-x
Trefwoorden: alternatieve splicing, ankyrin‑G, GABAerge interneuronen, calciumsignaalgeving, neuronale prikkelbaarheid