Clear Sky Science · fr
Un microexon spécifique d’un type neuronal dans Ank3/ankyrin-G module l’activité calcique et l’excitabilité neuronale
Comment de minuscules modifications génétiques façonnent le comportement des cellules cérébrales
Le fonctionnement du cerveau repose sur un équilibre délicat entre les neurones qui excitent les circuits et ceux qui les inhibent. Cette étude montre qu’un fragment génétique minuscule — seulement neuf acides aminés dans une protéine — contribue à régler l’intensité de décharge de certains neurones inhibiteurs et la manière dont ils gèrent les signaux calciques. Comme le même gène est associé au trouble bipolaire et à d’autres affections cérébrales, comprendre cet interrupteur microscopique offre des indices sur la façon dont des ajustements moléculaires subtils peuvent se répercuter jusqu’au comportement et au risque de maladie.
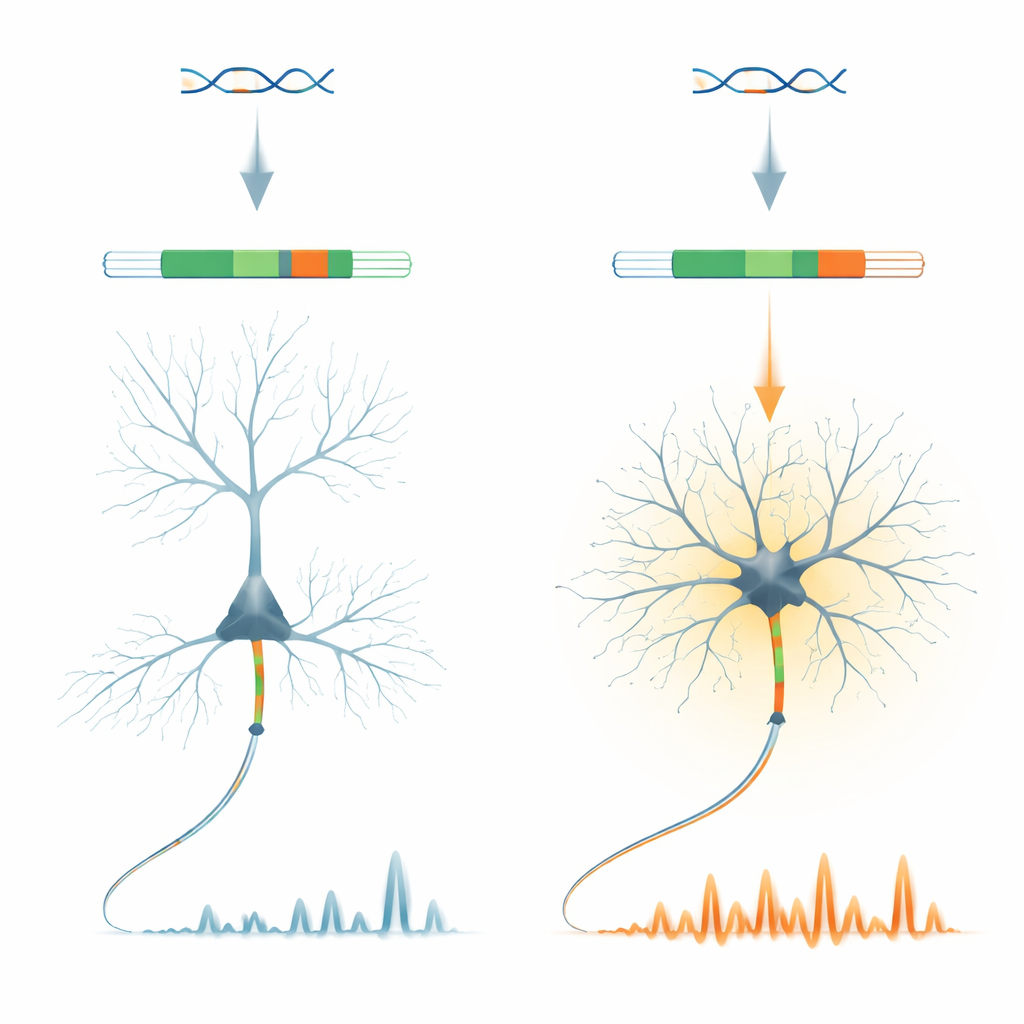
Un petit interrupteur génétique qui a un grand rôle
Les auteurs se concentrent sur une protéine appelée ankyrin‑G, un organisateur clé de la région où les signaux nerveux sont d’abord générés dans l’axone. Dans le gène Ank3 qui code pour ankyrin‑G, ils identifient un très court « microexon » nommé E35a. Cet élément est utilisé très différemment selon les types neuronaux : il est majoritairement exclu dans les neurones pyramidaux excitateurs du cortex, mais fréquemment inclus dans de nombreux neurones inhibiteurs producteurs de GABA et dans des neurones du cervelet. Remarquablement, ce schéma est conservé chez les vertébrés, ce qui suggère que l’évolution a fortement préservé cet interrupteur on/off spécifique aux types neuronaux.
Cellules cérébrales différentes, choix d’épissage différents
Les cellules décident d’inclure ou non E35a via un réseau coordonné de protéines liant l’ARN qui contrôlent le découpage et le montage de l’ARN pré‑messager. En réanalysant de larges jeux de données et en testant un rapporteur « minigène » simplifié en culture cellulaire, les auteurs montrent que plusieurs régulateurs favorisent ou bloquent l’inclusion d’E35a. Certains de ces régulateurs sont plus actifs dans les neurones excitateurs, d’autres dans les neurones inhibiteurs, et leur action combinée produit le profil caractéristique : forte inclusion dans de nombreux neurones inhibiteurs, faible inclusion dans la plupart des neurones excitateurs. Le niveau d’inclusion peut aussi varier avec l’activité neuronale, indiquant que ce segment minuscule fait partie d’un programme réactif à l’activité qui ajuste les variantes protéiques à mesure que les circuits mûrissent et s’activent.
La suppression du microexon modifie la décharge et les signaux calciques
Pour déterminer la fonction d’E35a, l’équipe a généré des souris chez lesquelles ce microexon est totalement supprimé, forçant toutes les molécules d’ankyrin‑G à adopter la forme « courte ». Ces animaux se développent et paraissent généralement normaux, mais leurs neurones inhibiteurs présentent des modifications nettes. Dans des coupes cérébrales, des interneurones à décharge rapide du cortex frontal tirent plus facilement et à des fréquences supérieures, bien que l’architecture de base de leur segment initial d’axone reste intacte. Chez des souris éveillées, l’imagerie two‑photon révèle que les neurones inhibiteurs ont environ le double d’activité calcique somatique par rapport aux contrôles, tandis que les neurones excitateurs voisins montrent seulement des changements mineurs. Cela indique que le microexon affine la manière dont certains neurones inhibiteurs intègrent les entrées et contrôlent leurs niveaux calciques internes.
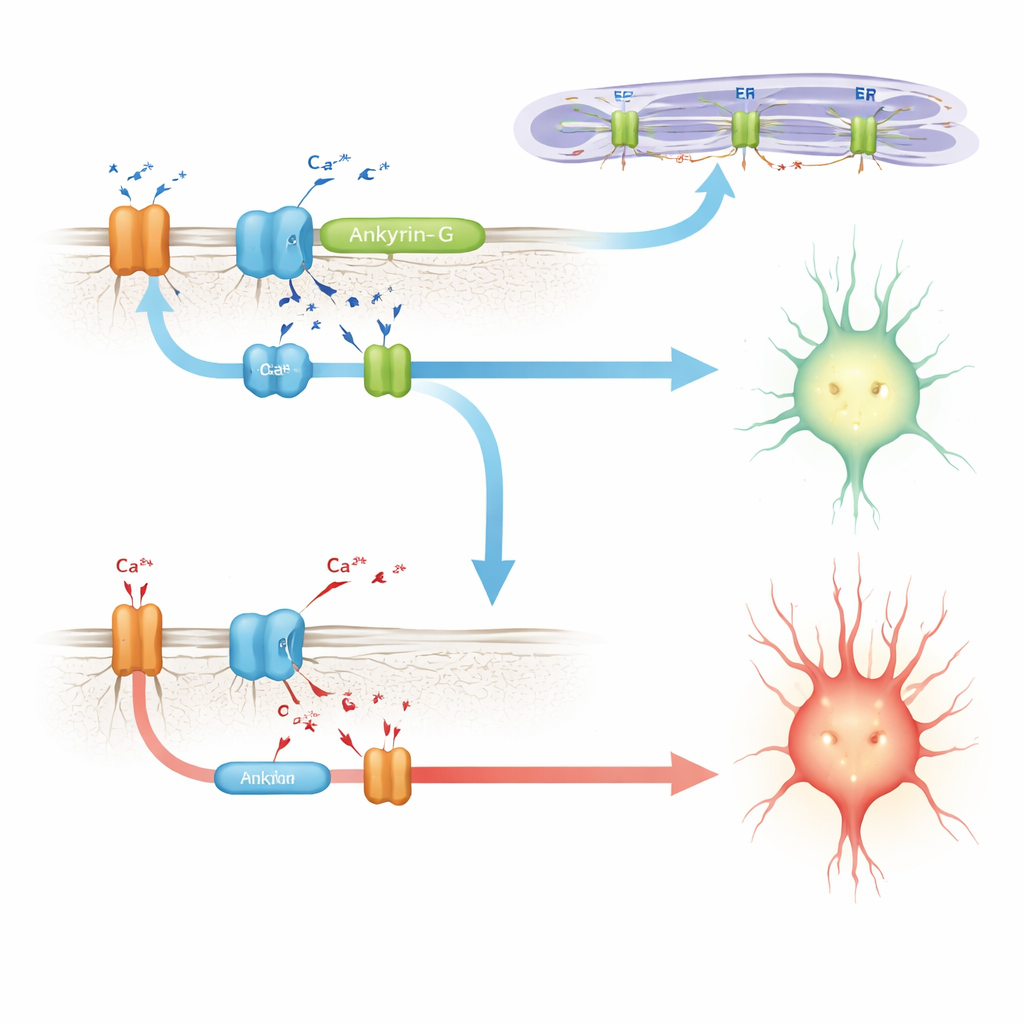
Relier ankyrin‑G à la machinerie de gestion du calcium
À la recherche d’un mécanisme, les auteurs se tournent vers des travaux antérieurs sur les cellules cardiaques, où une protéine apparentée, ankyrin‑B, aide à assembler un ensemble de composants gérant le calcium : la pompe sodium‑potassium, l’échangeur sodium‑calcium et les canaux de libération du calcium sur les membranes internes. Une mutation pathologique dans cette région perturbe le complexe et altère les rythmes calciques cardiaques. Ici, les scientifiques montrent que l’inclusion d’E35a dans ankyrin‑G renforce son interaction avec un ensemble similaire de partenaires dans le cerveau, incluant un récepteur à l’inositol trisphosphate et la pompe sodium‑potassium. Chez les souris dépourvues d’E35a, ces interactions sont nettement plus faibles. En culture cellulaire, une version d’ankyrin‑G contenant le peptide codé par E35a attire beaucoup plus le récepteur de libération du calcium qu’une version qui en est dépourvue, soutenant l’idée que ce microexon contribue à créer ou stabiliser des microdomaines régulateurs du calcium dans les neurones.
Du réglage moléculaire au comportement
Malgré des changements clairs au niveau cellulaire, l’impact comportemental chez les souris mutantes est subtil. Elles ne présentent pas de déficits majeurs de coordination, d’anxiété, de mémoire dans des tests simples, ni d’interaction sociale évidente. Cependant, l’analyse de la démarche et des mesures d’activité suggèrent des mouvements légèrement plus rapides et plus énergiques. Les auteurs proposent que des réseaux cérébraux plus larges puissent compenser l’excitabilité altérée des neurones inhibiteurs, masquant des effets comportementaux plus marqués dans les tests utilisés. Quoi qu’il en soit, les résultats illustrent comment un petit exon spécifique à un type neuronal peut ajouter une couche de contrôle sur le rôle structural général d’ankyrin‑G, ajustant la façon dont l’inhibition et la dynamique calcique sont modulées dans des circuits particuliers.
Pourquoi cela compte pour la compréhension du cerveau
Pour le grand public, le message clé est que la diversité du cerveau ne dépend pas seulement des gènes présents, mais aussi de la manière dont ces gènes sont édités en versions légèrement différentes selon les cellules. Cette étude montre qu’un insert de neuf acides aminés dans ankyrin‑G agit comme un « réglage de précision » de l’excitabilité et de la signalisation calcique de neurones inhibiteurs spécifiques, sans perturber l’architecture de base de leur région de lancement du signal. Comme le gène Ank3 est lié à des troubles psychiatriques tels que le trouble bipolaire, ces résultats offrent un aperçu mécanistique de la façon dont de minuscules changements dans l’épissage de l’ARN pourraient déplacer l’équilibre des circuits et influencer la vulnérabilité à la maladie, tout en soulignant la réutilisation évolutive d’une stratégie de contrôle du calcium déjà observée dans le muscle cardiaque.
Citation: Alam, S., Dermentzaki, G., Cabrera-Garcia, D. et al. A neuron type-specific microexon in Ank3/ankyrin-G modulates calcium activity and neuronal excitability. Nat Commun 17, 3173 (2026). https://doi.org/10.1038/s41467-026-69486-x
Mots-clés: épissage alternatif, ankyrin‑G, interneurones GABAergiques, signalisation calcique, excitabilité neuronale