Clear Sky Science · de
Ein neuronentyp-spezifischer Microexon in Ank3/ankyrin-G moduliert Calciumaktivität und neuronale Erregbarkeit
Wie winzige genetische Änderungen das Verhalten von Gehirnzellen formen
Gehirne beruhen auf einem empfindlichen Gleichgewicht zwischen Nervenzellen, die Netzwerke erregen, und solchen, die sie dämpfen. Diese Studie zeigt, dass ein winziges genetisches Fragment – nur neun Bausteine in einem einzelnen Protein – mitbestimmt, wie stark einige hemmende Nervenzellen feuern und wie sie mit Calciumsignalen umgehen. Da dasselbe Gen mit bipolarer Störung und anderen Hirnerkrankungen in Verbindung gebracht wird, liefert das Verständnis dieses mikroskopischen Schalters Hinweise darauf, wie subtile molekulare Anpassungen bis hin zu Verhalten und Krankheitsrisiko durchschlagen können.
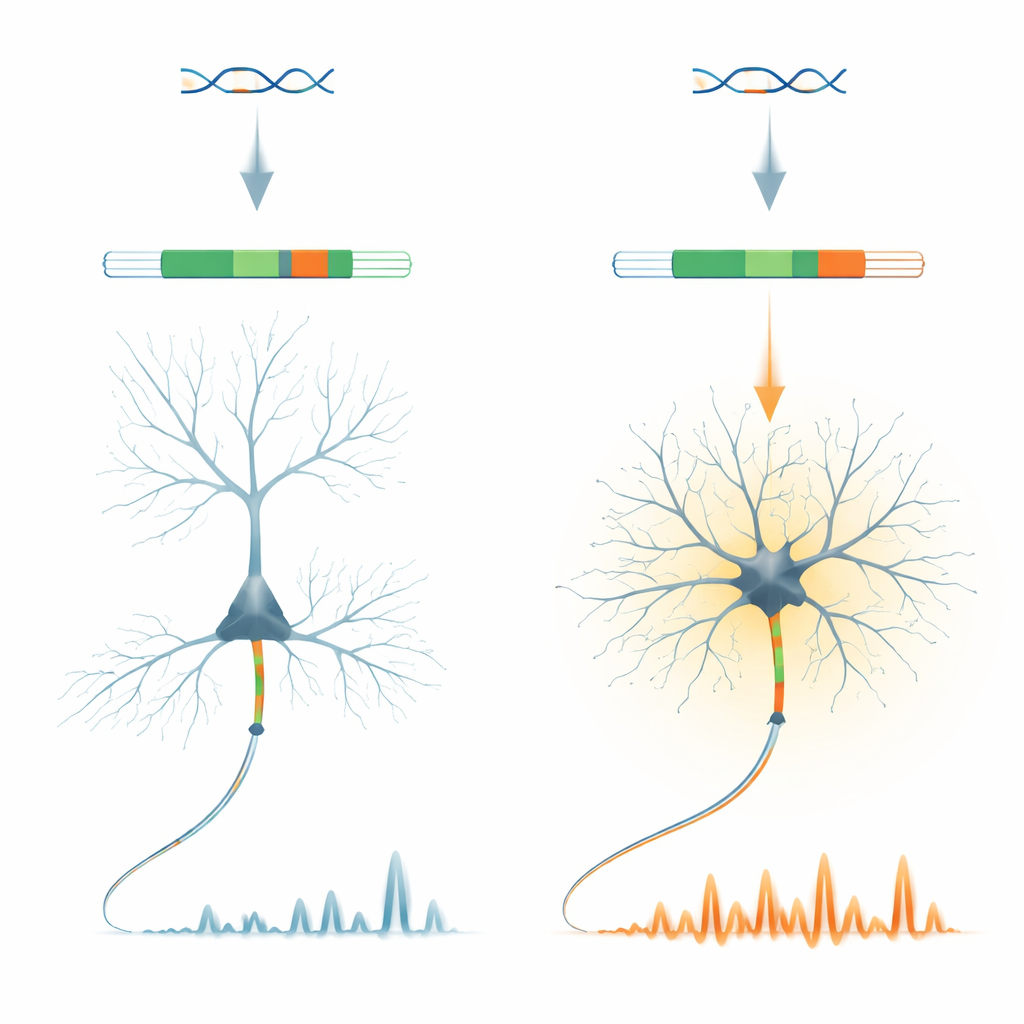
Ein kleiner genetischer Schalter mit großer Aufgabe
Die Forschenden konzentrieren sich auf ein Protein namens ankyrin-G, einen wichtigen Organisator der Region, in der Nervensignale im Axon zuerst entstehen. Innerhalb des Ank3-Gens, das ankyrin-G kodiert, identifizieren sie ein sehr kurzes „Microexon“ namens E35a. Dieses Snippet wird zwischen Neuronentypen sehr unterschiedlich verwendet: Es wird in den exzitatorischen Pyramidenneuronen des Kortex meist ausgelassen, ist aber in vielen inhibitorischen, GABA-produzierenden Neuronen und in Kleinhirnzellen häufig enthalten. Bemerkenswerterweise ist dieses Muster bei Wirbeltieren konserviert, was darauf hindeutet, dass die Evolution diesen neuronentyp-spezifischen Ein/Aus-Schalter stark bewahrt hat.
Verschiedene Gehirnzellen, verschiedene Spleißentscheidungen
Zellen entscheiden, ob sie E35a einbauen, durch ein koordiniertes Netzwerk von RNA-bindenden Proteinen, die bestimmen, wie Roh-RNA geschnitten und zusammengefügt wird. Durch die Reanalyse großer Datensätze und Tests mit einem vereinfachten „Minigen“-Reporter in Zellen zeigen die Autorinnen und Autoren, dass mehrere Regulatoren entweder die Einfügung von E35a fördern oder blockieren. Einige dieser Regulatoren sind in exzitatorischen Neuronen stärker aktiv, andere in inhibitorischen, und ihr zusammenspiel erzeugt das charakteristische Muster: hohe Einfügung in vielen inhibitorischen Zellen, geringe Einfügung in den meisten exzitatorischen Zellen. Der Einfügungsgrad kann sich auch mit neuronaler Aktivität verschieben, was darauf hinweist, dass dieses winzige Segment Teil eines aktivitätsabhängigen Programms ist, das Proteinvarianten anpasst, während Schaltkreise reifen und feuern.
Das Entfernen des Microexons verändert Feuern und Calciumsignale
Um zu untersuchen, was E35a tatsächlich bewirkt, erzeugte das Team Mäuse, bei denen dieses Microexon vollständig entfernt wurde, sodass alle ankyrin-G-Moleküle in der „kurzen“ Form vorliegen. Diese Tiere wachsen heran und erscheinen im Allgemeinen normal, doch ihre inhibitorischen Neurone zeigen auffällige Veränderungen. In Gehirnschnitten feuern schnell schaltende Interneurone im Frontalkortex leichter und mit höheren Raten, obwohl die grundlegende Architektur ihres Axoninitialsegments intakt bleibt. Bei wachen Mäusen zeigt die Zwei-Photonen-Bildgebung, dass inhibitorische Neurone ungefähr die doppelte somatische Calciumaktivität im Vergleich zu Kontrollen aufweisen, während benachbarte exzitatorische Neurone nur geringfügige Veränderungen zeigen. Das deutet darauf hin, dass das Microexon feinjustiert, wie bestimmte inhibitorische Zellen Eingänge integrieren und ihre intrazellulären Calciumspiegel kontrollieren.
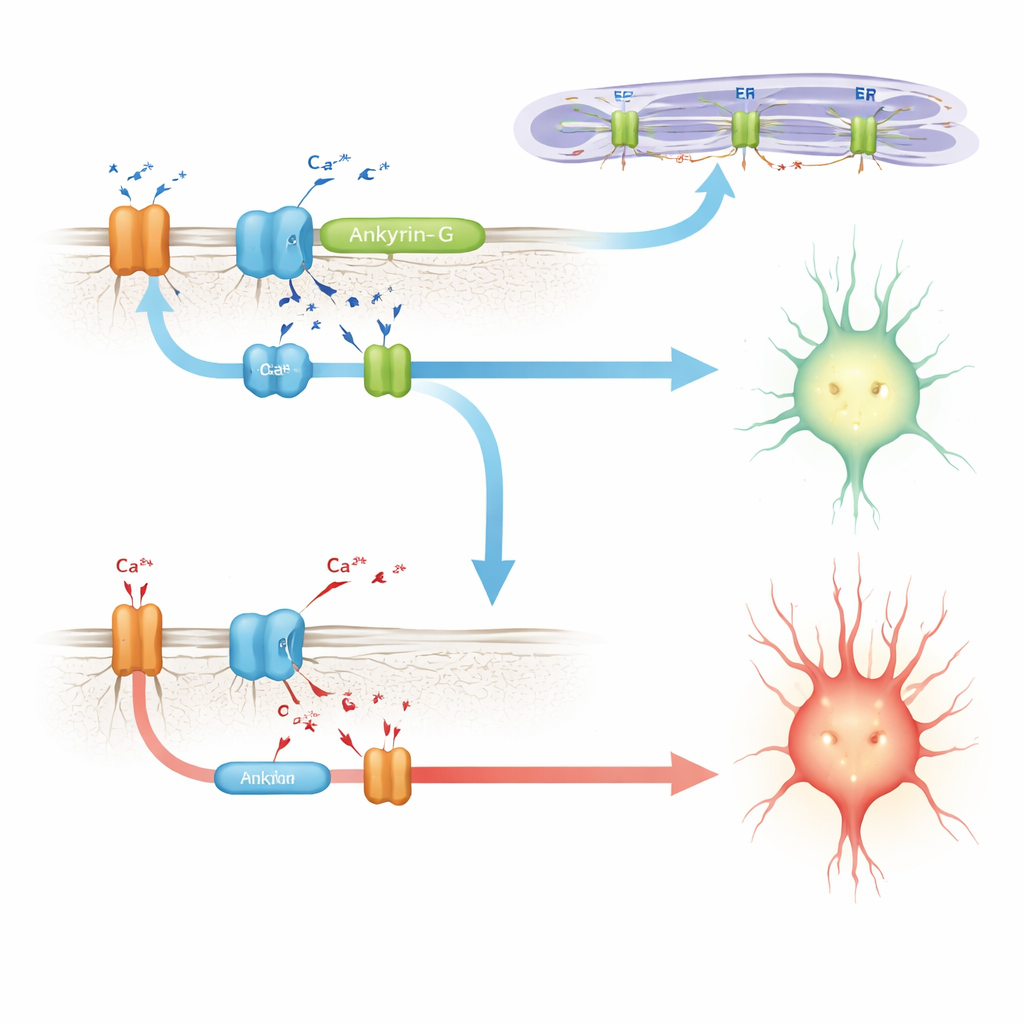
Verknüpfung von ankyrin-G mit der Calcium-Handling-Maschinerie
Auf der Suche nach einem Mechanismus verweisen die Autorinnen und Autoren auf frühere Arbeiten in Herzmuskelzellen, wo ein verwandtes Protein, ankyrin-B, dabei hilft, einen Komplex von Calcium-handhabenden Komponenten zusammenzubauen: die Natrium–Kalium-Pumpe, den Natrium–Calcium-Austauscher und Calcium-freisetzende Kanäle auf inneren Membranen. Eine Krankheitsmutation in dieser Region zerstört den Komplex und verändert die kardialen Calciumrhythmen. Hier zeigen die Forschenden, dass die Einfügung von E35a in ankyrin-G dessen Wechselwirkung mit einem ähnlichen Satz von Partnern im Gehirn verstärkt, darunter ein Inositoltrisphosphat-Rezeptor und die Natrium–Kalium-Pumpe. In Mäusen ohne E35a sind diese Interaktionen merklich schwächer. In kultivierten Zellen zieht eine Version von ankyrin-G, die das durch E35a kodierte Peptid enthält, deutlich mehr des Calciumfreisetzungs-Rezeptors an als eine Version ohne dieses Segment, was die Idee stützt, dass dieses Microexon beim Aufbau oder bei der Stabilisierung calciumregulierender Mikrodomainen in Neuronen hilft.
Von molekularer Feinabstimmung zu Verhalten
Trotz klarer Veränderungen auf zellulärer Ebene ist die Verhaltenswirkung bei den Mutantenmäusen subtil. Sie zeigen keine großen Defizite in Koordination, angstähnlichem Verhalten, Gedächtnis in einfachen Tests oder sozialer Interaktion. Ganganalysen und Aktivitätsmessungen deuten jedoch auf leicht schnellere, energiegeladenere Bewegung hin. Die Autorinnen und Autoren vermuten, dass breitere Gehirnnetzwerke die veränderte Erregbarkeit der inhibitorischen Neurone kompensieren und so dramatischere Verhaltensfolgen in den verwendeten Tests verdecken. Dennoch veranschaulichen die Befunde, wie ein kleines, neuronentyp-spezifisches Exon eine zusätzliche Kontrollebenen über die allgemeine strukturelle Rolle von ankyrin-G legen kann und die Abstimmung von Hemmung und Calciumausprägung in bestimmten Schaltkreisen beeinflusst.
Warum das für das Verständnis des Gehirns wichtig ist
Für Nicht-Spezialisten ist die Kernbotschaft, dass die Vielfalt des Gehirns nicht nur davon abhängt, welche Gene vorhanden sind, sondern auch davon, wie flexibel diese Gene in leicht unterschiedliche Versionen in verschiedenen Zellen bearbeitet werden. Diese Studie zeigt, dass ein neun Aminosäuren langer Einschub in ankyrin-G als Präzisionsregler für Erregbarkeit und Calciumsignalisierung bestimmter inhibitorischer Neurone wirkt, ohne die Kernarchitektur ihrer Signalausgangsregion zu stören. Da das Ank3-Gen mit psychiatrischen Erkrankungen wie bipolarer Störung verknüpft ist, bieten diese Ergebnisse einen mechanistischen Einblick, wie winzige Veränderungen im RNA-Spleißen das Gleichgewicht von Schaltkreisen verschieben und die Anfälligkeit für Krankheiten beeinflussen könnten, und betonen zugleich die evolutionäre Wiederverwendung einer zuvor im Herzmuskel beobachteten Calcium-Kontrollstrategie.
Zitation: Alam, S., Dermentzaki, G., Cabrera-Garcia, D. et al. A neuron type-specific microexon in Ank3/ankyrin-G modulates calcium activity and neuronal excitability. Nat Commun 17, 3173 (2026). https://doi.org/10.1038/s41467-026-69486-x
Schlüsselwörter: alternatives Spleißen, ankyrin-G, GABAerge Interneurone, Calcium-Signalgebung, neuronale Erregbarkeit