Clear Sky Science · zh
CycloPepper:用于预测环化结果并优化治疗用环肽合成的机器学习平台
把柔软的链条变成强大的环
癌症药物、抗生素和其他现代药物越来越多地由称为肽的短氨基酸链构成。当这些链被缝合成封闭的环状结构——环肽时,它们通常会变得更坚固、在体内存留时间更长,并且更容易穿透细胞。但在实验室里制造这些微小的环非常讲究,化学家可能会花数周时间猜测哪种方式能将链闭合。本文介绍了 CycloPepper,一种由机器学习驱动的平台,帮助研究者在几秒钟内预测哪些肽链可能形成稳定的环、哪些会失败,从而可能加速新肽类药物的发现。
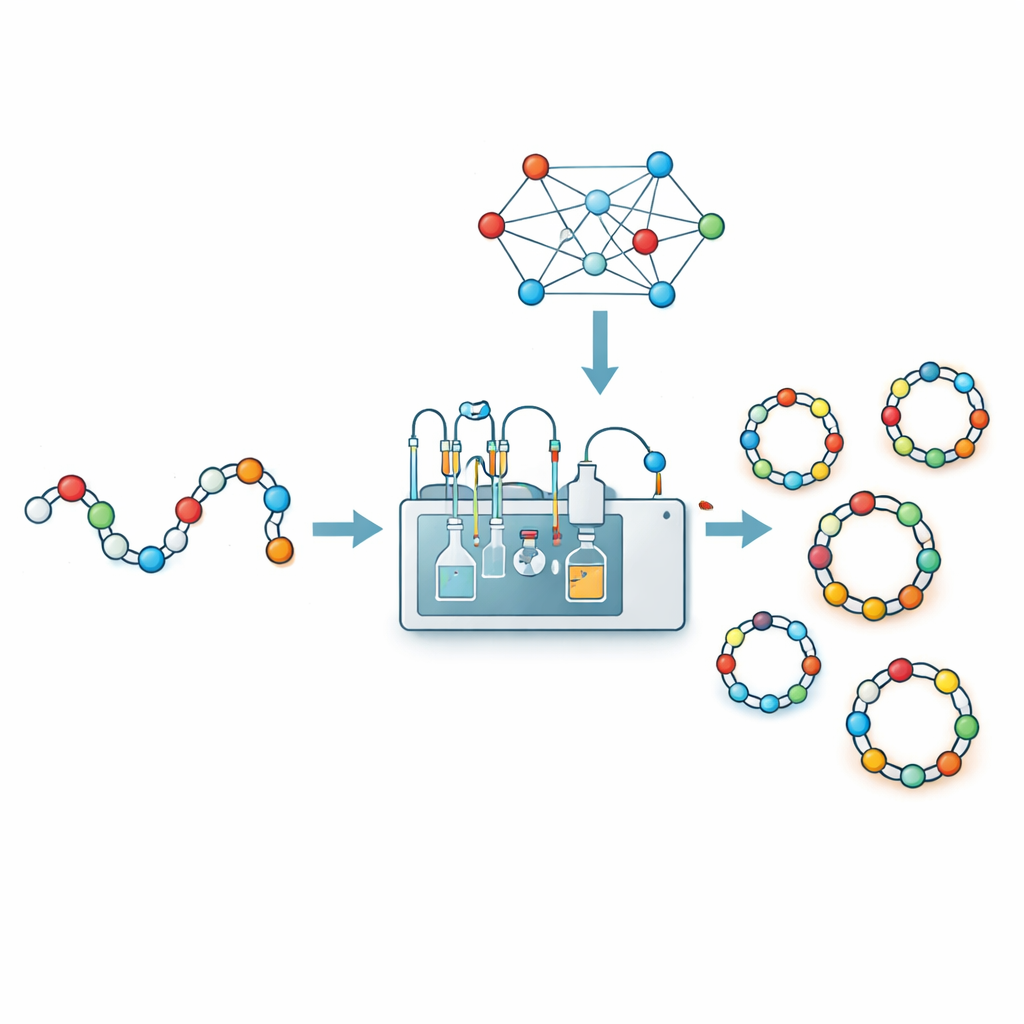
为什么环状肽很重要
肽是由氨基酸串联而成的分子,与构成蛋白质的基本单元相同。作为开放链时,它们可能松弛且容易被体内的酶降解。如果将链的两端头对尾连接形成环,分子会变得更紧凑、更刚性。这通常会提高其与生物靶标的结合强度、增加对消化酶的耐受性并改善穿透细胞膜的能力。若干重要药物,包括强效抗生素,基于此类环状结构。对于药物设计者而言,将线性肽转化为环是将弱而易碎的分子变成有效且持久药物的一项关键策略。
闭环的隐性难点
尽管环肽很有吸引力,但它们难以合成。要形成环,柔性的链必须折叠成恰当的形状,使两端能够相互反应而不是与邻近分子发生反应。尤其是短链,采用这种环状构象需要付出很高的“组织成本”,而连接位点附近拥挤的氨基酸则可能在物理上阻碍反应。化学家通常在微小的固体小珠上构建肽,这虽然简化了纯化过程,但会进一步限制链的折叠自由。因此,环化是否成功往往对化学家在一条大体相似序列上选择闭合位置极为敏感。直到现在,这一选择在很大程度上依赖经验和反复试错。
机器人与算法构建学习库
为用数据取代猜测,研究人员将自动化化学与机器学习相结合。利用名为 CycloBot 的机器人流合成系统和一种允许在固相上直接完成闭环的特制连接子,他们快速合成并测试了 306 条不同的肽链,长度从 2 到 14 个氨基酸不等。对于每一个序列,他们仅记录是否检测到纯净的环状产物。随后,他们将每个序列转化为丰富的数值描述:包含哪些氨基酸、两两氨基酸的顺序、逐位的位置编码,以及基于实验室经验挑选的一些标志(例如某些氨基酸出现在任一末端会促进或阻碍环化)。将这些 414 维的指纹输入多种机器学习模型,他们发现支持向量分类器的表现最佳,在交叉验证测试中大约能 84% 正确预测环化成功或失败。
将预测投入实验验证
团队随后用模型从未见过的新肽对其进行了挑战。他们设计了 8 条人工序列和 4 条受天然启发的候选治疗肽,并对每条序列尝试沿链上所有可能的闭合位置。总共进行了 74 次环化实验。机器学习模型的预测与实验结果在 64 个案例中一致,准确率为 86%。重要的是,该模型既能标出有希望的位点,也能识别出不利位点,这意味着它既能帮助化学家避免在不配合的序列上浪费精力,也能突出最可能成功的候选位点。
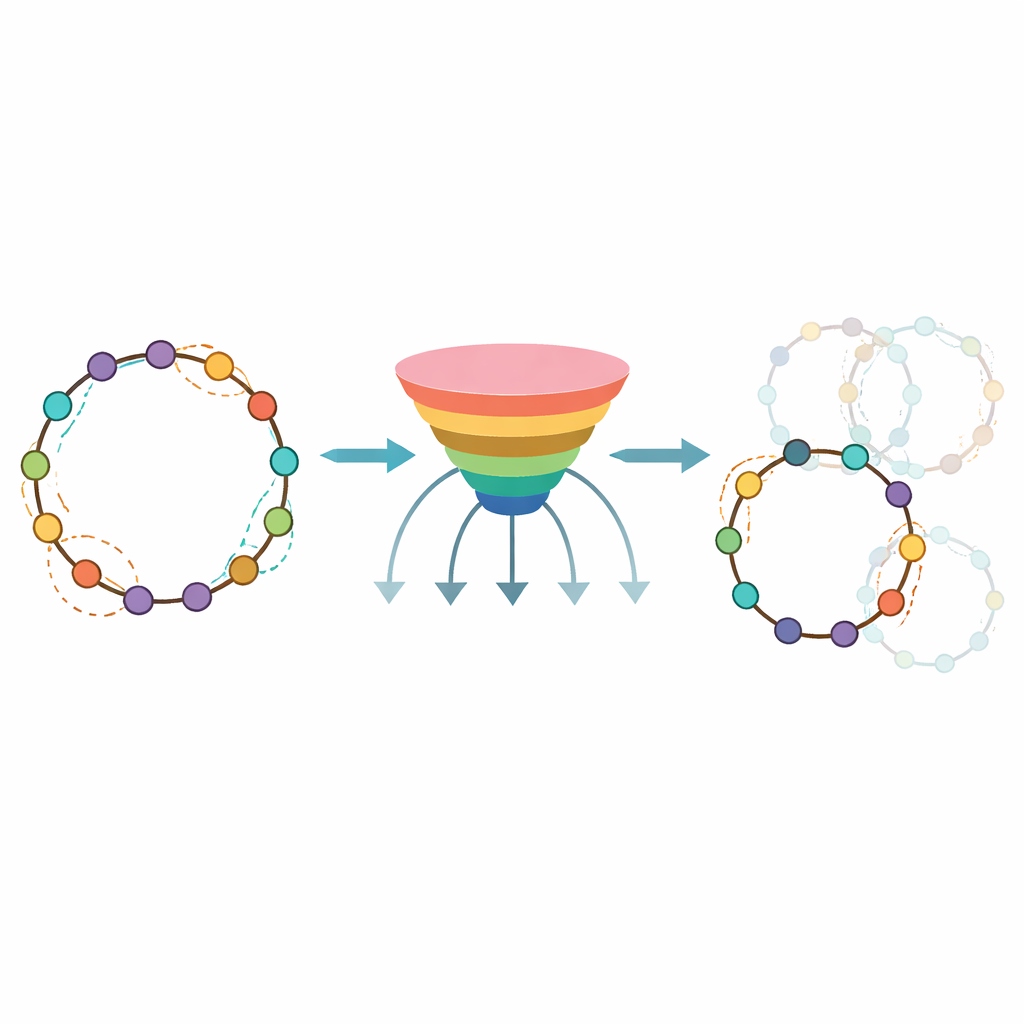
为药物设计者准备的实用工具
为使此方法在实验室之外也有用,作者将训练好的模型封装成名为 CycloPepper 的公共平台,提供可下载软件和网页工具。用户可以输入单个肽或一次上传多个肽,并在几秒内收到一个显示可能有效的头对尾闭合位点的图。团队通过为参与癌症和免疫疾病相关蛋白靶标设计数百个潜在环肽证明了该工具的价值,显示该工具能迅速筛掉近 40% 不太可能环化的序列。对非专业人士来说,结论是 CycloPepper 像一个智能的预筛选助理,将庞大的设计空间缩减为可操作的候选集合。通过将自动化合成与预测算法相结合,这项工作让更快、更有理性的环状肽药物发现更接近现实。
引用: Pan, Y., Hu, C., Li, J. et al. CycloPepper: a machine learning platform for predicting cyclization outcomes and optimizing synthesis of therapeutic cyclopeptides. Nat Commun 17, 2803 (2026). https://doi.org/10.1038/s41467-026-69441-w
关键词: 环状肽, 肽类药物设计, 化学中的机器学习, 自动化合成, 环化预测