Clear Sky Science · pt
CycloPepper: uma plataforma de aprendizado de máquina para prever resultados de ciclização e otimizar a síntese de ciclopeptídeos terapêuticos
Transformando cadeias flexíveis em anéis poderosos
Medicamentos contra o câncer, antibióticos e outras terapias modernas são cada vez mais construídos a partir de cadeias curtas de aminoácidos chamadas peptídeos. Quando essas cadeias são costuradas em anéis fechados, ou peptídeos cíclicos, frequentemente se tornam mais resistentes, duráveis e melhores em penetrar células. Mas fabricar esses minúsculos anéis no laboratório é surpreendentemente sensível, e químicos podem perder semanas tentando adivinhar qual posição usar para fechar a cadeia. Este estudo apresenta o CycloPepper, uma plataforma orientada por aprendizado de máquina que ajuda pesquisadores a prever, em segundos, quais cadeias peptídicas provavelmente formarão anéis estáveis e quais falharão, potencialmente acelerando a busca por novos medicamentos peptídicos.
Por que peptídeos em forma de anel importam
Peptídeos são sequências de aminoácidos, os mesmos blocos construtores das proteínas. Quando permanecem como cadeias abertas, podem ser frouxos e fáceis de serem degradados por enzimas do corpo. Se as duas extremidades da cadeia são unidas cabeça a cauda para formar um anel, a molécula fica mais compacta e rígida. Isso frequentemente melhora a afinidade pelo alvo biológico, a resistência a enzimas digestivas e a capacidade de atravessar membranas celulares. Diversos fármacos importantes, incluindo antibióticos potentes, baseiam‑se em tais estruturas cíclicas. Para projetistas de fármacos, transformar um peptídeo linear em um anel é uma estratégia central para converter uma molécula fraca e frágil em um remédio potente e duradouro.
A dificuldade oculta em fechar o anel
Apesar do apelo, peptídeos cíclicos são difíceis de sintetizar. Para formar um anel, uma cadeia flexível deve se dobrar justamente na conformação certa para que suas duas extremidades reajam entre si em vez de reagirem com um vizinho. Cadeias curtas, em particular, pagam um alto “custo organizacional” para adotar essa forma em laço, e aminoácidos volumosos perto do ponto de união podem fisicamente bloquear a reação. Químicos normalmente constroem peptídeos em minúsculas contas de um suporte sólido, o que simplifica a purificação mas pode restringir ainda mais a liberdade de dobramento da cadeia. Como resultado, o sucesso ou fracasso da formação do anel frequentemente depende sensivelmente de onde, ao longo de uma sequência por outro lado similar, o químico escolhe fechar o laço. Até agora, essa escolha tem sido, em grande parte, guiada pela experiência e tentativa e erro.
Robôs e algoritmos constroem uma biblioteca de aprendizado
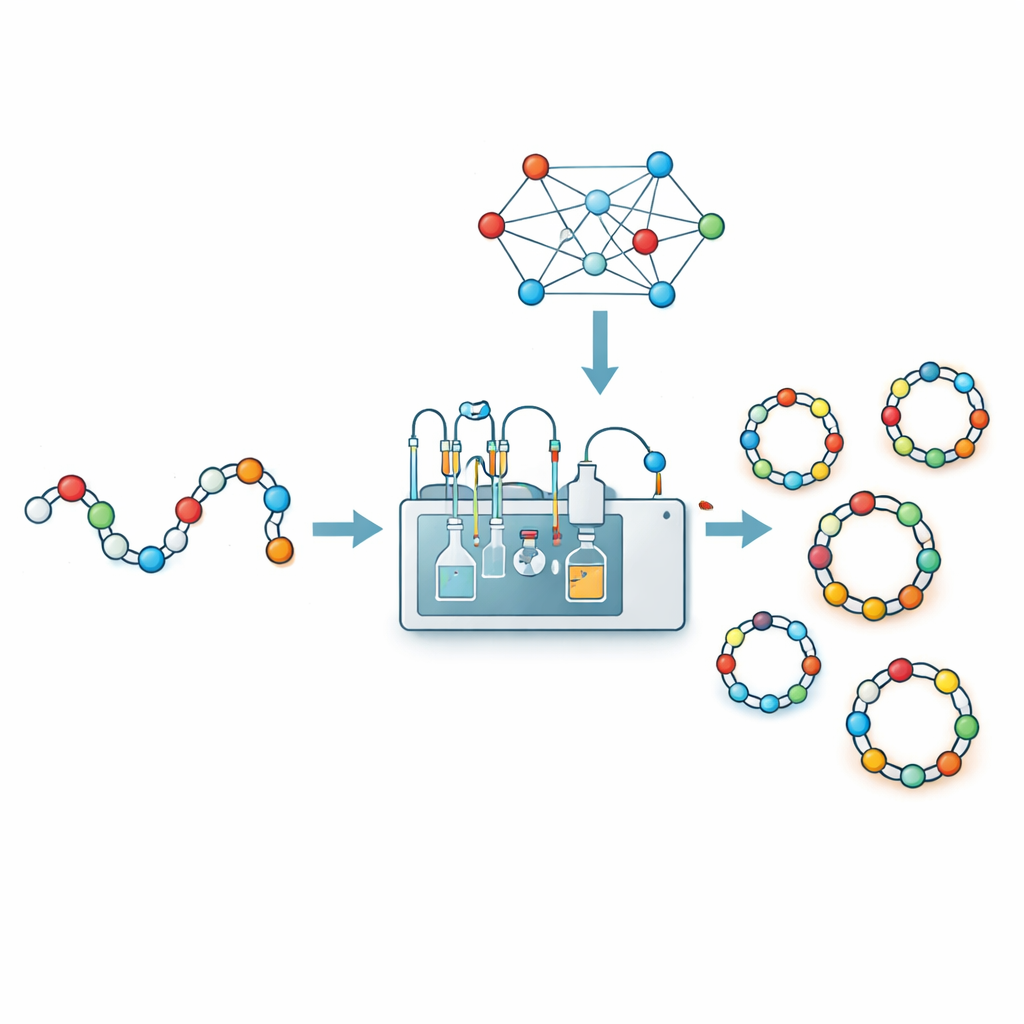
Para substituir suposições por dados, os pesquisadores combinaram química automatizada com aprendizado de máquina. Usando um sistema robótico de fluxo de síntese chamado CycloBot e um conector especial que permite o fechamento do anel diretamente no suporte sólido, eles rapidamente sintetizaram e testaram 306 diferentes cadeias peptídicas variando de 2 a 14 aminoácidos. Para cada sequência, registraram simplesmente se um produto cíclico limpo foi detectado ou não. Em seguida, traduziram cada sequência em uma descrição numérica rica: quais aminoácidos ela contém, como eles se ordenam em pares, um código posição a posição e um punhado de indicadores selecionados com base na experiência de laboratório (por exemplo, que certos aminoácidos nas extremidades tendem a ajudar ou atrapalhar a ciclização). Alimentando essas assinaturas de 414 dimensões em vários tipos de modelos de aprendizado de máquina, descobriram que um classificador de vetor de suporte forneceu o melhor desempenho, prevendo corretamente sucesso ou fracasso da ciclização em cerca de 84% das vezes em testes de validação cruzada.
Levando previsões ao teste experimental
A equipe então desafiou seu modelo com peptídeos novos que ele nunca havia visto. Eles projetaram oito sequências artificiais e quatro candidatos terapêuticos inspirados em sequências naturais, e para cada uma tentaram todas as posições possíveis para fechar o anel ao longo da cadeia. No total, realizaram 74 experimentos de ciclização. As previsões do modelo de aprendizado de máquina concordaram com os resultados de laboratório em 64 desses casos, uma precisão de 86%. Importante: o modelo foi eficiente em sinalizar tanto sítios promissores quanto desfavoráveis, ou seja, podia ajudar químicos a evitar desperdiçar esforço com sequências pouco cooperativas e também a destacar os candidatos mais prováveis de sucesso.
Uma ferramenta prática para projetistas de fármacos
Para tornar a abordagem útil além de seu próprio laboratório, os autores empacotaram o modelo treinado em uma plataforma pública chamada CycloPepper, disponível tanto como software baixável quanto como ferramenta web. Usuários podem digitar um único peptídeo ou enviar vários de uma vez e, em segundos, receber um mapa das posições de fechamento cabeça‑a‑cauda que têm maior probabilidade de funcionar. A equipe demonstrou seu valor projetando centenas de potenciais peptídeos cíclicos direcionados a proteínas envolvidas em câncer e doenças imunes, mostrando que a ferramenta pode rapidamente filtrar quase 40% das sequências que provavelmente não irão ciclizar. Para não especialistas, a conclusão é que o CycloPepper funciona como um assistente inteligente de pré‑triagem, reduzindo um vasto espaço de projeto a um conjunto prático de candidatos. Ao combinar síntese automatizada com algoritmos preditivos, este trabalho aproxima a promessa de descoberta mais rápida e racional de fármacos peptídicos em forma de anel de tornar‑se realidade.
Citação: Pan, Y., Hu, C., Li, J. et al. CycloPepper: a machine learning platform for predicting cyclization outcomes and optimizing synthesis of therapeutic cyclopeptides. Nat Commun 17, 2803 (2026). https://doi.org/10.1038/s41467-026-69441-w
Palavras-chave: peptídeos cíclicos, projeto de fármacos peptídicos, aprendizado de máquina na química, síntese automatizada, predição de ciclização