Clear Sky Science · it
CycloPepper: una piattaforma di machine learning per prevedere gli esiti della ciclizzazione e ottimizzare la sintesi di ciclopeptidi terapeutici
Trasformare catene flessibili in anelli potenti
I farmaci antitumorali, gli antibiotici e altre medicine moderne sono sempre più spesso costruiti a partire da brevi catene di amminoacidi chiamate peptidi. Quando queste catene vengono cucite a formare anelli chiusi, o peptidi ciclici, tendono a diventare più resistenti, duraturi e migliori nel penetrare nelle cellule. Ma fabbricare questi minuscoli anelli in laboratorio è sorprendentemente delicato, e i chimici possono sprecare settimane a indovinare come chiudere una catena. Questo studio presenta CycloPepper, una piattaforma guidata dal machine learning che aiuta i ricercatori a prevedere, in pochi secondi, quali catene peptidiche sono probabili candidate a formare anelli stabili e quali falliranno, accelerando potenzialmente la ricerca di nuovi farmaci peptidici.
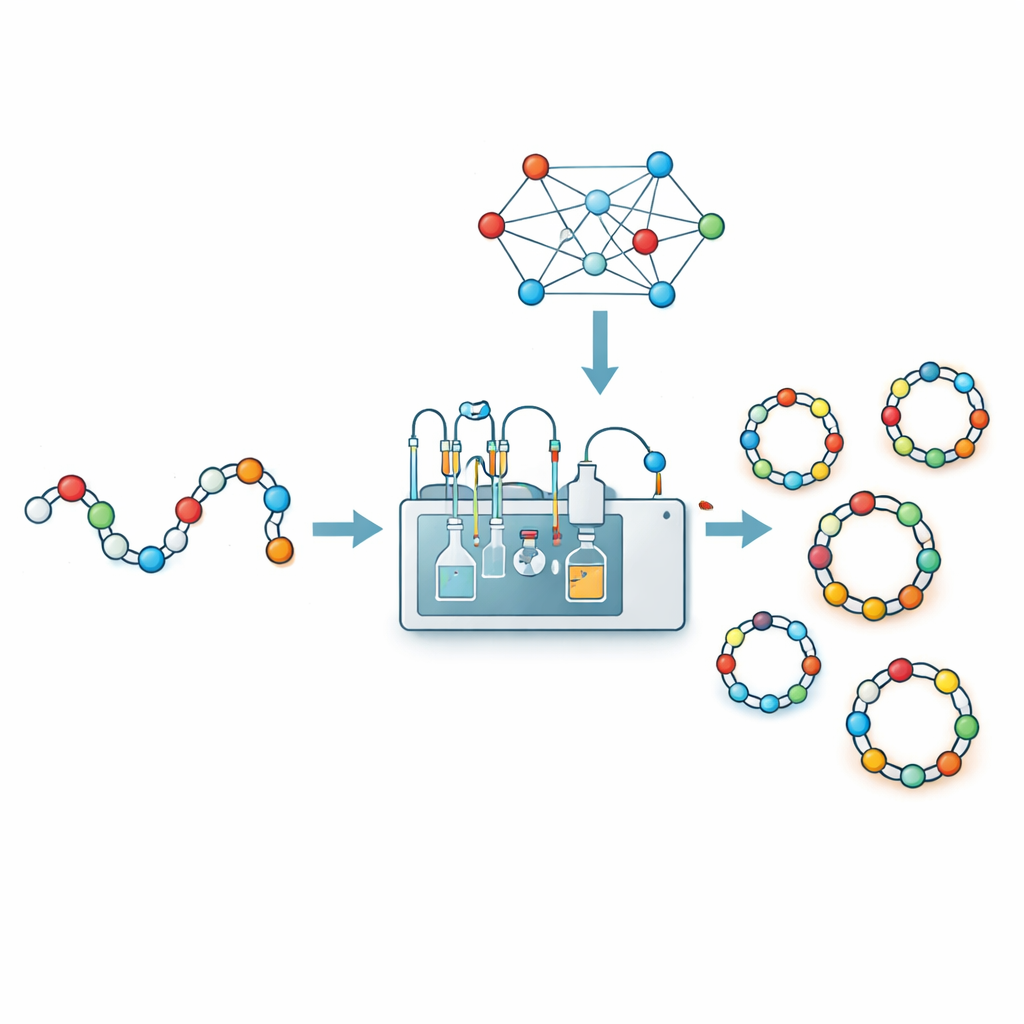
Perché i peptidi ad anello sono importanti
I peptidi sono sequenze di amminoacidi, gli stessi mattoni costitutivi delle proteine. Se lasciati come catene aperte possono essere flosci e facili prede degli enzimi presenti nell’organismo. Se le due estremità della catena vengono unite testa‑coda per formare un anello, la molecola diventa più compatta e rigida. Questo spesso migliora l’affinità per il bersaglio biologico, la resistenza alla degradazione enzimatica e la capacità di attraversare le membrane cellulari. Diversi farmaci importanti, inclusi potenti antibiotici, si basano su tali strutture cicliche. Per i progettisti di farmaci, trasformare un peptide lineare in un anello è una strategia chiave per convertire una molecola debole e fragile in un medicinale potente e durevole.
La difficoltà nascosta nel chiudere l’anello
Nonostante il loro interesse, i peptidi ciclici sono difficili da ottenere. Per formare un anello, una catena flessibile deve piegarsi nella conformazione giusta affinché le due estremità possano reagire tra loro invece che con un vicino. Le catene corte in particolare pagano un alto "costo organizzativo" per assumere questa forma ad anello, e amminoacidi ingombranti vicini al punto di giunzione possono fisicamente ostacolare la reazione. I chimici di solito sintetizzano i peptidi su piccole perle di materiale solido, il che semplifica la purificazione ma può limitare ulteriormente la libertà di piegatura della catena. Di conseguenza, il successo o il fallimento della formazione dell’anello dipende spesso in modo sensibile dal punto in cui, lungo una sequenza altrimenti simile, il chimico decide di chiudere il ciclo. Fino ad ora questa scelta è stata guidata in gran parte dall’esperienza e dal tentativo‑errore.
Robot e algoritmi costruiscono una libreria di apprendimento
Per sostituire l’indovinare con i dati, i ricercatori hanno combinato chimica automatizzata e machine learning. Utilizzando un sistema robotico di flow‑synthesis chiamato CycloBot e un linker speciale che permette la chiusura dell’anello direttamente sul supporto solido, hanno rapidamente sintetizzato e testato 306 diverse catene peptidiche di lunghezza compresa tra 2 e 14 amminoacidi. Per ogni sequenza hanno semplicemente registrato se è stato rilevato o meno un prodotto ciclico pulito. Hanno quindi tradotto ogni sequenza in una ricca descrizione numerica: quali amminoacidi contiene, come sono ordinati in coppie, un codice posizione per posizione e una manciata di flag scelti a mano basati sull’esperienza di laboratorio (per esempio, che certi amminoacidi alle estremità tendono ad aiutare o ostacolare la formazione dell’anello). Alimentando queste impronte digitali a 414 dimensioni in diversi tipi di modelli di machine learning, hanno trovato che un classificatore a vettori di supporto offriva la migliore prestazione, prevedendo correttamente il successo o il fallimento della ciclizzazione circa l’84 percento delle volte nei test di cross‑validation.
Mettere le previsioni alla prova sperimentale
Il team ha quindi sfidato il modello con peptidi nuovi che non aveva mai visto. Hanno progettato otto sequenze artificiali e quattro candidati terapeutici ispirati a peptidi naturali, e per ciascuno hanno provato tutti i possibili punti di chiusura lungo la catena. In totale hanno eseguito 74 esperimenti di ciclizzazione. Le previsioni del modello di machine learning corrispondevano ai risultati di laboratorio in 64 di questi casi, per una accuratezza dell’86 percento. È importante che il modello fosse bravo a segnalare sia siti promettenti sia siti sfavorevoli, il che significa che potrebbe aiutare i chimici a evitare di sprecare sforzi su sequenze poco cooperative e allo stesso tempo evidenziare i candidati più probabili al successo.
Uno strumento pratico per i progettisti di farmaci
Per rendere l’approccio utile oltre il proprio laboratorio, gli autori hanno incapsulato il modello addestrato in una piattaforma pubblica chiamata CycloPepper, disponibile sia come software scaricabile sia come strumento web. Gli utenti possono inserire un singolo peptide o caricarne molti insieme e, nel giro di pochi secondi, ricevere una mappa dei punti di chiusura testa‑coda più probabili. Il team ha dimostrato il valore dello strumento progettando centinaia di potenziali peptidi ciclici diretti contro proteine coinvolte in tumori e malattie immunitarie, mostrando che lo strumento può rapidamente scartare quasi il 40 percento delle sequenze improbabili da ciclizzare. Per i non specialisti, il messaggio è che CycloPepper funziona come un assistente di pre‑screening intelligente, riducendo un vasto spazio di progettazione a un insieme pratico di candidati. Combinando sintesi automatizzata e algoritmi predittivi, questo lavoro avvicina la promessa di una scoperta più rapida e razionale di farmaci peptidici ad anello alla realtà.
Citazione: Pan, Y., Hu, C., Li, J. et al. CycloPepper: a machine learning platform for predicting cyclization outcomes and optimizing synthesis of therapeutic cyclopeptides. Nat Commun 17, 2803 (2026). https://doi.org/10.1038/s41467-026-69441-w
Parole chiave: peptidi ciclici, progettazione di farmaci peptidici, machine learning in chimica, sintesi automatizzata, predizione della ciclizzazione