Clear Sky Science · ru
CycloPepper: платформа машинного обучения для прогнозирования результатов циклизации и оптимизации синтеза терапевтических циклопептидов
Преобразование гибких цепочек в мощные кольца
Препараты от рака, антибиотики и другие современные лекарства всё чаще создают из коротких цепочек аминокислот, называемых пептидами. Когда такие цепочки сшивают в замкнутые кольца — циклические пептиды — они часто становятся прочнее, более стабильными и лучше проникают в клетки. Но синтез этих крошечных колец в лаборатории оказывается удивительно капризным: химики могут тратить недели на попытки угадать, каким образом лучше замкнуть цепочку. В этом исследовании представлена CycloPepper — платформа на основе машинного обучения, помогающая исследователям за секунды прогнозировать, какие пептидные цепочки вероятно образуют стабильные кольца, а какие потерпят неудачу, что может существенно ускорить поиск новых пептидных лекарств.
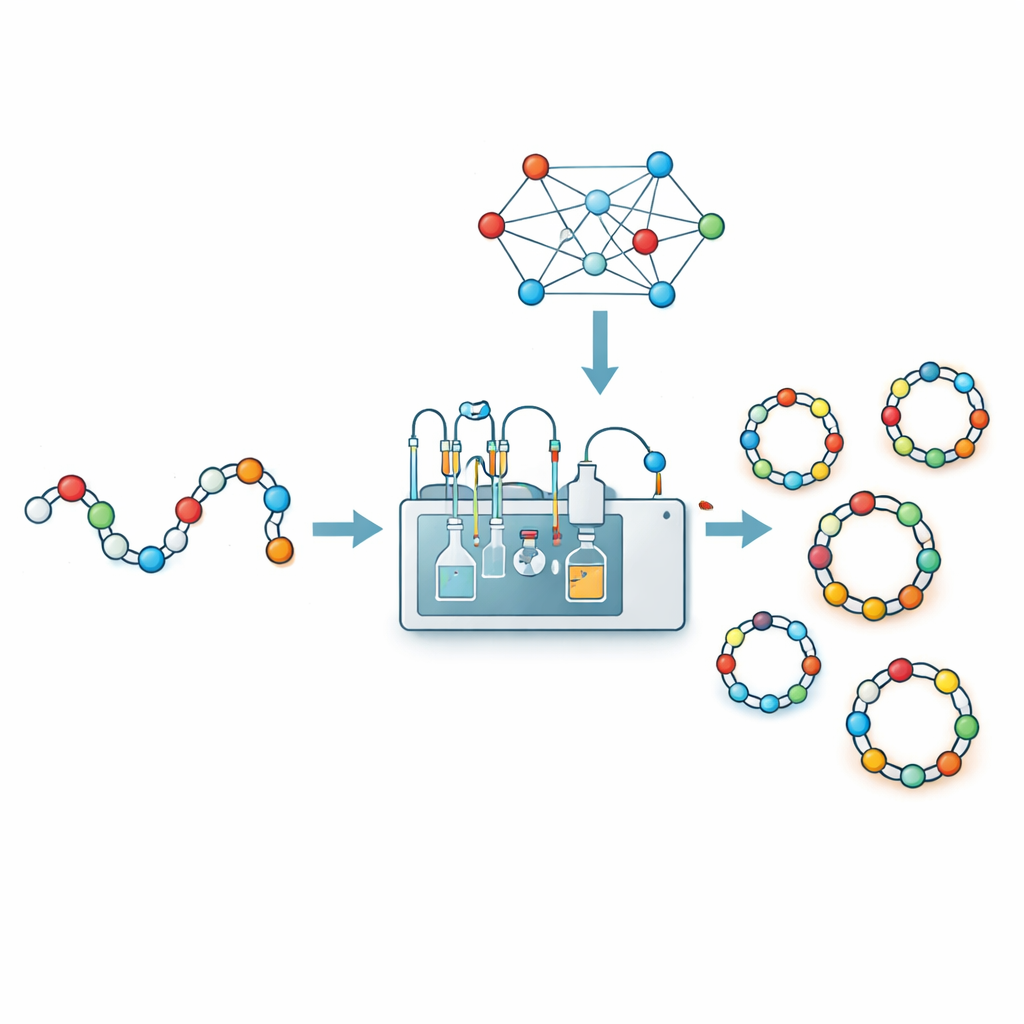
Почему циклические пептиды важны
Пептиды — это цепочки аминокислот, тех же строительных блоков, что и в белках. В открытом виде они могут быть вялыми и легко разрушаться ферментами в организме. Если два конца цепочки соединить «голова‑в‑хвост» и получить кольцо, молекула становится более компактной и жёсткой. Часто это улучшает аффинность к биологической мишени, устойчивость к перевариванию ферментами и способность пересекать клеточные мембраны. Несколько важных лекарств, включая мощные антибиотики, основаны на таких циклических структурах. Для разработчиков лекарств превращение линейного пептида в кольцо — ключевая стратегия для преобразования слабой, хрупкой молекулы в сильное и долговечное средство.
Скрытая сложность при замыкании кольца
Несмотря на все преимущества, циклические пептиды трудно синтезировать. Для образования кольца гибкая цепочка должна сложиться в точную конфигурацию, чтобы её два конца реагировали друг с другом, а не с соседней цепью. Особенно короткие цепи «платят» высокую «организационную цену», чтобы принять эту петлеобразную форму, а громоздкие аминокислоты рядом с местом соединения могут физически мешать реакции. Химики обычно строят пептиды на крошечных твёрдых шариках, что упрощает очистку, но дополнительно ограничивает свободу складывания цепочки. В результате успешность или неудача образования кольца часто очень чувствительны к тому, в каком месте, вдоль в остальном похожей последовательности, химик решает замкнуть петлю. До сих пор этот выбор во многом определялся опытом и методом проб и ошибок.
Роботы и алгоритмы создают библиотеку знаний
Чтобы заменить догадки данными, исследователи объединили автоматизированную химию и машинное обучение. С помощью роботизированной системы потокового синтеза CycloBot и специального линкера, позволяющего осуществлять замыкание прямо на твёрдой опоре, они быстро синтезировали и протестировали 306 различных пептидных цепочек длиной от 2 до 14 аминокислот. Для каждой последовательности они просто фиксировали, был ли обнаружен чистый циклический продукт или нет. Затем каждую последовательность перевели в богатое численное описание: какие аминокислоты она содержит, как они упорядочены в парах, позиционно‑по‑позиции код и несколько вручную отобранных признаков, основанных на лабораторном опыте (например, что некоторые аминокислоты на концах обычно способствуют или мешают образованию кольца). Введя эти 414‑мерные отпечатки в несколько типов моделей машинного обучения, они обнаружили, что наилучший результат показал классификатор опорных векторов, правильно прогнозируя успех или неудачу циклизации примерно в 84 процента случаев при кросс‑валидации.
Проверка прогнозов в экспериментах
Затем команда проверила модель на новых пептидах, которых она не видела ранее. Они спроектировали восемь искусственных последовательностей и четыре натуралистично вдохновлённых терапевтических кандидата, и для каждой пробовали все возможные места замыкания вдоль цепочки. В сумме было проведено 74 эксперимента по циклизации. Прогнозы модели совпали с лабораторными результатами в 64 случаях, что соответствует точности 86 процентов. Важно, что модель хорошо отмечала как перспективные, так и неблагоприятные сайты, то есть могла помочь химикам избежать пустой траты времени на плохо поддающиеся последовательности и одновременно выделять наиболее вероятные кандидаты.
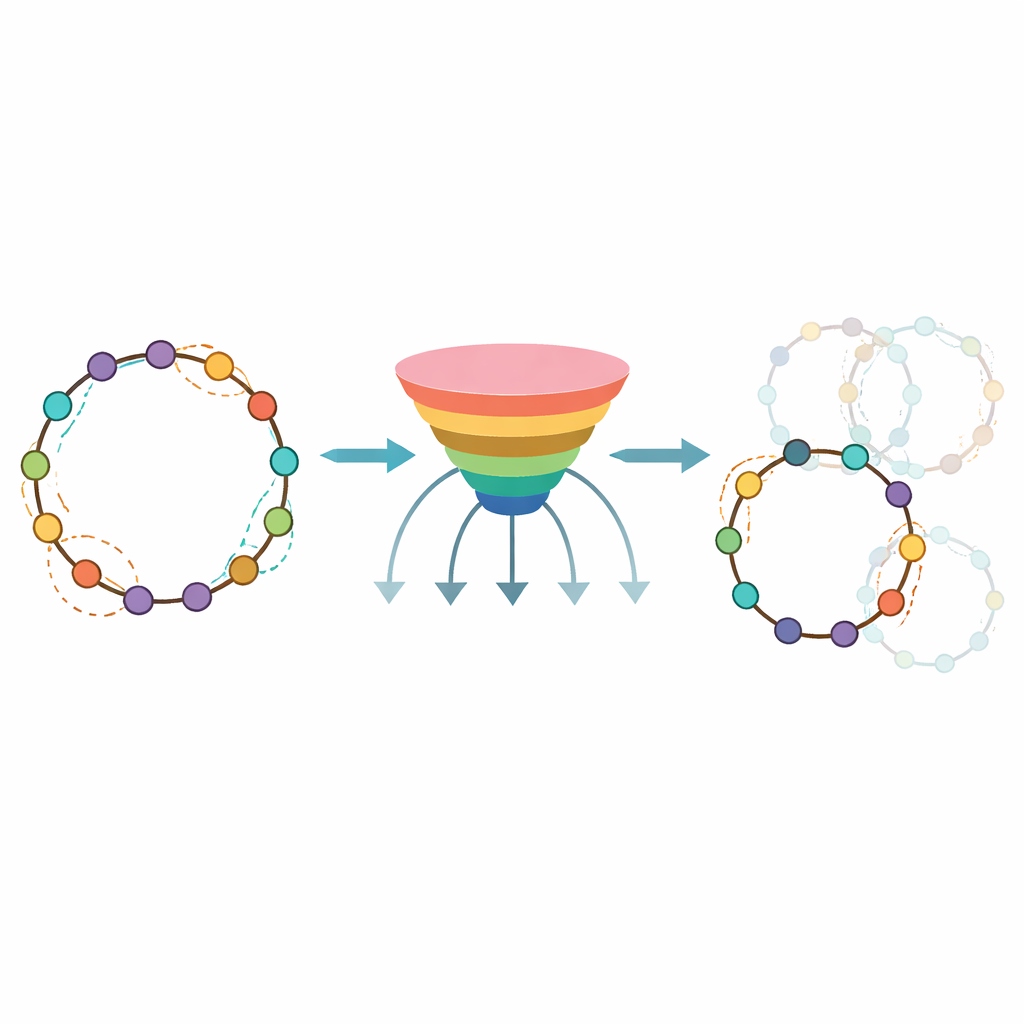
Практический инструмент для разработчиков лекарств
Чтобы сделать подход полезным за пределами своей лаборатории, авторы упаковали обученную модель в публичную платформу CycloPepper, доступную как в виде загружаемого ПО, так и веб‑сервиса. Пользователи могут ввести один пептид или загрузить множество последовательностей и в течение секунд получить карту мест «голова‑в‑хвост», которые, вероятно, будут работать. Команда продемонстрировала её полезность, спроектировав сотни потенциальных циклических пептидов, нацеленных на белки, связанные с раком и заболеваниями иммунной системы, показав, что инструмент быстро отсекает почти 40 процентов последовательностей, маловероятных к циклизации. Для неспециалистов вывод прост: CycloPepper выступает как умный помощник предварительного отбора, сокращая огромное пространство проектирования до практического набора кандидатов. Объединив автоматизированный синтез с предиктивными алгоритмами, эта работа приближает обещание более быстрой и рациональной разработки кольцевых пептидных лекарств к реальности.
Цитирование: Pan, Y., Hu, C., Li, J. et al. CycloPepper: a machine learning platform for predicting cyclization outcomes and optimizing synthesis of therapeutic cyclopeptides. Nat Commun 17, 2803 (2026). https://doi.org/10.1038/s41467-026-69441-w
Ключевые слова: циклические пептиды, дизайн пептидных препаратов, машинное обучение в химии, автоматизированный синтез, прогнозирование циклизации