Clear Sky Science · tr
CycloPepper: terapötik siklopeptidlerin siklizasyon sonuçlarını tahmin etmek ve sentezi optimize etmek için makine öğrenimi platformu
Esnek zincirleri güçlü halkalara dönüştürmek
Kanser ilaçları, antibiyotikler ve diğer modern ilaçlar giderek peptidler olarak adlandırılan kısa amino asit zincirlerinden inşa ediliyor. Bu zincirler kapalı halkalar hâline dikildiğinde, yani siklik peptidler oluşturduklarında, genellikle daha dayanıklı, daha uzun ömürlü ve hücrelere girmede daha başarılı olurlar. Ancak bu minik halkaları laboratuvarda yapmak şaşırtıcı derecede hassastır ve kimyagerler zinciri hangi şekilde kapatacaklarını tahmin etmek için haftalar harcayabilir. Bu çalışma, peptid zincirlerinin hangi bölümlerinin kararlı halkalar oluşturma olasılığının yüksek olduğunu ve hangilerinin başarısız olacağını saniyeler içinde tahmin etmeye yardımcı olan makine öğrenimi destekli CycloPepper platformunu tanıtıyor; bu da yeni peptid ilaç arayışını hızlandırabilir.
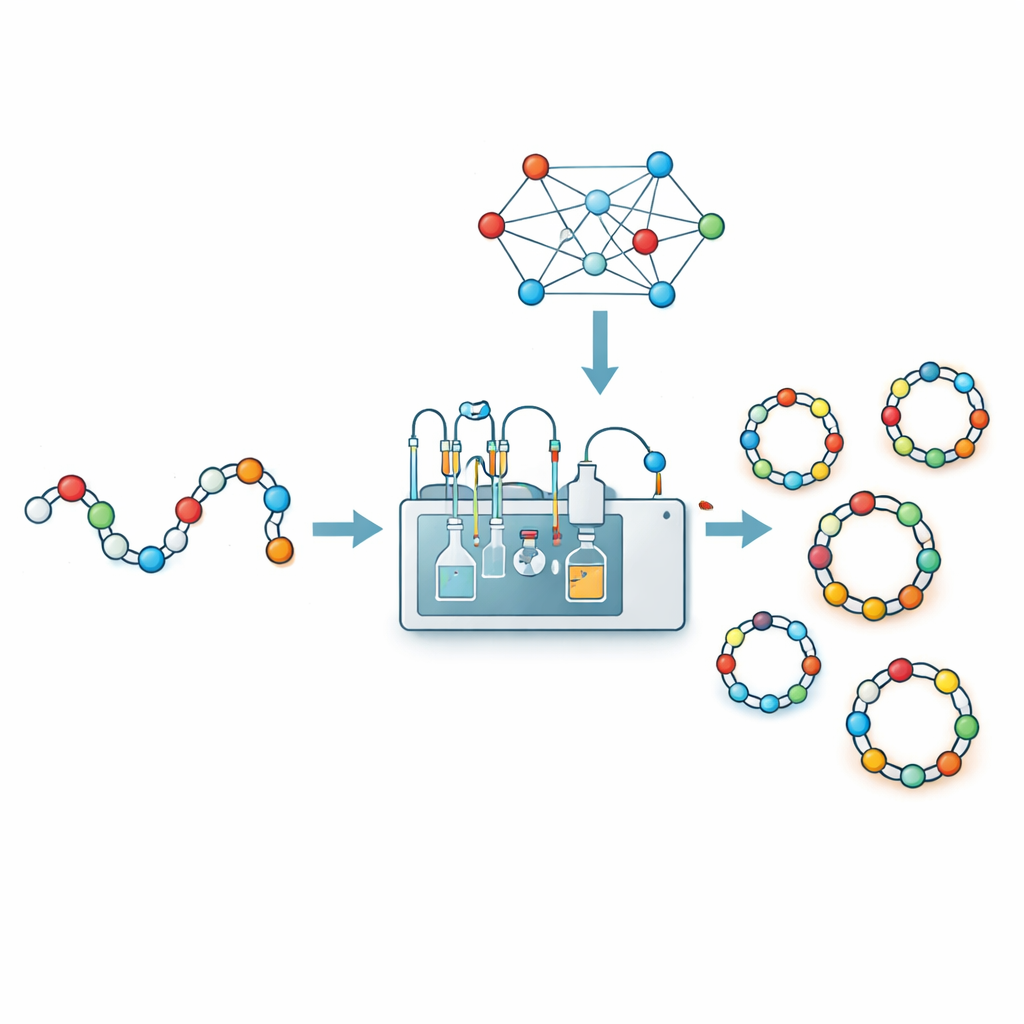
Neden halka biçimli peptidler önemli
Peptidler, proteinleri oluşturan aynı yapı taşları olan amino asitlerin dizileridir. Açık zincir hâlinde bırakıldıklarında gevşek olabilir ve vücutta enzimler tarafından kolayca parçalanabilirler. Zincirin iki ucu baş‑kuyruk birleştirilerek bir halka oluşturulduğunda molekül daha kompakt ve rijit hâle gelir. Bu genellikle biyolojik hedefe bağlanma gücünü, sindirim enzimlerine karşı dayanımını ve hücre zarlarını geçme yeteneğini iyileştirir. Güçlü antibiyotikleri de içeren birkaç önemli ilaç bu tür siklik yapılara dayanır. İlaç tasarımcıları için lineer bir peptidi halka hâline getirmek, zayıf ve kırılgan bir molekülü etkili ve dayanıklı bir ilaca dönüştürmenin anahtar stratejilerinden biridir.
Halkanın kapatılmasındaki gizli zorluk
Cazibesine rağmen siklik peptidler yapmak zordur. Bir halka oluşturmak için esnek bir zincirin uçlarının birbirleriyle reaksiyona girebilecek şekilde tam olarak doğru biçimde katlanması gerekir; komşularıyla reaksiyona girmemelidir. Özellikle kısa zincirler, bu döngüsel şekli benimsemek için yüksek bir “organizasyon maliyeti” öder ve birleşme noktasına yakın kalabalık amino asitler reaksiyonu fiziksel olarak engelleyebilir. Kimyagerler genellikle peptidleri saflaştırmayı kolaylaştıran küçük katı destek boncukları üzerinde sentezler; bu da zincirin serbestçe katlanmasını daha da kısıtlayabilir. Sonuç olarak, halkanın başarılı olup olmaması sıklıkla, aksi takdirde benzer bir dizide kimyagerin döngüyü nerede kapatmayı seçtiğine hassas biçimde bağlıdır. Bugüne kadar bu seçim çoğunlukla deneyim ve deneme‑yanılma ile yönlendirilmiştir.
Robotlar ve algoritmalar öğrenen bir kütüphane oluşturuyor
Tahminleri veriye dayandırmak için araştırmacılar otomatik kimyayı makine öğrenimi ile birleştirdiler. CycloBot adındaki robotik akış‑sentez sistemi ve halka kapatılmasının katı destek üzerinde doğrudan gerçekleşmesine izin veren özel bir bağlayıcı kullanarak, 2 ila 14 amino aside kadar değişen 306 farklı peptid zincirini hızla ürettiler ve test ettiler. Her dizinin temiz bir siklik ürün verip vermediğini kaydettiler. Ardından her diziyi zengin bir sayısal tanıma dönüştürdüler: hangi amino asitleri içerdiği, ikili sıralama düzenleri, pozisyon‑bazlı bir kod ve laboratuvar deneyimine dayanan birkaç el ile seçilmiş işaretçi (örneğin, belirli amino asitlerin uçlarda olması halkalaşmayı kolaylaştırma veya engelleme eğilimi). Bu 414 boyutlu parmak izlerini birkaç tür makine öğrenimi modeline verdiklerinde, destek vektör sınıflandırıcısının en iyi performansı verdiğini ve çapraz doğrulama testlerinde siklizasyon başarısını veya başarısızlığını yaklaşık yüzde 84 doğrulukla tahmin ettiğini buldular.
Tahminleri deneysel olarak test etmek
Ardından ekip, modellerini daha önce hiç görmediği yeni peptidlerle test etti. Sekiz yapay dizi ve dört doğal esinli terapötik aday tasarladılar ve her biri için zincir boyunca halkanın kapatılabileceği tüm olası yerleri denediler. Toplamda 74 siklizasyon deneyi gerçekleştirdiler. Makine öğrenimi modelinin tahminleri, 64 vakada laboratuvar sonuçlarıyla örtüştü; bu da yüzde 86 doğruluk demekti. Önemli olarak, model hem umut verici hem de zayıf kapanma bölgelerini iyi şekilde işaretleyebiliyordu; bu da kimyagerlerin işbirliği yapmayan diziler üzerinde zaman kaybetmesini önlemeye yardımcı olmasının yanı sıra en olası başarılı bölgeleri öne çıkarabileceği anlamına gelir.
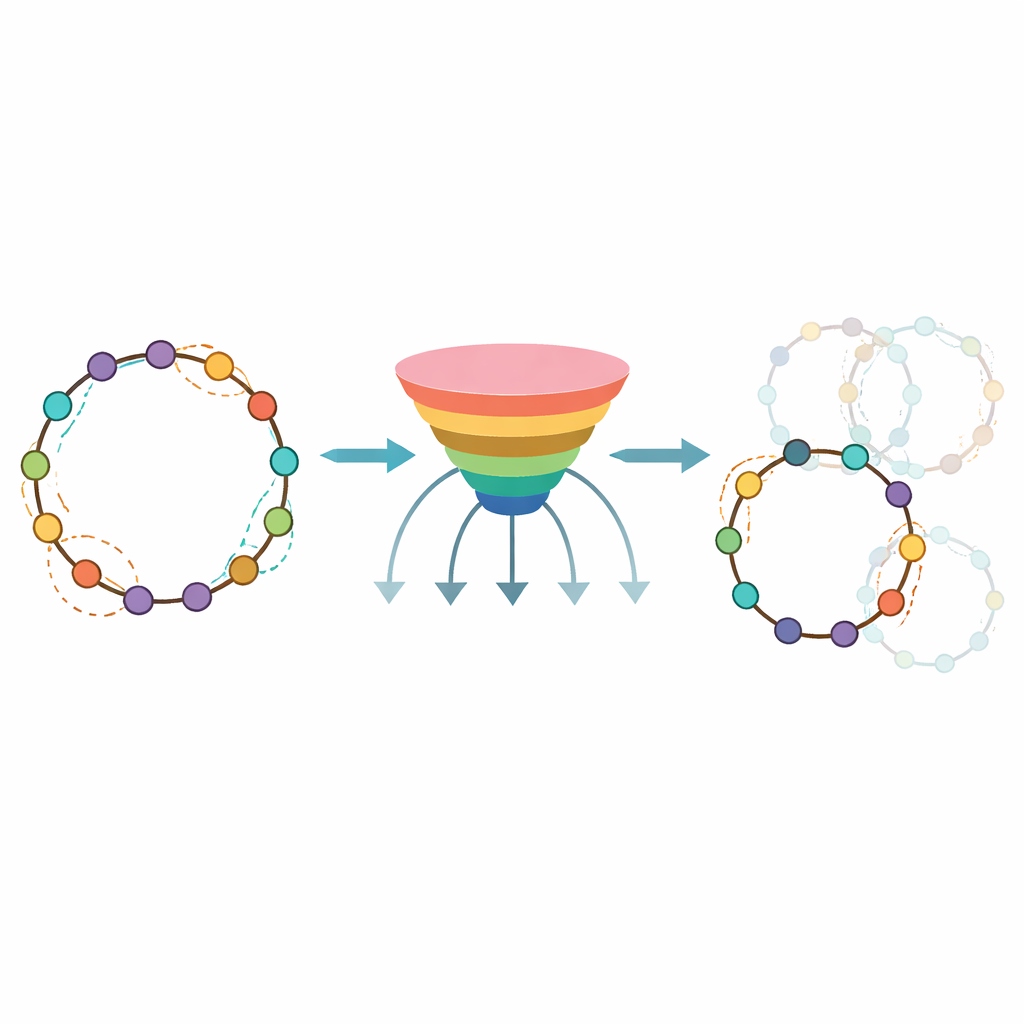
İlaç tasarımcıları için pratik bir araç
Yaklaşımlarını kendi laboratuvarlarının ötesinde faydalı kılmak için yazarlar eğitilmiş modeli CycloPepper adında herkese açık bir platforma dönüştürdüler; bu platform hem indirilebilir yazılım hem de web aracı olarak sunuluyor. Kullanıcılar tek bir peptidi yazabilir veya birden fazlasını toplu olarak yükleyebilir ve saniyeler içinde hangi baş‑kuyruk kapatma noktalarının çalışmasının muhtemel olduğuna dair bir harita alırlar. Ekip, kanser ve bağışıklık hastalıklarıyla ilişkili protein hedeflerine yönelik yüzlerce potansiyel siklik peptid tasarlayarak aracın değerini gösterdi; araç, siklize olma olasılığı düşük yaklaşık yüzde 40 diziyi hızla filtreleyebildi. Uzman olmayanlar için çıkarım şu: CycloPepper akıllı bir ön‑eleme asistanı gibi çalışarak geniş bir tasarım alanını pratik bir aday setine daraltıyor. Otomatik sentezi öngörücü algoritmalarla birleştirerek, bu çalışma halka biçimli peptid ilaçların daha hızlı ve daha akılcı keşfini bir adım daha yakına getiriyor.
Atıf: Pan, Y., Hu, C., Li, J. et al. CycloPepper: a machine learning platform for predicting cyclization outcomes and optimizing synthesis of therapeutic cyclopeptides. Nat Commun 17, 2803 (2026). https://doi.org/10.1038/s41467-026-69441-w
Anahtar kelimeler: siklik peptidler, peptid ilaç tasarımı, kimyada makine öğrenimi, otomatik sentez, siklizasyon tahmini