Clear Sky Science · fr
CycloPepper : une plateforme d’apprentissage automatique pour prédire l’issue des cyclisations et optimiser la synthèse de cyclopeptides thérapeutiques
Transformer des chaînes flexibles en anneaux puissants
Les médicaments contre le cancer, les antibiotiques et d’autres traitements modernes sont de plus en plus constitués de courtes chaînes d’acides aminés appelées peptides. Lorsque ces chaînes sont cousues en anneaux fermés, ou peptides cycliques, elles deviennent souvent plus solides, plus durables et meilleures pour pénétrer dans les cellules. Mais fabriquer ces minuscules anneaux en laboratoire est étonnamment délicat, et les chimistes peuvent perdre des semaines à deviner comment refermer une chaîne. Cette étude présente CycloPepper, une plateforme pilotée par apprentissage automatique qui aide les chercheurs à prédire, en quelques secondes, quelles chaînes peptidiques sont susceptibles de former des anneaux stables et lesquelles échoueront, accélérant potentiellement la découverte de nouveaux médicaments peptidiques.
Pourquoi les peptides en forme d’anneau sont importants
Les peptides sont des chaînes d’acides aminés, les mêmes briques de construction que les protéines. Lorsqu’ils restent sous forme de chaînes ouvertes, ils peuvent être mous et faciles à dégrader par les enzymes de l’organisme. Si les deux extrémités de la chaîne sont reliées tête‑queue pour former un anneau, la molécule devient plus compacte et rigide. Cela améliore souvent son affinité pour sa cible biologique, sa résistance aux enzymes digestives et sa capacité à traverser les membranes cellulaires. Plusieurs médicaments importants, dont des antibiotiques puissants, reposent sur de telles structures cycliques. Pour les concepteurs de médicaments, transformer un peptide linéaire en anneau est une stratégie clé pour métamorphoser une molécule faible et fragile en un médicament puissant et durable.
La difficulté cachée de la fermeture de l’anneau
Malgré leur intérêt, les peptides cycliques sont difficiles à synthétiser. Pour former un anneau, une chaîne flexible doit se replier dans la bonne conformation afin que ses deux extrémités réagissent entre elles plutôt qu’avec une voisine. Les chaînes courtes paient en particulier un lourd « coût d’organisation » pour adopter cette forme bouclée, et des acides aminés encombrants proches du point de jonction peuvent bloquer physiquement la réaction. Les chimistes construisent généralement les peptides sur de minuscules billes de support solide, ce qui simplifie la purification mais restreint encore la liberté de repliement de la chaîne. En conséquence, le succès ou l’échec de la formation de l’anneau dépend souvent de manière très sensible de l’endroit, le long d’une séquence par ailleurs semblable, où le chimiste choisit de fermer la boucle. Jusqu’à présent, ce choix a été guidé principalement par l’expérience et l’essai‑erreur.
Des robots et des algorithmes construisent une bibliothèque d’apprentissage
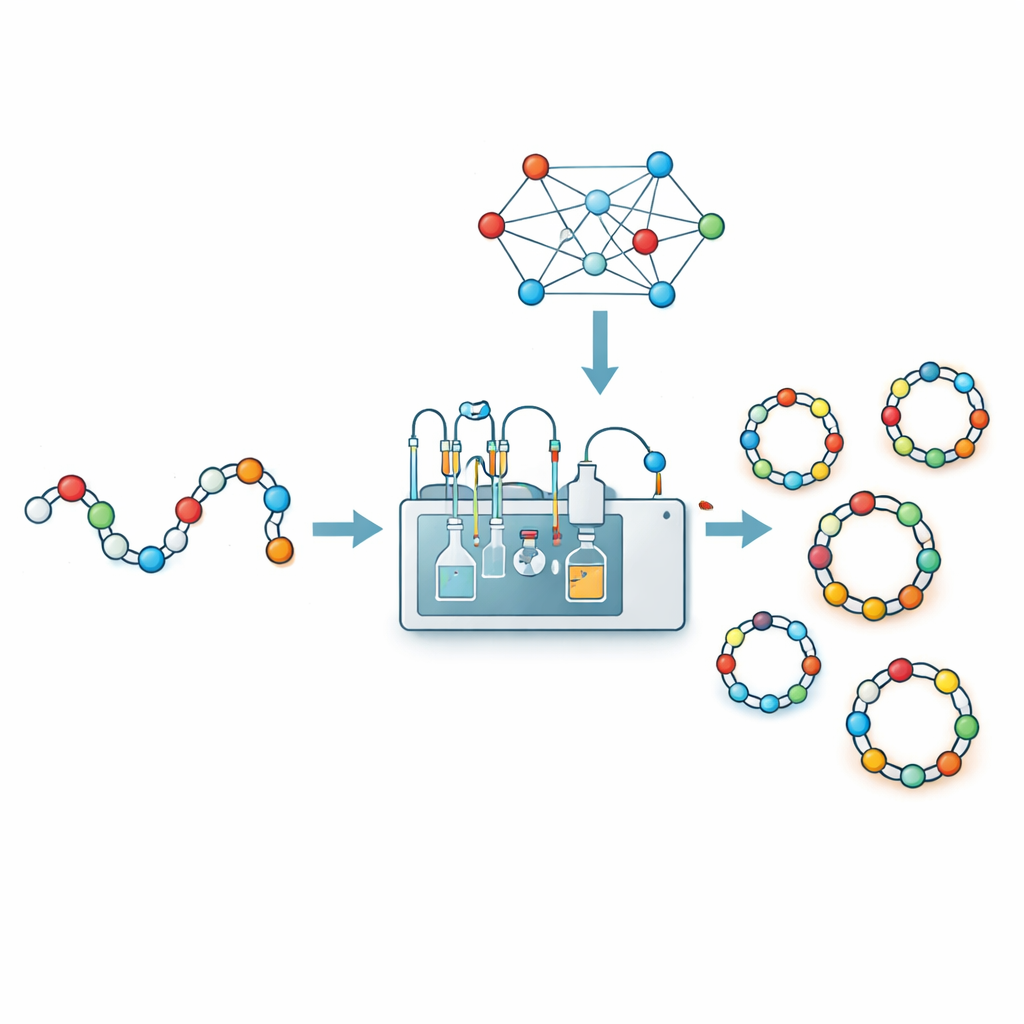
Pour remplacer les conjectures par des données, les chercheurs ont combiné chimie automatisée et apprentissage automatique. Utilisant un système robotisé de synthèse en flux appelé CycloBot et un linker spécial permettant la fermeture directement sur le support solide, ils ont rapidement synthétisé et testé 306 chaînes peptidiques différentes allant de 2 à 14 acides aminés. Pour chaque séquence, ils ont simplement enregistré si un produit cyclique propre était détecté ou non. Ils ont ensuite transformé chaque séquence en une description numérique riche : quels acides aminés elle contient, comment ils sont ordonnés par paires, un codage position par position, et une poignée de indicateurs sélectionnés à la main sur la base de l’expérience de laboratoire (par exemple, que certains acides aminés aux extrémités tendent à favoriser ou à gêner la cyclisation). En alimentant ces empreintes à 414 dimensions dans plusieurs types de modèles d’apprentissage automatique, ils ont constaté qu’un classificateur à vecteurs de support offrait la meilleure performance, prédisant correctement le succès ou l’échec de la cyclisation dans environ 84 % des cas lors de tests de validation croisée.
Mettre les prédictions à l’épreuve expérimentale
L’équipe a ensuite mis son modèle au défi avec des peptides nouveaux pour lui. Ils ont conçu huit séquences artificielles et quatre candidats thérapeutiques d’inspiration naturelle, et pour chacune ont essayé tous les emplacements possibles de fermeture le long de la chaîne. Au total, ils ont réalisé 74 expériences de cyclisation. Les prédictions du modèle d’apprentissage automatique correspondaient aux résultats de laboratoire dans 64 de ces cas, soit une précision de 86 %. Il est important de noter que le modèle était capable de signaler à la fois les sites prometteurs et les sites non propices, ce qui signifie qu’il peut aider les chimistes à éviter de perdre du temps sur des séquences difficiles et à mettre en avant les options les plus prometteuses.
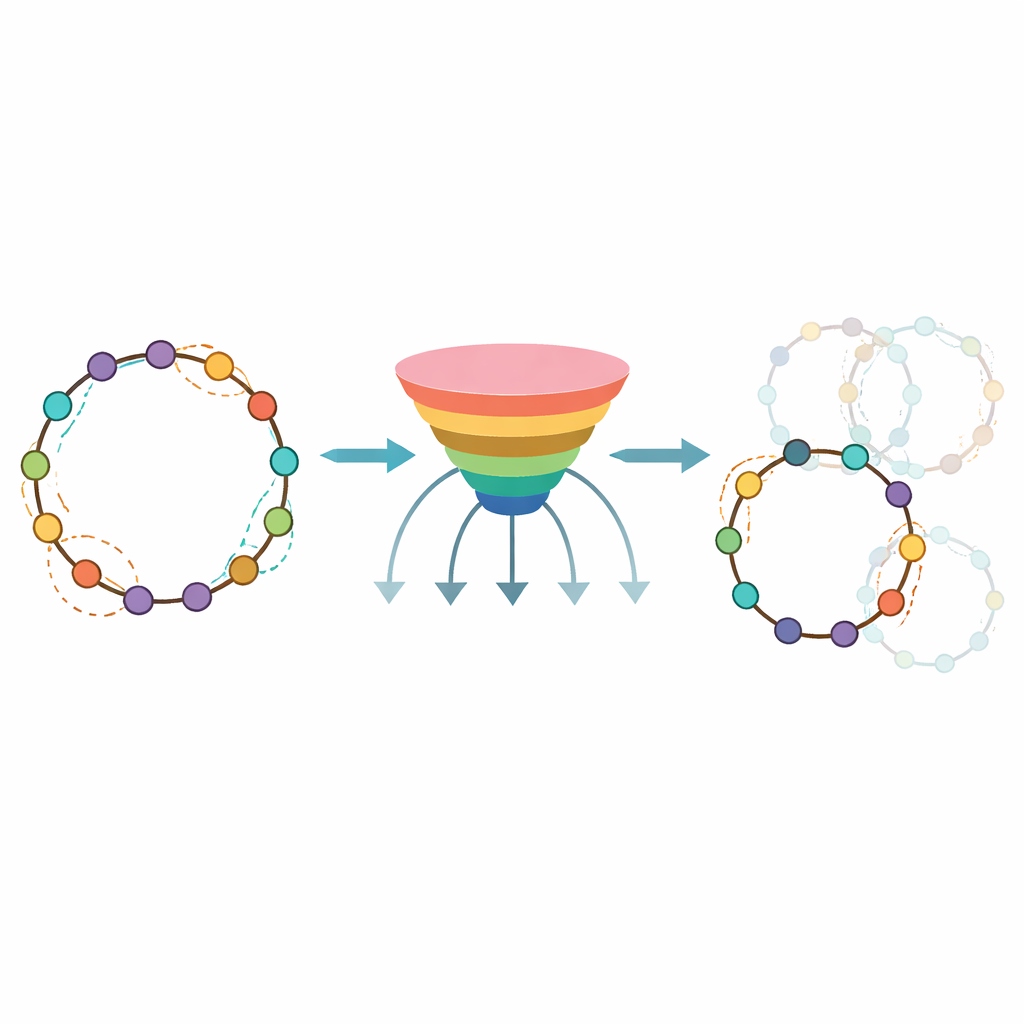
Un outil pratique pour les concepteurs de médicaments
Pour rendre leur approche utile au‑delà de leur propre laboratoire, les auteurs ont empaqueté le modèle entraîné dans une plateforme publique appelée CycloPepper, disponible à la fois en logiciel téléchargeable et en outil web. Les utilisateurs peuvent saisir un peptide unique ou en téléverser plusieurs à la fois, et recevoir en quelques secondes une carte des sites de fermeture tête‑queue susceptibles de fonctionner. L’équipe a démontré sa valeur en concevant des centaines de peptides cycliques potentiels ciblant des protéines impliquées dans le cancer et les maladies immunitaires, montrant que l’outil peut rapidement filtrer près de 40 % des séquences peu susceptibles de cycliser. Pour les non‑spécialistes, la conclusion est que CycloPepper agit comme un assistant de présélection intelligent, réduisant un vaste espace de conception à un ensemble pratique de candidats. En combinant synthèse automatisée et algorithmes prédictifs, ce travail rapproche la découverte plus rapide et plus rationnelle de médicaments peptidiques en forme d’anneau d’une application concrète.
Citation: Pan, Y., Hu, C., Li, J. et al. CycloPepper: a machine learning platform for predicting cyclization outcomes and optimizing synthesis of therapeutic cyclopeptides. Nat Commun 17, 2803 (2026). https://doi.org/10.1038/s41467-026-69441-w
Mots-clés: peptides cycliques, conception de médicaments peptidiques, apprentissage automatique en chimie, synthèse automatisée, prédiction de cyclisation