Clear Sky Science · nl
CycloPepper: een machinelearningplatform voor het voorspellen van cyclisatie-uitkomsten en het optimaliseren van de synthese van therapeutische cyclopeptiden
Flexibele ketens veranderen in krachtige ringen
Kankergeneesmiddelen, antibiotica en andere moderne medicijnen worden steeds vaker opgebouwd uit korte ketens aminozuren, peptide genoemd. Wanneer deze ketens tot gesloten ringen worden genaaid, of cyclische peptiden vormen, worden ze vaak steviger, langer houdbaar en beter in staat om in cellen te dringen. Het synthetiseren van deze kleine ringen in het lab blijkt echter verrassend lastig, en chemici kunnen weken verspillen met uitproberen welke manier van sluiten werkt. Deze studie introduceert CycloPepper, een door machine learning aangedreven platform dat onderzoekers in seconden helpt voorspellen welke peptideketens waarschijnlijk stabiele ringen vormen en welke falen, en zo mogelijk de zoektocht naar nieuwe peptidegeneesmiddelen versnelt.
Waarom ringvormige peptiden ertoe doen
Peptiden zijn rijtjes aminozuren, dezelfde bouwstenen als eiwitten. Als ze als open ketens blijven, kunnen ze slapper zijn en zijn ze gemakkelijk door enzymen in het lichaam af te breken. Wanneer de twee uiteinden van de keten kop‑naar‑staart aan elkaar worden verbonden om een ring te vormen, wordt het molecuul compacter en stijver. Dat verbetert vaak hoe sterk het aan het biologische doel bindt, hoe goed het enzymen overleeft en hoe eenvoudig het door celmembranen kan gaan. Verschillende belangrijke geneesmiddelen, waaronder krachtige antibiotica, zijn gebaseerd op zulke cyclische structuren. Voor geneesmiddelontwerpers is het omzetten van een lineair peptide in een ring een belangrijke strategie om een zwak, kwetsbaar molecuul om te vormen tot een krachtige en duurzame therapie.
De verborgen moeilijkheid bij het sluiten van de ring
Ondanks hun aantrekkingskracht zijn cyclische peptiden moeilijk te maken. Om een ring te vormen moet een flexibele keten in precies de juiste vorm vouwen zodat de twee uiteinden met elkaar reageren in plaats van met een buur. Vooral korte ketens betalen een hoge "organisatiekost" om deze geloopte vorm aan te nemen, en drukbezette aminozuren dicht bij het aansluitpunt kunnen de reactie fysiek blokkeren. Chemici bouwen peptiden vaak op kleine bolletjes vast materiaal, wat de zuivering vereenvoudigt maar de vrijheid van vouwen verder kan beperken. Als gevolg daarvan hangt het slagen of falen van ringvorming vaak gevoelig af van waar, langs een anderszins vergelijkbare sequentie, de chemicus besluit de lus te sluiten. Tot nu toe werd die keuze grotendeels geleid door ervaring en trial‑and‑error.
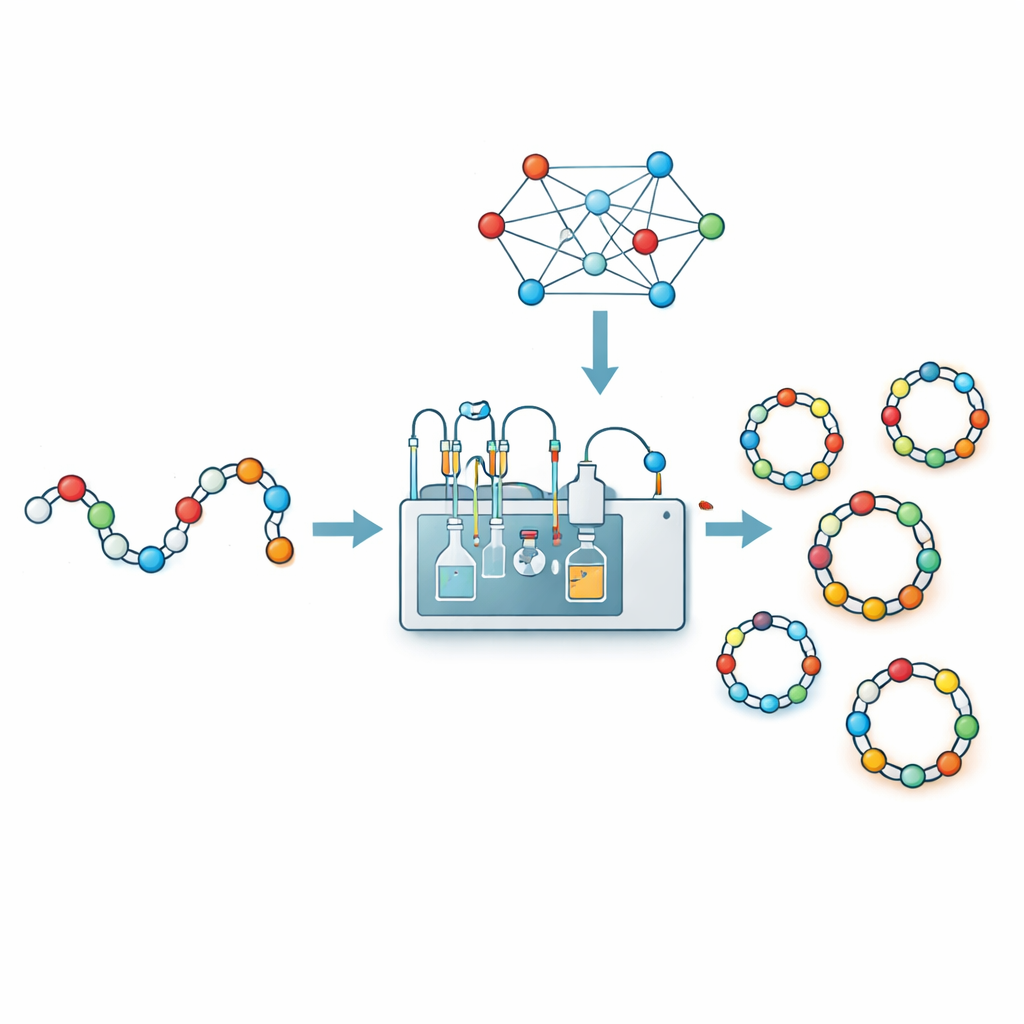
Robots en algoritmen bouwen een leerbibliotheek
Om giswerk te vervangen door data combineerden de onderzoekers geautomatiseerde chemie met machine learning. Met een robotisch flow‑synthesesysteem genaamd CycloBot en een speciale linker die sluiting van de ring direct op de vaste drager mogelijk maakt, maakten en testten ze snel 306 verschillende peptideketens variërend van 2 tot 14 aminozuren. Voor elke sequentie noteerden ze eenvoudig of een zuiver cyclisch product werd gedetecteerd of niet. Vervolgens vertaalden ze elke sequentie in een rijke numerieke omschrijving: welke aminozuren het bevat, hoe ze in paren geordend zijn, een positie‑voor‑positie code, en een handvol zorgvuldig gekozen vlaggen op basis van labervaring (bijvoorbeeld dat bepaalde aminozuren aan een uiteinde de ringvorming hebben geholpen of belemmerd). Door deze 414‑dimensionale vingerafdrukken aan verschillende typen machine‑learningmodellen te voeren, vonden ze dat een support vector classifier de beste prestaties gaf, en ongeveer 84 procent correct cyclisatie‑succes of ‑falen voorspelde in kruisvalidatietests.
Voorspellingen aan de experimentele toets onderwerpen
Het team stelde hun model vervolgens op de proef met nieuwe peptiden die het nog nooit had gezien. Ze ontwierpen acht kunstmatige sequenties en vier natuurlijk geïnspireerde therapeutische kandidaten, en probeerden voor elk alle mogelijke plaatsen om de ring langs de keten te sluiten. In totaal voerden ze 74 cyclisatie‑experimenten uit. De voorspellingen van het machine‑learningmodel kwamen overeen met de labresultaten in 64 van deze gevallen, een nauwkeurigheid van 86 procent. Belangrijk is dat het model zowel veelbelovende als ongunstige locaties goed kon signaleren, wat betekent dat het chemici kan helpen vermijden dat ze tijd verspillen aan onwillige sequenties en tegelijkertijd de meest waarschijnlijke kanshebbers aanwijst.
Een praktisch hulpmiddel voor geneesmiddelontwerpers
Om hun aanpak nuttig te maken buiten hun eigen lab verpakten de auteurs het getrainde model in een openbaar platform genaamd CycloPepper, beschikbaar als zowel downloadbare software als een webtool. Gebruikers kunnen één peptide invoeren of er veel tegelijk uploaden, en binnen enkele seconden een kaart ontvangen van welke kop‑naar‑staart sluitingsplaatsen waarschijnlijk werken. Het team toonde de waarde aan door honderden potentiële cyclische peptiden te ontwerpen gericht op eiwitdoelen die betrokken zijn bij kanker en immuunziekten, en liet zien dat het hulpmiddel snel bijna 40 procent van sequenties kan filteren die waarschijnlijk niet cycliseren. Voor niet‑specialisten is de kern dat CycloPepper fungeert als een slimme pre‑screeningassistent en een enorme ontwerp ruimte terugbrengt tot een praktische set kandidaten. Door geautomatiseerde synthese te combineren met voorspellende algoritmen brengt dit werk de belofte van snellere, meer rationele ontdekking van ringvormige peptiden als geneesmiddelen een stap dichterbij de realiteit.
Bronvermelding: Pan, Y., Hu, C., Li, J. et al. CycloPepper: a machine learning platform for predicting cyclization outcomes and optimizing synthesis of therapeutic cyclopeptides. Nat Commun 17, 2803 (2026). https://doi.org/10.1038/s41467-026-69441-w
Trefwoorden: cyclische peptiden, ontwerp van peptiden als geneesmiddelen, machine learning in chemie, geautomatiseerde synthese, cyclisatievoorspelling