Clear Sky Science · de
CycloPepper: eine Machine‑Learning‑Plattform zur Vorhersage von Cyclisierungs‑Ergebnissen und zur Optimierung der Synthese therapeutischer Cyclopeptide
Knickende Ketten in kraftvolle Ringe verwandeln
Krebsmedikamente, Antibiotika und andere moderne Wirkstoffe werden zunehmend aus kurzen Aminosäureketten hergestellt, die Peptide genannt werden. Wenn diese Ketten zu geschlossenen Ringen vernäht werden — also zu zyklischen Peptiden — werden sie oft robuster, haltbarer und besser darin, in Zellen einzudringen. Das Herstellen dieser winzigen Ringe im Labor ist jedoch überraschend heikel, und Chemiker können Wochen damit verschwenden, herauszufinden, wie eine Kette am besten geschlossen wird. Diese Studie stellt CycloPepper vor, eine von Machine Learning getriebene Plattform, die Forschenden in Sekunden hilft vorherzusagen, welche Peptidketten wahrscheinlich stabile Ringe bilden und welche scheitern werden — und so die Suche nach neuen Peptidwirkstoffen potenziell beschleunigt.
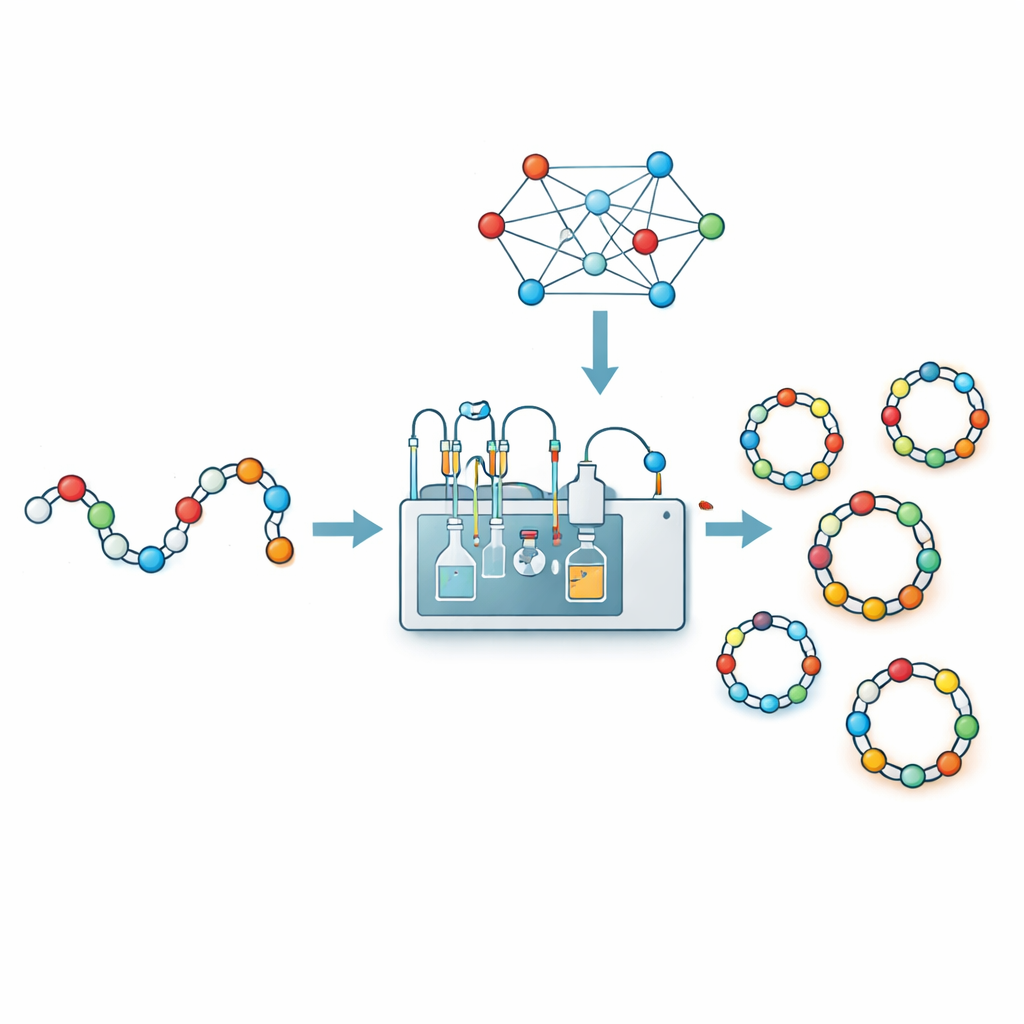
Warum ringförmige Peptide wichtig sind
Peptide sind Ketten von Aminosäuren, denselben Bausteinen, aus denen Proteine bestehen. Als offene Ketten können sie schwach und leicht von Körperenzymen abgebaut werden. Wenn die beiden Enden der Kette Kopf‑zu‑Schwanz verbunden werden, wird das Molekül kompakter und starrer. Dies verbessert häufig die Bindungsstärke an ein biologisches Ziel, die Resistenz gegenüber Verdauungsenzymen und die Fähigkeit, Zellmembranen zu passieren. Mehrere wichtige Medikamente, darunter potente Antibiotika, basieren auf solchen zyklischen Strukturen. Für Wirkstoffdesigner ist die Umwandlung eines linearen Peptids in einen Ring eine Schlüsselstrategie, um ein schwaches, empfindliches Molekül in ein wirksames und langlebiges Medikament zu verwandeln.
Die verborgene Schwierigkeit beim Schließen des Rings
Trotz ihrer Vorzüge sind zyklische Peptide schwer herzustellen. Um einen Ring zu bilden, muss sich eine flexible Kette genau in die richtige Gestalt falten, damit ihre beiden Enden miteinander reagieren, statt mit Nachbarmolekülen. Besonders kurze Ketten zahlen eine hohe „Organisationskosten“, um diese geschlossene Form anzunehmen, und dichte Aminosäuren in der Nähe der Verknüpfungsstelle können die Reaktion physisch blockieren. Chemiker bauen Peptide meist auf winzigen festen Kügelchen auf, was die Reinigung erleichtert, aber die Faltungsfreiheit zusätzlich einschränken kann. Daher hängt der Erfolg oder Misserfolg der Ringbildung oft empfindlich davon ab, an welcher Stelle einer ansonsten ähnlichen Sequenz der Chemiker den Ring schließt. Bislang wurde diese Entscheidung weitgehend durch Erfahrung und Versuch und Irrtum geleitet.
Roboter und Algorithmen bauen eine Lernbibliothek
Um das Raten durch Daten zu ersetzen, kombinierten die Forschenden automatisierte Chemie mit Machine Learning. Mithilfe eines robotischen Flow‑Synthese‑Systems namens CycloBot und eines speziellen Linkers, der das Schließen des Rings direkt auf der festen Trägersubstanz erlaubt, stellten sie schnell 306 verschiedene Peptidketten mit Längen von 2 bis 14 Aminosäuren her und testeten sie. Für jede Sequenz protokollierten sie einfach, ob ein sauberer cyclischer Produktnachweis vorlag oder nicht. Anschließend übersetzten sie jede Sequenz in eine reichhaltige numerische Beschreibung: welche Aminosäuren sie enthält, wie diese paarweise angeordnet sind, ein positionsspezifischer Code und eine Handvoll erfahrungsbasierter Flags (zum Beispiel, dass bestimmte Aminosäuren an den Enden das Cyclisieren fördern oder behindern). Diese 414‑dimensionalen Fingerprints fütterten sie in mehrere Typen von Machine‑Learning‑Modellen; ein Support‑Vector‑Classifier erzielte die beste Leistung und sagte in Kreuzvalidierungstests die Cyclisierungswahrscheinlichkeit korrekt in etwa 84 Prozent der Fälle voraus.
Vorhersagen im experimentellen Test
Das Team stellte das Modell anschließend vor neue Peptide, die es noch nie gesehen hatte. Sie entwarfen acht künstliche Sequenzen und vier natürlich inspirierte therapeutische Kandidaten und versuchten bei jedem alle möglichen Stellen entlang der Kette, den Ring zu schließen. Insgesamt führten sie 74 Cyclisierungs‑Experimente durch. Die Vorhersagen des Machine‑Learning‑Modells stimmten in 64 dieser Fälle mit den Laborergebnissen überein, was einer Genauigkeit von 86 Prozent entspricht. Wichtig war, dass das Modell sowohl vielversprechende als auch ungeeignete Stellen gut kennzeichnete — es konnte Chemikern helfen, Zeitverschwendung an widerspenstigen Sequenzen zu vermeiden und zugleich die erfolgversprechendsten Kandidaten hervorheben.
Ein praktisches Werkzeug für Wirkstoffdesigner
Um ihren Ansatz über das eigene Labor hinaus nützlich zu machen, packten die Autoren das trainierte Modell in eine öffentliche Plattform namens CycloPepper, verfügbar sowohl als herunterladbare Software als auch als Web‑Tool. Nutzer können ein einzelnes Peptid eingeben oder viele gleichzeitig hochladen und erhalten innerhalb von Sekunden eine Karte, welche Kopf‑zu‑Schwanz‑Verschlussstellen wahrscheinlich funktionieren. Das Team demonstrierte den Nutzen, indem es Hunderte potenzieller zyklischer Peptide gegen Proteinziele entwarf, die an Krebs und Immunerkrankungen beteiligt sind, und zeigte, dass das Tool schnell fast 40 Prozent der Sequenzen herausfiltern kann, die wahrscheinlich nicht cyclisieren. Für Nichtfachleute lautet die Botschaft: CycloPepper wirkt wie ein intelligenter Vorsortierer, der einen riesigen Designraum auf eine praktische Menge von Kandidaten reduziert. Durch die Kombination automatisierter Synthese mit vorhersagenden Algorithmen rückt diese Arbeit die Aussicht auf schnellere, rationalere Entdeckung ringförmiger Peptidwirkstoffe näher an die Realität.
Zitation: Pan, Y., Hu, C., Li, J. et al. CycloPepper: a machine learning platform for predicting cyclization outcomes and optimizing synthesis of therapeutic cyclopeptides. Nat Commun 17, 2803 (2026). https://doi.org/10.1038/s41467-026-69441-w
Schlüsselwörter: zyklische Peptide, Peptid‑Wirkstoffdesign, Machine Learning in der Chemie, automatisierte Synthese, Cyclisierungs‑Vorhersage