Clear Sky Science · sv
CycloPepper: en maskininlärningsplattform för att förutsäga cykliseringsutfall och optimera syntes av terapeutiska cykliska peptider
Att förvandla flexibla kedjor till kraftfulla ringar
Cancermedel, antibiotika och andra moderna läkemedel byggs i allt större utsträckning av korta kedjor av aminosyror som kallas peptider. När dessa kedjor sys ihop till slutna ringar, eller cykliska peptider, blir de ofta tåligare, mer långlivade och bättre på att ta sig in i celler. Men att framställa dessa små ringar i labbet är förvånansvärt pilligt, och kemister kan slösa veckor på att gissa vilket sätt som är bäst för att stänga en kedja. Denna studie presenterar CycloPepper, en maskininlärningsdriven plattform som hjälper forskare att på sekunder förutsäga vilka peptidkedjor som sannolikt bildar stabila ringar och vilka som misslyckas, vilket potentiellt snabbar upp sökandet efter nya peptidläkemedel.
Varför ringformade peptider spelar roll
Peptider är strängar av aminosyror, samma byggstenar som utgör proteiner. När de lämnas som öppna kedjor kan de vara sladdriga och lätta för kroppens enzymer att bryta ner. Om kedjans två ändar fogas ihop huvud‑till‑svans för att bilda en ring blir molekylen mer kompakt och styv. Detta förbättrar ofta hur starkt den binder till sitt biologiska mål, hur väl den överlever matsmältningsenzymer och hur lätt den tar sig igenom cellmembran. Flera viktiga läkemedel, inklusive kraftfulla antibiotika, bygger på sådana cykliska strukturer. För läkemedelsdesigners är det en nyckelstrategi att göra en linjär peptid till en ring för att förvandla en svag, ömtålig molekyl till ett potent och hållbart läkemedel.
Den dolda svårigheten i att stänga ringen
Trots sin attraktionskraft är cykliska peptider svåra att framställa. För att bilda en ring måste en flexibel kedja vika sig till precis rätt form så att dess två ändar kan reagera med varandra istället för med en granne. Särskilt korta kedjor betalar en brant ”organisationskostnad” för att anta denna loopade form, och trånga aminosyror nära fogpunkten kan fysiskt blockera reaktionen. Kemister bygger vanligtvis peptider på små pärlor av fast material, vilket underlättar rening men kan begränsa hur fritt kedjan kan vika sig. Följaktligen beror framgång eller misslyckande vid ringbildning ofta känsligt på var längs en annars likartad sekvens kemisten väljer att stänga loopen. Hittills har detta val till stor del styrts av erfarenhet och trial‑and‑error.
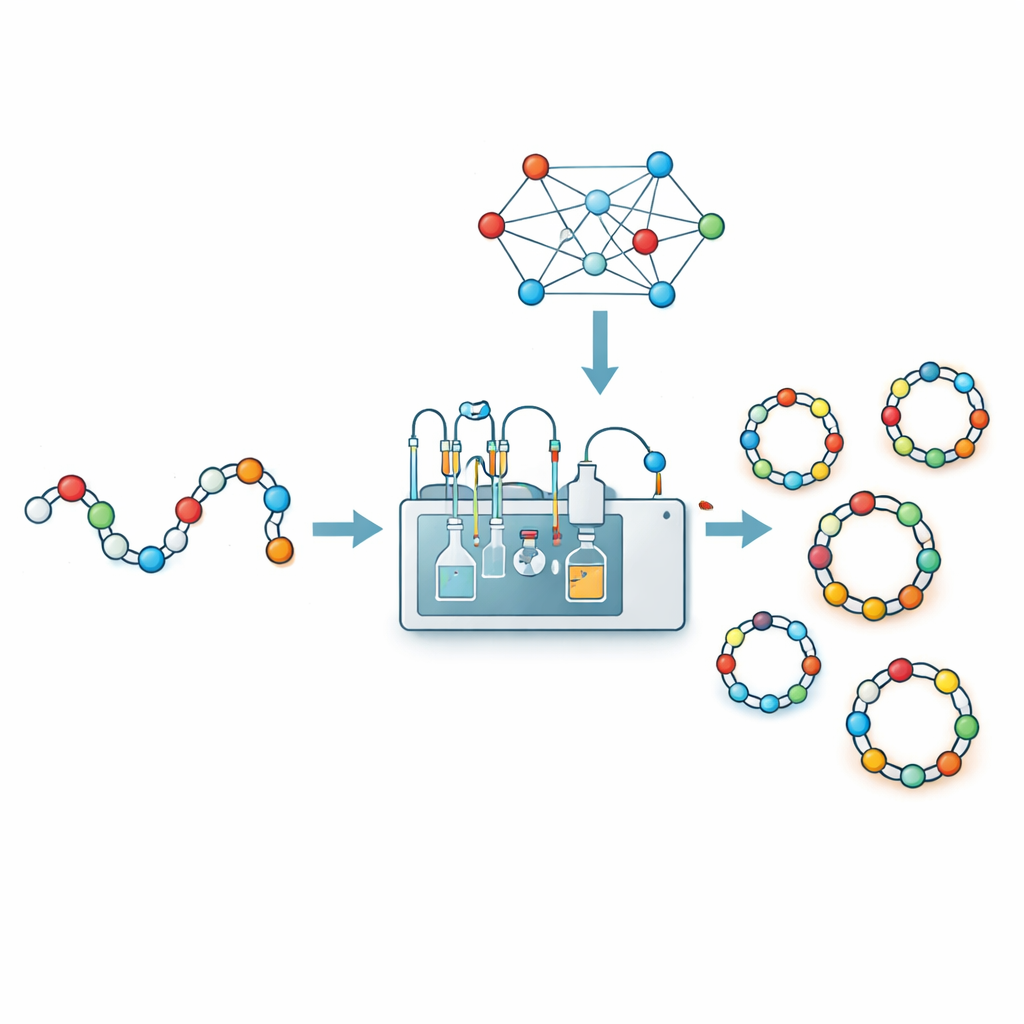
Robotar och algoritmer bygger ett lärande bibliotek
För att ersätta gissningar med data kombinerade forskarna automatiserad kemi med maskininlärning. Med hjälp av ett robotiserat flödessynthessystem kallat CycloBot och en speciell länkare som tillåter ringstängning direkt på det fasta stödet framställde och testade de snabbt 306 olika peptidkedjor med längder från 2 till 14 aminosyror. För varje sekvens noterade de enkelt om en ren cyklisk produkt upptäcktes eller inte. De översatte sedan varje sekvens till en rik numerisk beskrivning: vilka aminosyror den innehåller, hur de är ordnade i par, en positions‑för‑positions‑kod och ett fåtal handplockade flaggor baserade på laboratorieerfarenhet (till exempel att vissa aminosyror i ändarna tenderar att hjälpa eller hindra ringbildning). Genom att mata dessa 414‑dimensionella fingeravtryck in i flera typer av maskininlärningsmodeller fann de att en stödvektor‑klassificerare gav bäst prestanda och korrekt förutsade cykliseringsframgång eller misslyckande i cirka 84 procent av fallen i korsvalideringstester.
Sätta förutsägelserna på experimentellt prov
Teamet utmanade sedan sin modell med nya peptider den aldrig tidigare sett. De designade åtta artificiella sekvenser och fyra naturligt inspirerade terapeutiska kandidater, och för var och en försökte de alla möjliga platser för att stänga ringen längs kedjan. Totalt genomförde de 74 cykliseringsförsök. Maskininlärningsmodellens förutsägelser stämde överens med labbresultaten i 64 av dessa fall, vilket motsvarar en noggrannhet på 86 procent. Viktigt var att modellen var bra på att flagga både lovande och dåliga ställen, vilket innebär att den kan hjälpa kemister att undvika att slösa tid på ovilliga sekvenser samtidigt som den framhäver de mest sannolika vinnarna.
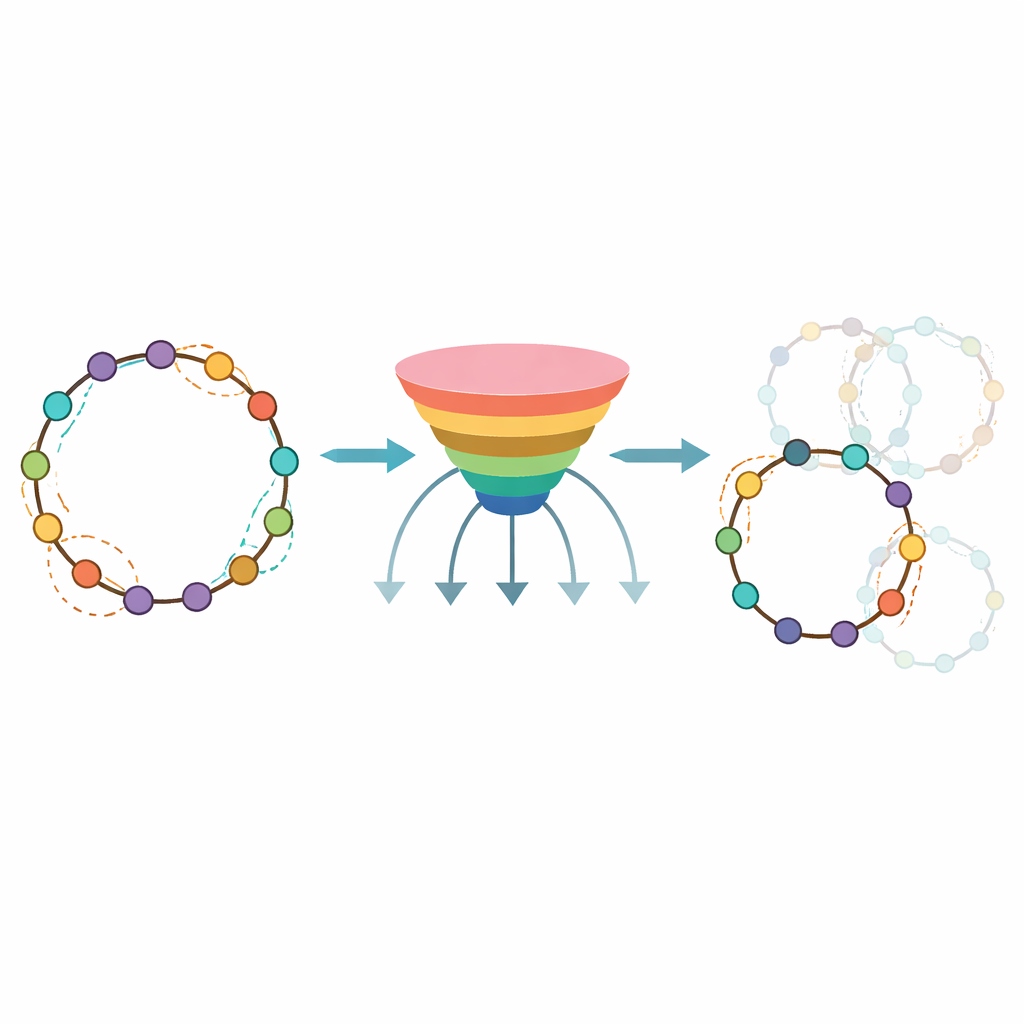
Ett praktiskt verktyg för läkemedelsdesigners
För att göra sin metod användbar utanför det egna laboratoriet paketerade författarna den tränade modellen i en publik plattform kallad CycloPepper, tillgänglig både som nedladdningsbar programvara och som ett webbverktyg. Användare kan skriva in en enskild peptid eller ladda upp många på en gång, och inom sekunder få en karta över vilka huvud‑till‑svans‑stängningsställen som sannolikt fungerar. Gruppen demonstrerade dess värde genom att designa hundratals potentiella cykliska peptider riktade mot proteiner involverade i cancer och immunsjukdomar, och visade att verktyget snabbt kan filtrera bort nästan 40 procent av sekvenser som sannolikt inte cykliserar. För icke‑specialister är slutsatsen att CycloPepper fungerar som en smart förhandsgranskningsassistent som krymper ett enormt designutrymme till en praktisk uppsättning kandidater. Genom att kombinera automatiserad syntes med prediktiva algoritmer för denna typ av arbete för det snabbare, mer rationella upptäckandet av ringformade peptidläkemedel ett steg närmare verkligheten.
Citering: Pan, Y., Hu, C., Li, J. et al. CycloPepper: a machine learning platform for predicting cyclization outcomes and optimizing synthesis of therapeutic cyclopeptides. Nat Commun 17, 2803 (2026). https://doi.org/10.1038/s41467-026-69441-w
Nyckelord: cykliska peptider, peptiddesign för läkemedel, maskininlärning i kemi, automatiserad syntes, cykliseringsprediktion