Clear Sky Science · pl
CycloPepper: platforma uczenia maszynowego do przewidywania wyników cyklizacji i optymalizacji syntezy terapeutycznych cyklopeptydów
Przekształcanie giętkich łańcuchów w potężne pierścienie
Leki przeciwnowotworowe, antybiotyki i inne nowoczesne terapie coraz częściej opierają się na krótkich łańcuchach aminokwasów zwanych peptydami. Gdy te łańcuchy zostaną zszyte w zamknięte pierścienie, czyli peptydy cykliczne, często stają się twardsze, trwalsze i lepiej przenikają do komórek. Jednak wytwarzanie tych drobnych pierścieni w laboratorium bywa zaskakująco kapryśne, a chemicy mogą tracić tygodnie na zgadywaniu, w jaki sposób zamknąć łańcuch. Niniejsze badanie przedstawia CycloPepper — platformę napędzaną uczeniem maszynowym, która pomaga badaczom przewidzieć w ciągu sekund, które łańcuchy peptydowe prawdopodobnie utworzą stabilne pierścienie, a które zawiodą, co może przyspieszyć poszukiwanie nowych peptydowych leków.
Dlaczego peptydy pierścieniowe są ważne
Peptydy to łańcuchy aminokwasów — tych samych cegiełek budujących białka. Jako otwarte łańcuchy mogą być wiotkie i łatwe do rozkładu przez enzymy w organizmie. Jeśli połączy się dwa końce łańcucha „głowa‑ogon”, aby utworzyć pierścień, cząsteczka staje się bardziej zwarta i sztywna. Często poprawia to siłę wiązania z biologicznym celem, odporność na enzymy trawienne i zdolność przenikania przez błony komórkowe. Kilka ważnych leków, w tym silne antybiotyki, opiera się na takich strukturach cyklicznych. Dla projektantów leków przekształcenie liniowego peptydu w pierścień to kluczowa strategia, by słabą, nietrwałą cząsteczkę zamienić w silny i trwały lek.
Ukryta trudność zamykania pierścienia
Mimo atrakcyjności peptydy cykliczne są trudne do otrzymania. Aby powstał pierścień, giętki łańcuch musi zwinąć się w odpowiedni kształt, tak aby jego dwa końce zareagowały ze sobą, a nie z sąsiadem. Krótkie łańcuchy ponoszą szczególnie wysoką „cenę organizacyjną”, by przyjąć tę zapętloną konformację, a zatłoczone aminokwasy w pobliżu miejsca łączenia mogą fizycznie blokować reakcję. Chemicy zwykle budują peptydy na maleńkich ziarnach stałego nośnika, co ułatwia oczyszczanie, ale może dodatkowo ograniczać swobodę składania łańcucha. W efekcie powodzenie lub niepowodzenie utworzenia pierścienia często zależy wrażliwie od tego, w którym miejscu — wzdłuż podobnej sekwencji — chemik decyduje się zamknąć pętlę. Do tej pory wybór ten bazował głównie na doświadczeniu i metodzie prób i błędów.
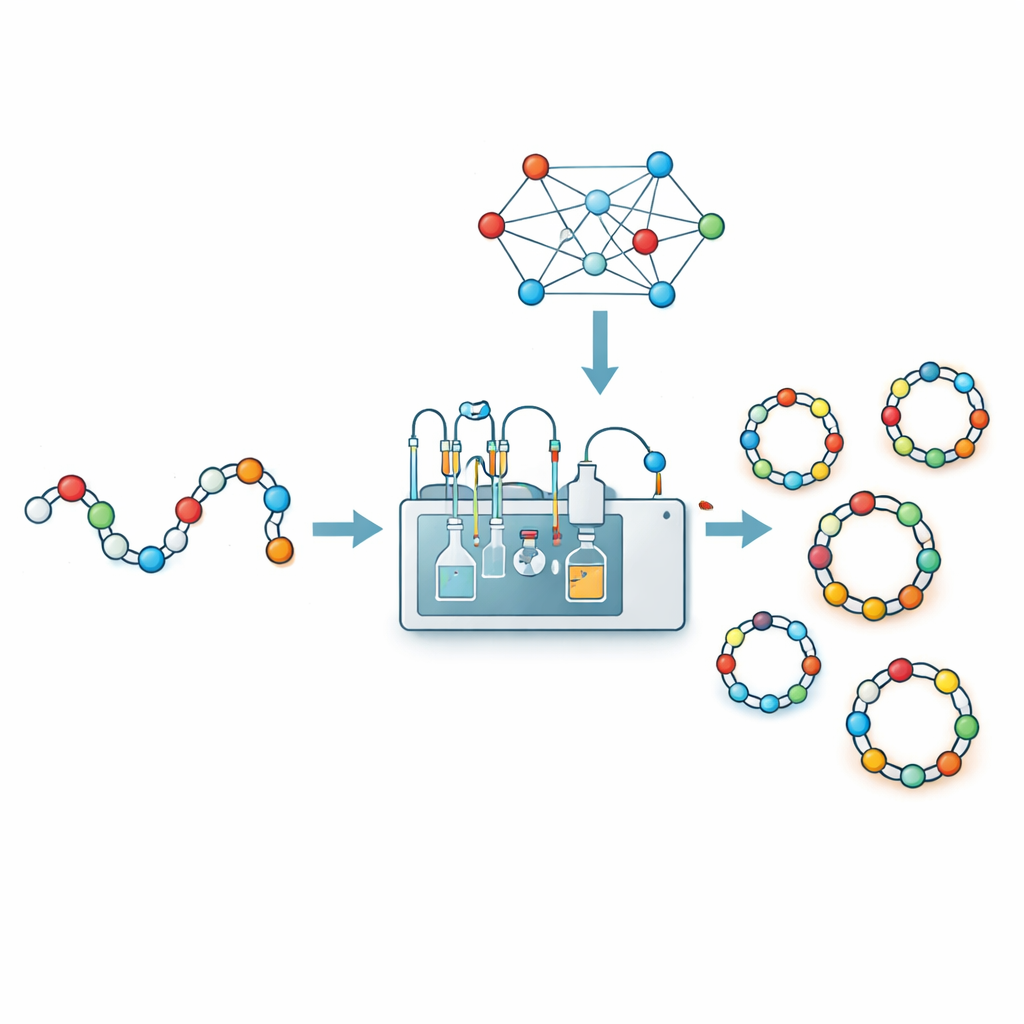
Roboty i algorytmy budują bibliotekę wiedzy
Aby zastąpić zgadywanie danymi, autorzy połączyli chemię automatyczną z uczeniem maszynowym. Korzystając z robotycznego systemu syntezy przepływowej nazwanego CycloBot oraz specjalnego łącznika umożliwiającego zamknięcie pierścienia bezpośrednio na nośniku stałym, szybko wytworzyli i przetestowali 306 różnych łańcuchów peptydowych o długościach od 2 do 14 aminokwasów. Dla każdej sekwencji rejestrowali po prostu, czy wykryto czysty produkt cykliczny, czy nie. Następnie przetłumaczyli każdą sekwencję na bogaty opis numeryczny: jakie aminokwasy zawiera, jak są uporządkowane w parach, kod pozycji po pozycji oraz kilka ręcznie wybranych wskaźników opartych na doświadczeniu laboratoryjnym (na przykład że niektóre aminokwasy na końcach mają tendencję do ułatwiania lub utrudniania tworzenia pierścienia). Podając te 414‑wymiarowe odciski palców do kilku rodzajów modeli uczenia maszynowego, odkryli, że klasyfikator wektorów nośnych (SVC) dał najlepsze wyniki, poprawnie przewidując powodzenie lub porażkę cyklizacji w około 84 procentach przypadków w testach krzyżowej walidacji.
Weryfikacja przewidywań w eksperymencie
Zespół następnie wystawił model na próbę z nowymi peptydami, których nigdy wcześniej nie widział. Zaprojektowali osiem sztucznych sekwencji i cztery inspirowane naturalnie kandydatury terapeutyczne, i dla każdej próbowali wszystkich możliwych miejsc zamknięcia pierścienia wzdłuż łańcucha. W sumie przeprowadzili 74 eksperymenty cyklizacji. Przewidywania modelu uczenia maszynowego zgadzały się z wynikami laboratoryjnymi w 64 przypadkach, co daje dokładność 86 procent. Co ważne, model dobrze sygnalizował zarówno obiecujące, jak i nieopłacalne miejsca, co oznacza, że może pomóc chemikom unikać marnowania wysiłku na niechętne sekwencje, a także wskazać najbardziej prawdopodobne zwycięzcy.
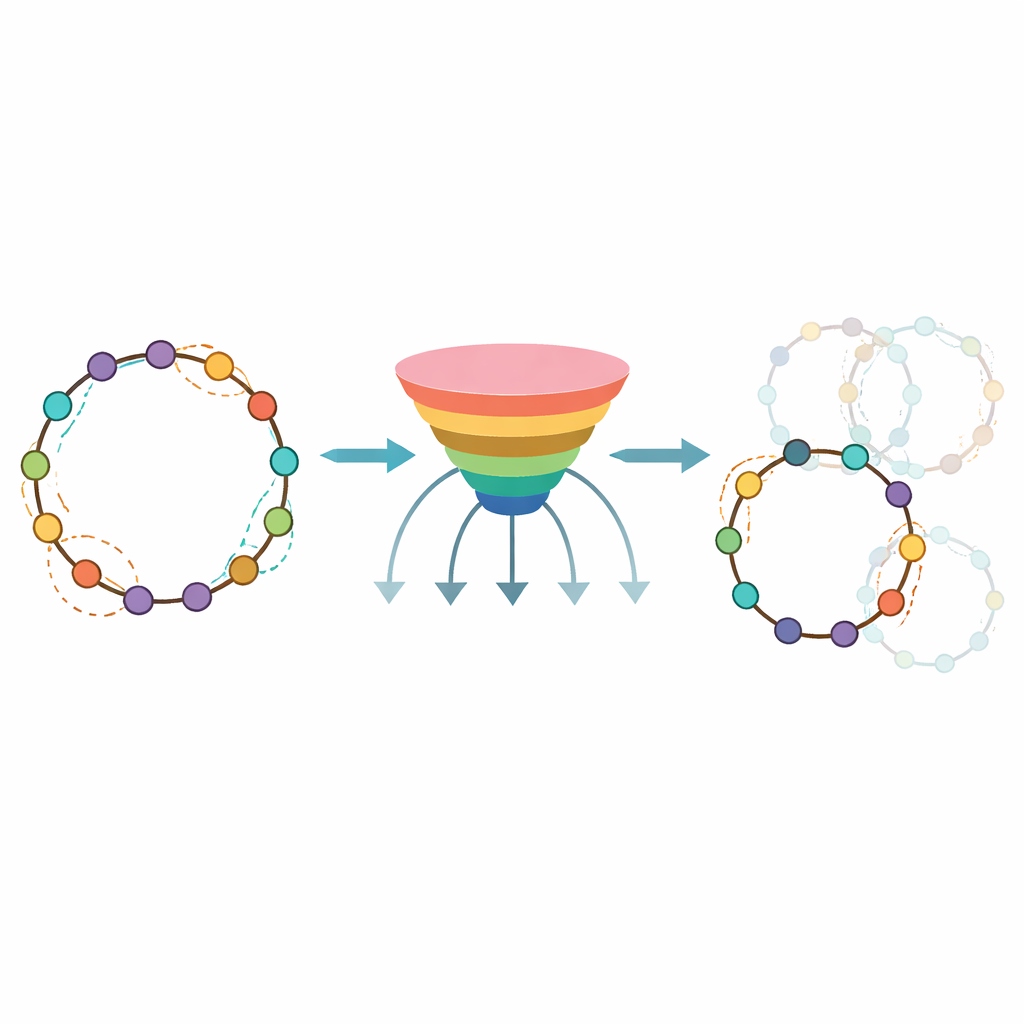
Praktyczne narzędzie dla projektantów leków
Aby uczynić swoje podejście użytecznym poza własnym laboratorium, autorzy opakowali wytrenowany model w publiczną platformę nazwaną CycloPepper, dostępną jako oprogramowanie do pobrania i narzędzie internetowe. Użytkownicy mogą wpisać pojedynczy peptyd lub przesłać wiele naraz i w ciągu sekund otrzymać mapę miejsc zamknięcia głowa‑ogon, które prawdopodobnie zadziałają. Zespół wykazał jej przydatność, projektując setki potencjalnych peptydów cyklicznych skierowanych przeciwko białkowym celom zaangażowanym w nowotwory i choroby autoimmunologiczne, pokazując, że narzędzie może szybko wyeliminować niemal 40 procent sekwencji mało prawdopodobnych do cyklizacji. Dla osób spoza specjalności kluczowe przesłanie jest takie, że CycloPepper działa jak inteligentny asystent preselekcji, zmniejszając ogromną przestrzeń projektową do praktycznego zestawu kandydatów. Łącząc automatyczną syntezę z predykcyjnymi algorytmami, praca ta przybliża obietnicę szybszego, bardziej racjonalnego odkrywania pierścieniowych leków peptydowych do rzeczywistości.
Cytowanie: Pan, Y., Hu, C., Li, J. et al. CycloPepper: a machine learning platform for predicting cyclization outcomes and optimizing synthesis of therapeutic cyclopeptides. Nat Commun 17, 2803 (2026). https://doi.org/10.1038/s41467-026-69441-w
Słowa kluczowe: peptydy cykliczne, projektowanie leków peptydowych, uczenie maszynowe w chemii, automatyczna synteza, predykcja cyklizacji