Clear Sky Science · es
CycloPepper: una plataforma de aprendizaje automático para predecir resultados de ciclización y optimizar la síntesis de ciclopeptidos terapéuticos
Convertir cadenas flexibles en anillos poderosos
Los fármacos contra el cáncer, los antibióticos y otras medicinas modernas se construyen cada vez más a partir de cadenas cortas de aminoácidos llamadas péptidos. Cuando estas cadenas se cosen para formar anillos cerrados, o péptidos cíclicos, con frecuencia se vuelven más resistentes, duran más y atraviesan mejor las células. Pero fabricar estos pequeños anillos en el laboratorio resulta sorprendentemente delicado, y los químicos pueden perder semanas adivinando la mejor forma de cerrar una cadena. Este estudio presenta CycloPepper, una plataforma impulsada por aprendizaje automático que ayuda a los investigadores a predecir, en cuestión de segundos, qué cadenas peptídicas probablemente formarán anillos estables y cuáles fracasarán, acelerando potencialmente la búsqueda de nuevos fármacos peptídicos.
Por qué importan los péptidos en forma de anillo
Los péptidos son cadenas de aminoácidos, los mismos bloques constructores que componen las proteínas. Cuando se mantienen como cadenas abiertas, pueden ser flexibles y fáciles de degradar por las enzimas del organismo. Si se unen las dos extremos de la cadena de cabeza a cola para formar un anillo, la molécula se vuelve más compacta y rígida. Esto suele mejorar cuán fuertemente se une a su diana biológica, cuánto resiste a las enzimas digestivas y con qué facilidad atraviesa las membranas celulares. Varios fármacos importantes, incluidos antibióticos potentes, se basan en estas estructuras cíclicas. Para los diseñadores de fármacos, convertir un péptido lineal en un anillo es una estrategia clave para transformar una molécula débil y frágil en un medicamento potente y durable.
La dificultad oculta al cerrar el anillo
A pesar de su atractivo, los péptidos cíclicos son difíciles de fabricar. Para formar un anillo, una cadena flexible debe plegarse en la forma adecuada para que sus dos extremos reaccionen entre sí en lugar de con una molécula vecina. Las cadenas cortas, en particular, pagan un alto “coste organizativo” para adoptar esta conformación en bucle, y aminoácidos voluminosos cerca del punto de unión pueden bloquear físicamente la reacción. Los químicos suelen sintetizar péptidos sobre pequeñas perlas de material sólido, lo que facilita la purificación pero puede restringir aún más la libertad de plegamiento de la cadena. Como resultado, el éxito o fracaso de la formación del anillo suele depender de forma muy sensible de dónde, a lo largo de una secuencia por lo demás similar, el químico decide cerrar el bucle. Hasta ahora, esta elección se ha guiado en gran medida por la experiencia y la prueba y error.
Robots y algoritmos construyen una biblioteca de aprendizaje
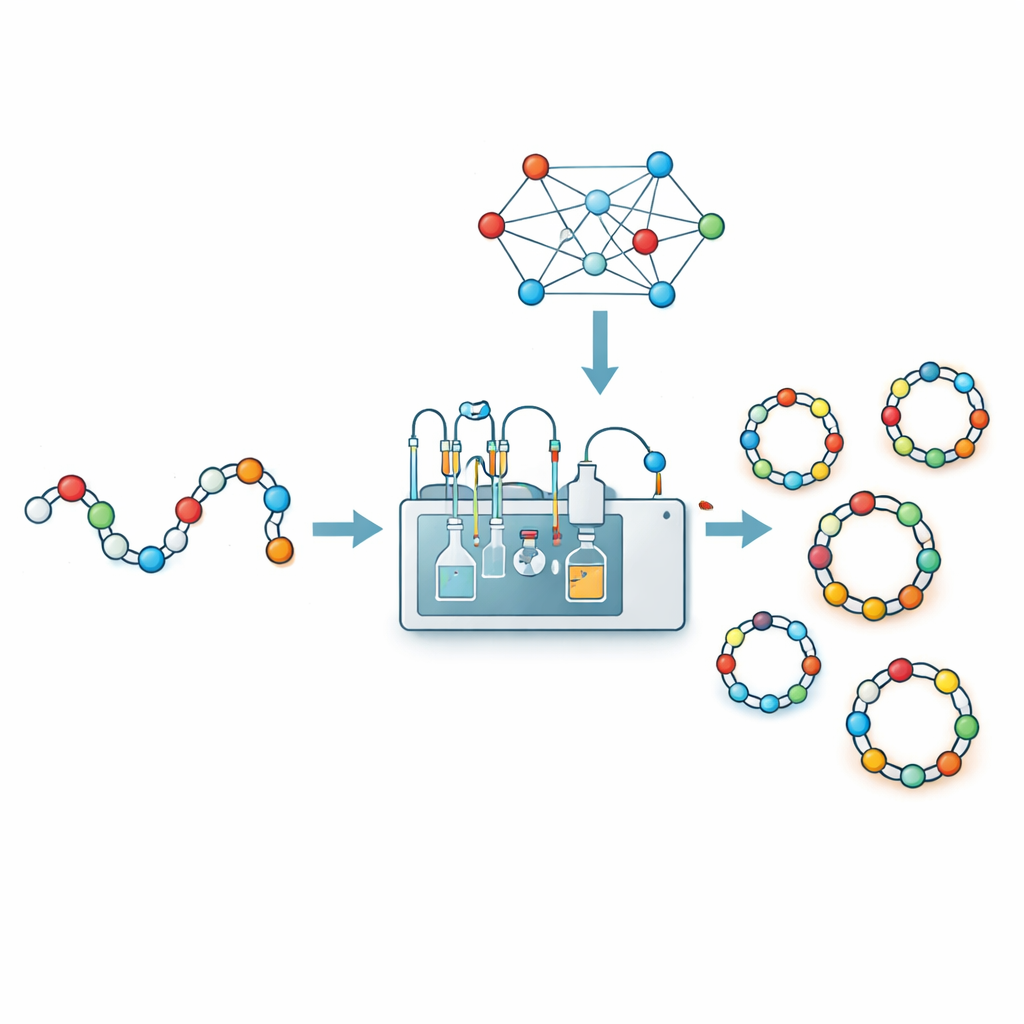
Para sustituir con datos la conjetura, los investigadores combinaron química automatizada con aprendizaje automático. Usando un sistema robótico de síntesis en flujo llamado CycloBot y un enlaçador especial que permite que la ciclización ocurra directamente sobre el soporte sólido, fabricaron y probaron rápidamente 306 cadenas peptídicas diferentes que iban de 2 a 14 aminoácidos. Para cada secuencia, registraron simplemente si se detectó o no un producto cíclico limpio. Luego tradujeron cada secuencia a una descripción numérica rica: qué aminoácidos contiene, cómo están ordenados por pares, un código posición por posición y un puñado de indicadores seleccionados manualmente basados en la experiencia de laboratorio (por ejemplo, que ciertos aminoácidos en cualquiera de los extremos tienden a ayudar o dificultar la ciclización). Al alimentar estas huellas de 414 dimensiones en varios tipos de modelos de aprendizaje automático, encontraron que un clasificador de vectores de soporte ofrecía el mejor rendimiento, prediciendo correctamente el éxito o el fracaso de la ciclización en aproximadamente el 84 por ciento de los casos en pruebas de validación cruzada.
Poner las predicciones a prueba experimental
El equipo después desafió a su modelo con péptidos nuevos que nunca había visto. Diseñaron ocho secuencias artificiales y cuatro candidatos terapéuticos inspirados en moléculas naturales, y para cada uno probaron todos los lugares posibles para cerrar el anillo a lo largo de la cadena. En total, realizaron 74 experimentos de ciclización. Las predicciones del modelo de aprendizaje automático coincidieron con los resultados de laboratorio en 64 de estos casos, una precisión del 86 por ciento. De forma importante, el modelo fue bueno tanto para señalar sitios prometedores como para identificar sitios pobres, lo que significa que puede ayudar a los químicos a evitar perder esfuerzos en secuencias poco cooperativas y, al mismo tiempo, resaltar las opciones con más probabilidades de éxito.
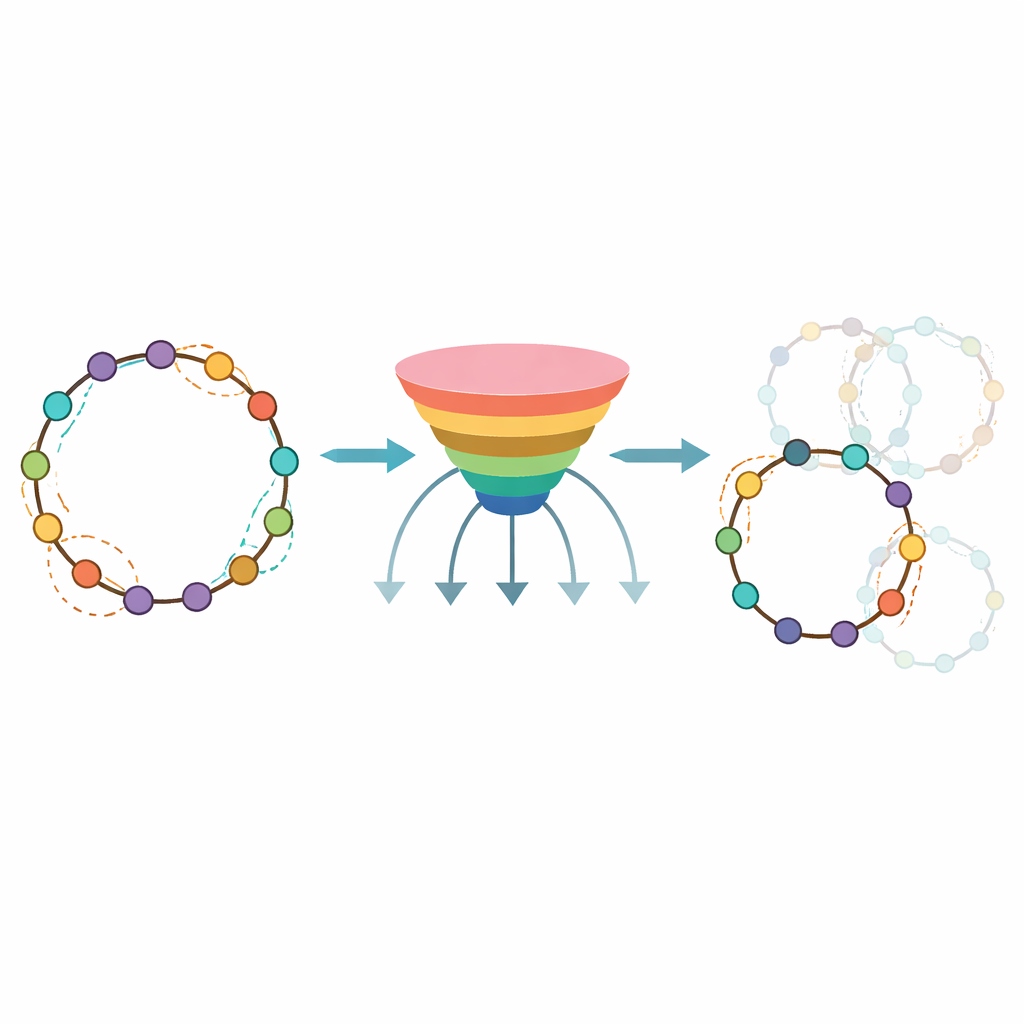
Una herramienta práctica para diseñadores de fármacos
Para que su enfoque fuera útil más allá de su propio laboratorio, los autores empaquetaron el modelo entrenado en una plataforma pública llamada CycloPepper, disponible tanto como software descargable como herramienta web. Los usuarios pueden introducir un péptido único o subir muchos a la vez y, en cuestión de segundos, recibir un mapa de qué sitios de cierre cabeza a cola probablemente funcionen. El equipo demostró su utilidad diseñando cientos de péptidos cíclicos potenciales dirigidos a proteínas implicadas en el cáncer y enfermedades inmunes, mostrando que la herramienta puede filtrar rápidamente casi el 40 por ciento de las secuencias que probablemente no se ciclicen. Para los no especialistas, la conclusión es que CycloPepper actúa como un asistente de preselección inteligente, reduciendo un vasto espacio de diseño a un conjunto práctico de candidatos. Al combinar síntesis automatizada con algoritmos predictivos, este trabajo acerca un paso más la promesa de un descubrimiento más rápido y racional de fármacos peptídicos en forma de anillo a la realidad.
Cita: Pan, Y., Hu, C., Li, J. et al. CycloPepper: a machine learning platform for predicting cyclization outcomes and optimizing synthesis of therapeutic cyclopeptides. Nat Commun 17, 2803 (2026). https://doi.org/10.1038/s41467-026-69441-w
Palabras clave: péptidos cíclicos, diseño de fármacos peptídicos, aprendizaje automático en química, síntesis automatizada, predicción de ciclización