Clear Sky Science · zh
塔利莫根肽拉赫帕雷疫苗(T‑VEC)与阿特珠单抗在新辅助化疗后HER2阴性乳腺癌中的应用:一项窗口期II期试验(SOLTI‑1503 PROMETEO)
为顽固乳腺肿瘤带来新希望
许多早期乳腺癌患者现在在手术前接受强强度化疗。对部分患者而言,肿瘤缩小到手术时无法检测到,长期预后极佳。但另一些患者仍残留可见的抗药性肿块,这些患者复发风险更高。PROMETEO研究在试验中检验了一种新方法:在残余癌组织中使用能杀伤癌细胞的病毒配合增强免疫的抗体,试图“唤醒”对抗癌症的免疫反应。
将病毒变成盟友
该试验针对的是肿瘤缺乏HER2蛋白的女性,这是乳腺癌中常见的一类,既包括激素受体阳性者也包括三阴性患者。所有参与者均已完成标准的新辅助化疗,但影像及活检仍显示肿块至少1厘米,提示肿瘤对药物有抗性。研究者使用塔利莫根肽拉赫帕雷(T‑VEC),一种改造过的疱疹病毒,能感染并毁灭癌细胞,同时释放吸引免疫细胞的信号。该病毒与阿特珠单抗联用,后者可阻断肿瘤用以关闭免疫攻击的PD‑L1“刹车”。治疗在化疗与手术之间的11周窗口期内进行。
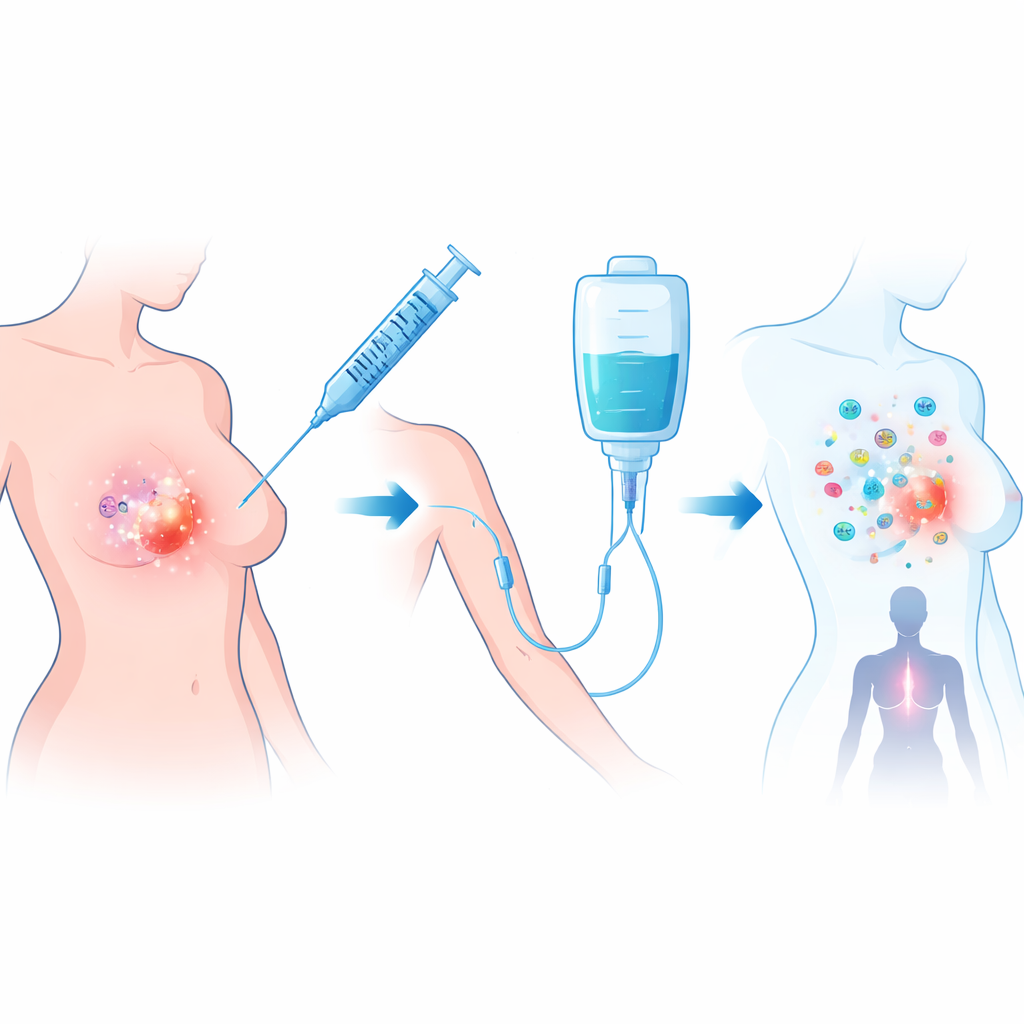
手术室里的发现
共有28名女性接受了治疗;大多数为激素受体阳性、HER2阴性的肿瘤,其余为三阴性病变。每位患者先在乳腺肿瘤处注射一次低剂量T‑VEC,随后进行四次更高剂量的注射并配合阿特珠单抗静脉输注。外科在随后切除肿瘤时,病理学家仔细评估残余癌组织的多少。在26例可评估的患者中,7例(约四分之一)在乳腺和淋巴结中均未见侵袭性癌,称为病理完全缓解(pCR)。这一结果达到了试验预设目标,值得注意的是这些肿瘤先前都已显示对化疗耐药。总体而言,治疗耐受性良好,主要为轻度副反应,如发热、关节疼痛及短暂的血液学检测异常;未见危及生命的严重反应或与治疗相关的死亡。
观察免疫系统的苏醒
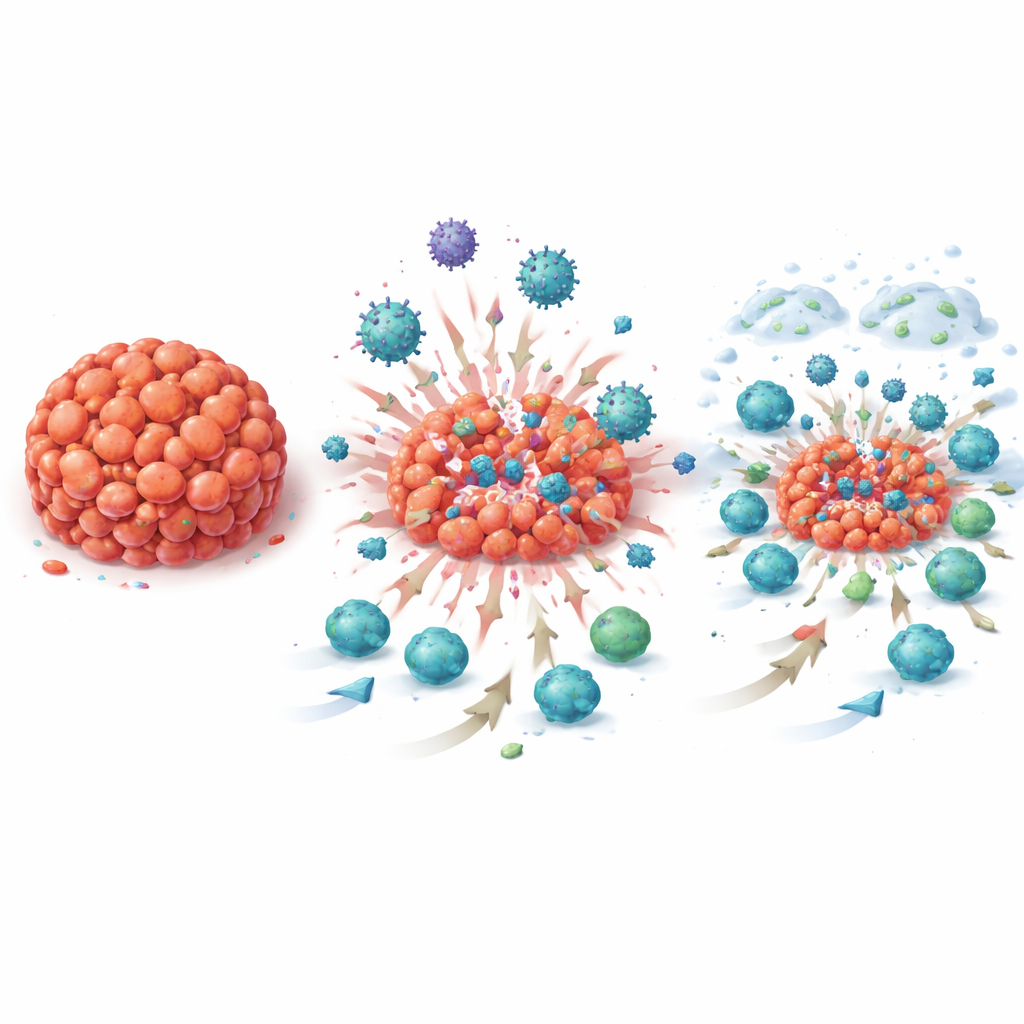
由于本研究属于“窗口期”试验,研究团队在治疗前、治疗中和术后采集了多次活检,难得地提供了肿瘤微环境随时间变化的动态视图。在显微镜下,研究者观察到随治疗进行,肿瘤浸润淋巴细胞数量增加——这些白细胞能够攻击癌细胞。类似微型淋巴结的结构(三级淋巴结构)变得更常见,且肿瘤更频繁地表达PD‑L1,也就是阿特珠单抗的靶点。对肿瘤样本的基因表达分析与这些显微观察一致:数百个与免疫相关的基因特征(包括B细胞、T细胞和抗体生成相关的特征)在单独使用T‑VEC后显著上调,联合治疗后再次升高,并在手术时仍维持在高位。这些变化不仅出现在肿瘤完全消失的患者中,也出现在有残余疾病的患者中,表明该策略在总体上重新激活了抗肿瘤免疫。
关于长期保护的初步迹象
研究者在术后对患者进行随访以观察癌症是否复发。中位随访近四年后,仅有四名女性出现远处转移,而这些患者术时均未达到肿瘤完全消失。相比之下,全部七例术中肿瘤被清除的患者均无复发。尽管样本量小且研究缺乏对照组,这一模式仍支持这样的观点:治疗后可见肿瘤的清除与更好的长期结局密切相关,即便在这一高风险人群中亦是如此。
这对患者可能意味着什么
PROMETEO试验表明,在化疗与手术之间短期加入一种溶瘤病毒加上免疫激活抗体对那些新辅助化疗后仍存活性肿瘤的HER2阴性乳腺癌女性是可行且看似安全的。这一方法在耐药肿瘤内诱发了强烈的免疫激活信号,并在一部分患者中出现了肿瘤完全消失的结果,尤其是在激素受体阳性患者中——在这类患者中此类反应通常罕见。尽管仍需更大规模的随机试验来确认该策略是否真正提高治愈率,但结果提示,在手术前将肿瘤转变为一种炎性、免疫富集的状态,可能为目前可选方案有限的患者提供一种降低复发风险的新途径。
引用: Pascual, T., Vidal, M., Cejalvo, J.M. et al. Talimogene laherparepvec and atezolizumab in HER2-negative breast cancer following neoadjuvant chemotherapy: a window-of-opportunity phase II trial (SOLTI-1503 PROMETEO). Nat Commun 17, 2817 (2026). https://doi.org/10.1038/s41467-026-69222-5
关键词: 溶瘤病毒, 乳腺癌免疫治疗, HER2阴性, 残余肿瘤, 新辅助化疗