Clear Sky Science · de
Talimogene laherparepvec und Atezolizumab bei HER2-negativem Brustkrebs nach neoadjuvanter Chemotherapie: eine Window-of-Opportunity-Phase-II-Studie (SOLTI-1503 PROMETEO)
Neue Hoffnung für hartnäckige Brusttumoren
Viele Frauen mit frühem Brustkrebs erhalten inzwischen vor der Operation intensive Chemotherapie. Bei manchen schrumpft der Tumor so stark, dass bei der Operation kein Tumorresten mehr nachweisbar ist und die Langzeitprognose ausgezeichnet ist. Andere bleiben mit einem sichtbaren Tumorrest zurück, der der Behandlung widerstanden hat. Diese Patientinnen haben ein erhöhtes Risiko für ein Wiederauftreten der Erkrankung. Die PROMETEO-Studie prüfte eine neue Methode, das Immunsystem gegen diesen verbleibenden Tumor „aufzuwecken“, indem ein krebsabtötendes Virus zusammen mit einem immunstimulierenden Antikörper eingesetzt wurde.
Ein Virus als Verbündeter
Die Studie konzentrierte sich auf Frauen mit HER2-negativen Tumoren, eine häufige Brustkrebsvariante, die hormonabhängig oder triple-negativ sein kann. Alle hatten bereits die standardmäßige neoadjuvante Chemotherapie abgeschlossen, wiesen aber noch eine auf Bildern und Biopsie sichtbare Tumormasse von mindestens einem Zentimeter auf, was auf Chemoresistenz hinwies. Die Forschenden setzten Talimogene laherparepvec (T‑VEC) ein, ein modifiziertes Herpesvirus, das Krebszellen infiziert und zerstört und dabei Signale freisetzt, die Immunzellen anziehen. Es wurde mit Atezolizumab kombiniert, einem Antikörper, der die PD‑L1‑„Bremse“ blockiert, die Tumoren nutzen, um Immunangriffe abzuschalten. Die Behandlung erfolgte innerhalb eines 11‑wöchigen Intervalls zwischen Chemotherapie und Operation.
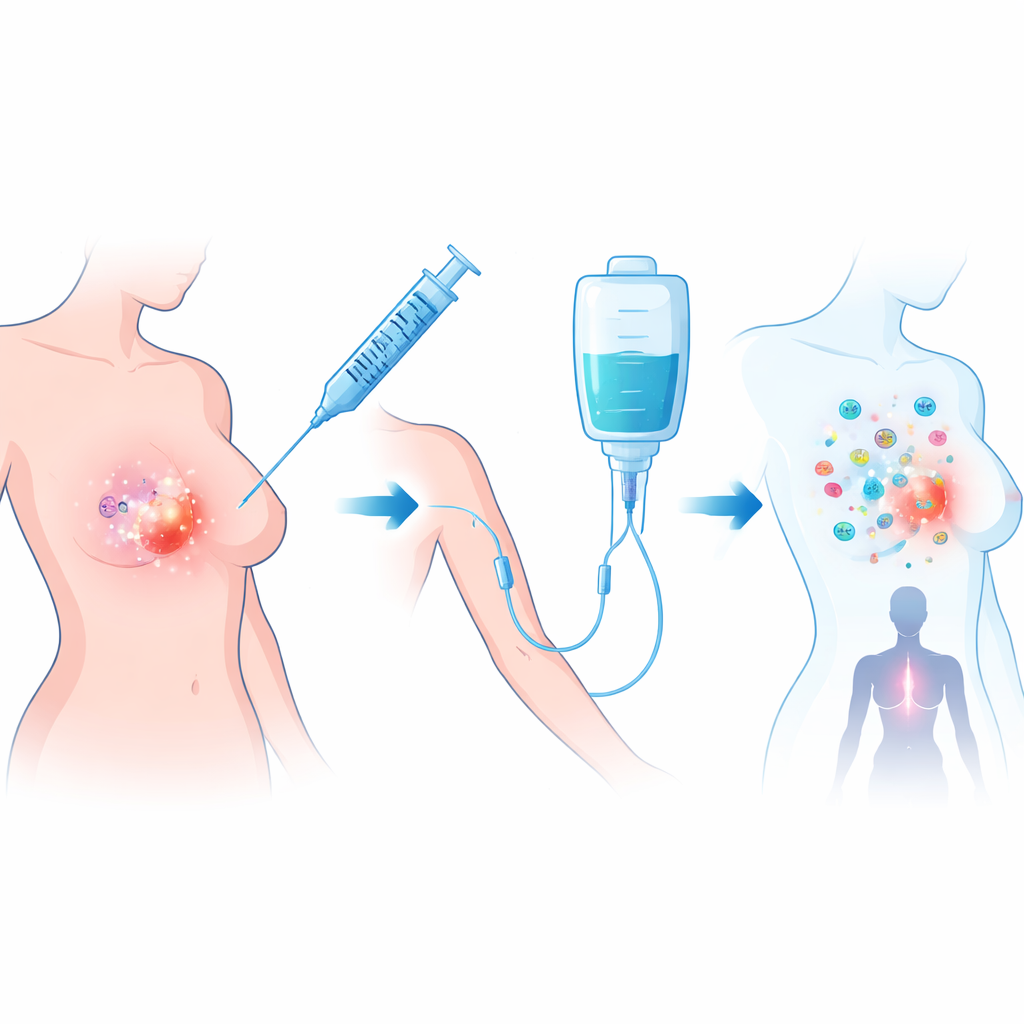
Was die Studie im Operationssaal zeigte
28 Frauen wurden behandelt; die Mehrheit hatte hormonrezeptorpositive, HER2‑negative Tumoren, der Rest war triple‑negativ. Jede Patientin erhielt eine niedrige Anfangsdosis T‑VEC direkt in den Brusttumor, gefolgt von vier höheren Injektionen zusammen mit Atezolizumab‑Infusionen. Bei der späteren Tumorentfernung maßen Pathologen genau, wie viel Tumorrest verblieben war. Bei 7 von 26 auswertbaren Patientinnen — etwa eine von vier — war nach der Operation weder invasiver Tumor in der Brust noch in den Lymphknoten nachweisbar; dieses Ergebnis nennt man pathologisches komplettes Ansprechen. Damit wurde das vordefinierte Ziel der Studie erreicht und das Ergebnis ist bemerkenswert, da alle diese Tumoren zuvor als chemoresistent bestätigt worden waren. Die Behandlung wurde insgesamt gut vertragen; es traten überwiegend milde Nebenwirkungen wie Fieber, Gelenkschmerzen und vorübergehende Blutbildveränderungen auf; lebensbedrohliche Reaktionen oder behandlungsbedingte Todesfälle wurden nicht beobachtet.
Beobachtung, wie das Immunsystem erwacht
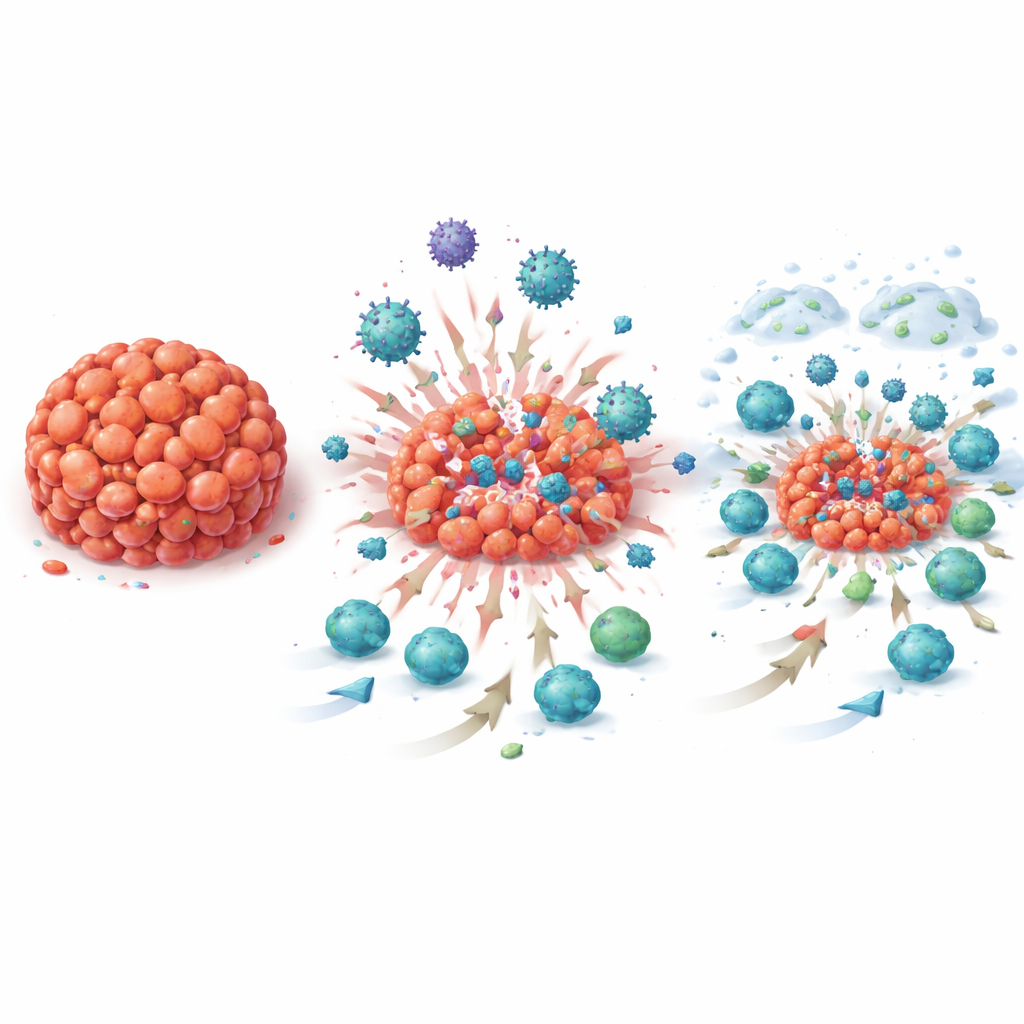
Da es sich um eine Window‑of‑Opportunity‑Studie handelte, entnahm das Team mehrfach Biopsien vor, während und nach der neuen Behandlung und ermöglichte so eine seltene, filmartige Beobachtung der Veränderungen im Tumormilieu über die Zeit. Unter dem Mikroskop zeigte sich eine Zunahme tumorinfiltrierender Lymphozyten — weißer Blutzellen, die Krebs angreifen können — im Verlauf der Behandlung. Strukturen, die winzigen Lymphknoten ähneln, sogenannte tertiäre lymphatische Strukturen, traten häufiger auf, und die Tumoren zeigten öfter Anzeichen von PD‑L1, dem Ziel von Atezolizumab. Die Genaktivitätsanalysen der Tumorproben spiegelten diese visuellen Veränderungen wider: Hunderte immunbezogener Gen‑Signaturen, darunter solche für B‑Zellen, T‑Zellen und Antikörperproduktion, steigerten sich deutlich nach T‑VEC allein und erneut nach der Kombinationstherapie und blieben bis zur Operation erhöht. Diese Veränderungen zeigten sich nicht nur bei Patientinnen, deren Tumoren verschwanden, sondern auch bei denen mit Resttumor, was darauf hindeutet, dass die Strategie allgemein die anti‑tumorale Immunantwort reaktivierte.
Erste Hinweise auf Langzeitschutz
Die Forschenden verfolgten die Patientinnen auch nach der Operation, um zu sehen, ob der Krebs zurückkehrte. Nach einer medianen Nachbeobachtungszeit von fast vier Jahren hatten nur vier Frauen Fernmetastasen entwickelt, und keine dieser Frauen hatte ein komplettes Tumorverschwinden bei der Operation erreicht. Im Gegensatz dazu blieben alle sieben Patientinnen, deren Tumoren komplett eliminiert worden waren, frei von Rückfällen. Obwohl die Fallzahlen gering sind und die Studie keine Kontrollgruppe hatte, stützt dieses Muster die Idee, dass das Beseitigen sichtbarer Tumoren nach der Behandlung eng mit besseren Langzeitresultaten verbunden ist, selbst in dieser Hochrisikogruppe.
Was das für Patientinnen bedeuten könnte
Die PROMETEO‑Studie zeigt, dass das kurzzeitige Hinzufügen eines krebsabtötenden Virus zusammen mit einem immunaktivierenden Antikörper zwischen Chemotherapie und Operation bei Frauen mit HER2‑negativem Brustkrebs, der eine Erstbehandlung überlebt hat, machbar ist und offenbar sicher erscheint. Der Ansatz löste starke Hinweise auf Immunaktivierung in resistenten Tumoren aus und führte bei einem bedeutenden Anteil der Patientinnen, insbesondere bei denen mit hormonrezeptorpositiver Erkrankung — wo solche Anspreche sonst selten sind — zu einem kompletten Tumoransprechen. Größere randomisierte Studien sind erforderlich, um zu bestätigen, ob diese Strategie tatsächlich die Heilungsraten verbessert; die Ergebnisse legen jedoch nahe, dass das Umwandeln des Tumors in ein entzündetes, immunreiches Areal kurz vor der Operation eine neue Möglichkeit bieten könnte, das Rückfallrisiko für Patientinnen mit derzeit begrenzten Optionen zu senken.
Zitation: Pascual, T., Vidal, M., Cejalvo, J.M. et al. Talimogene laherparepvec and atezolizumab in HER2-negative breast cancer following neoadjuvant chemotherapy: a window-of-opportunity phase II trial (SOLTI-1503 PROMETEO). Nat Commun 17, 2817 (2026). https://doi.org/10.1038/s41467-026-69222-5
Schlüsselwörter: onkolytisches Virus, Immuntherapie bei Brustkrebs, HER2-negativ, restliche Erkrankung, neoadjuvante Chemotherapie