Clear Sky Science · es
Talimogene laherparepvec y atezolizumab en cáncer de mama HER2-negativo tras quimioterapia neoadyuvante: ensayo fase II de ventana de oportunidad (SOLTI-1503 PROMETEO)
Nueva esperanza para tumores mamarios resistentes
Muchas mujeres con cáncer de mama en estadio temprano reciben hoy quimioterapia intensiva antes de la cirugía. En algunos casos, esto reduce el tumor tanto que no se detecta cáncer en el momento de la intervención, y su pronóstico a largo plazo es excelente. Pero otras pacientes quedan con una masa visible de cáncer que ha resistido el tratamiento. Estas pacientes afrontan un mayor riesgo de recaída. El estudio PROMETEO evaluó una nueva forma de “despertar” al sistema inmunitario frente a ese cáncer residual usando un virus oncolítico junto con un anticuerpo que potencia la respuesta inmune.
Convertir un virus en aliado
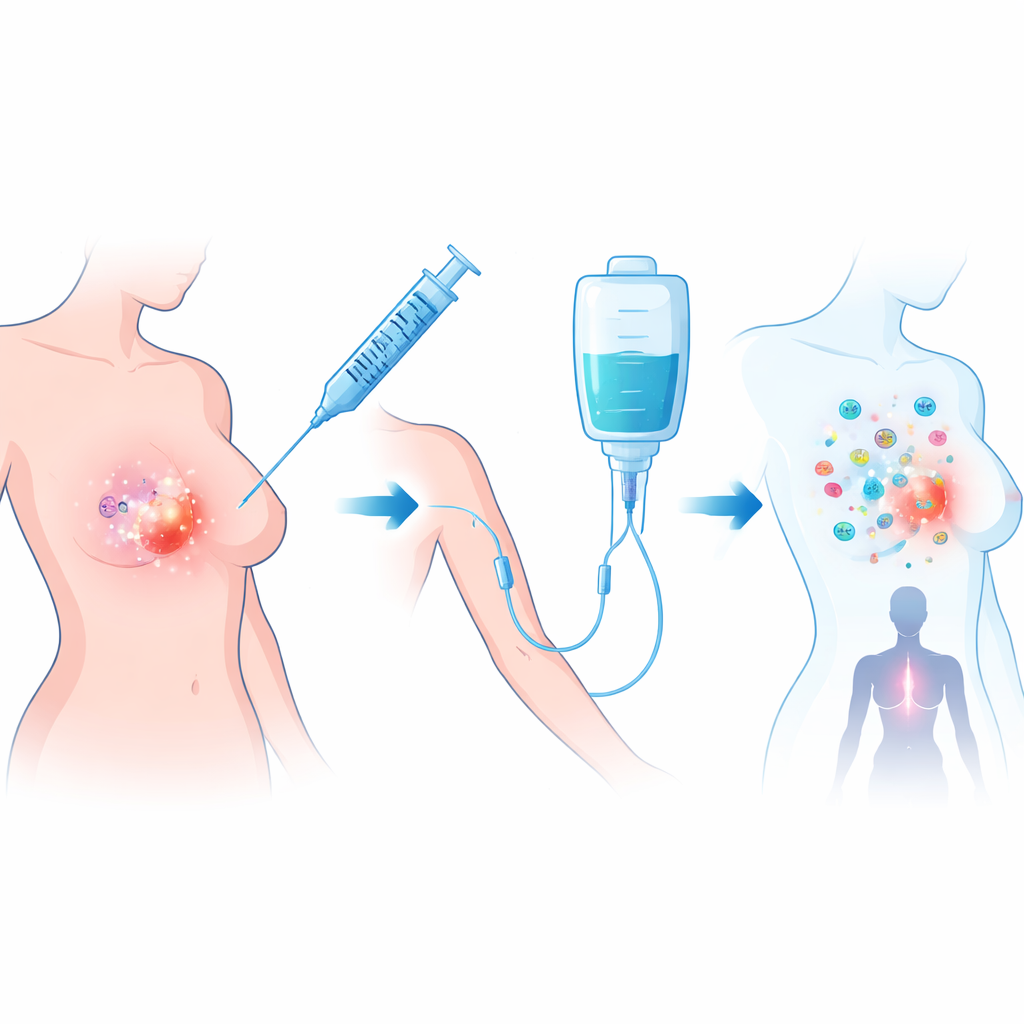
El ensayo se centró en mujeres cuyos tumores carecían de la proteína HER2, un subtipo frecuente de cáncer de mama que puede ser hormonodependiente o triple negativo. Todas habían completado la quimioterapia preoperatoria estándar pero seguían teniendo una masa de al menos un centímetro en imagen y biopsia, lo que demostraba resistencia a los fármacos. Los investigadores emplearon talimogene laherparepvec (T‑VEC), un virus del herpes modificado que infecta y destruye células tumorales a la vez que libera señales que atraen células inmunitarias. Lo combinaron con atezolizumab, un anticuerpo que bloquea el “freno” PD‑L1 que los tumores usan para apagar los ataques inmunitarios. El tratamiento se administró durante una ventana de 11 semanas entre la quimioterapia y la cirugía.
Qué encontró el estudio en el quirófano
Se trataron veintiocho mujeres; la mayoría presentaba tumores hormonorreceptor positivos y HER2‑negativos, y el resto enfermedad triple negativa. Cada paciente recibió una inyección inicial de baja dosis de T‑VEC directamente en el tumor de la mama, seguida de cuatro inyecciones de mayor dosis junto con perfusiones de atezolizumab. Cuando los cirujanos extirparon posteriormente los tumores, los patólogos evaluaron cuidadosamente la cantidad de cáncer restante. En 7 de 26 pacientes evaluables —aproximadamente una de cada cuatro— no quedó cáncer invasivo ni en la mama ni en los ganglios, un resultado conocido como respuesta patológica completa. Esto alcanzó el objetivo predefinido del ensayo y es notable porque todos esos tumores ya habían demostrado ser resistentes a la quimioterapia. El tratamiento fue en general bien tolerado, con efectos secundarios mayoritariamente leves como fiebre, dolores articulares y alteraciones transitorias en analíticas; no hubo reacciones potencialmente letales ni muertes relacionadas con el tratamiento.
Ver al sistema inmunitario despertar
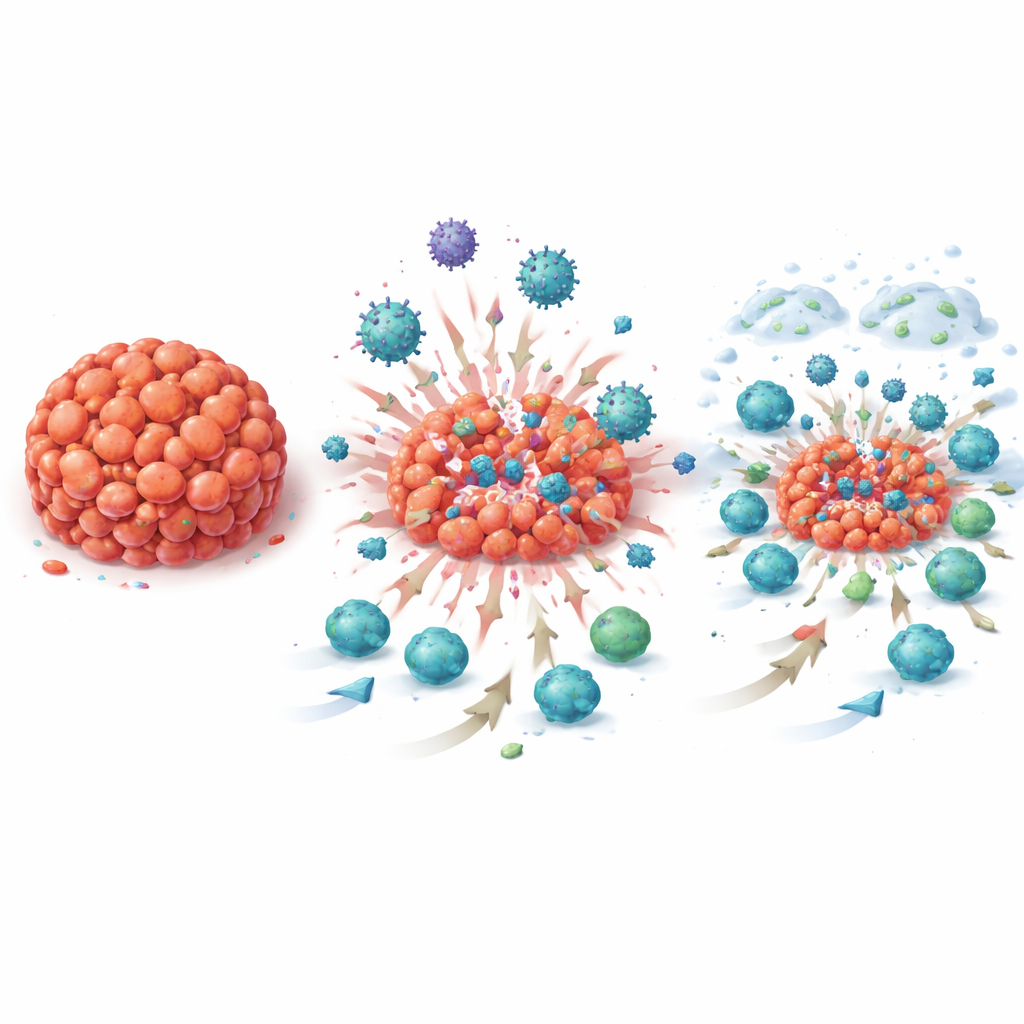
Al ser un ensayo de “ventana de oportunidad”, el equipo recogió múltiples biopsias antes, durante y después del nuevo tratamiento, proporcionando una visión poco habitual, casi cinematográfica, de cómo cambiaba el entorno tumoral con el tiempo. Al microscopio, los investigadores observaron un aumento de linfocitos infiltrantes del tumor —glóbulos blancos capaces de atacar el cáncer— conforme avanzaba el tratamiento. Estructuras semejantes a pequeños ganglios, llamadas estructuras linfoides terciarias, se hicieron más frecuentes, y los tumores mostraron con más frecuencia señales de PD‑L1, precisamente el blanco del atezolizumab. Los análisis de actividad génica de las muestras tumorales respaldaron estos cambios visibles: cientos de firmas génicas relacionadas con la inmunidad, incluidas las asociadas a células B, células T y producción de anticuerpos, aumentaron de forma marcada tras T‑VEC solo y de nuevo tras la terapia combinada, y se mantuvieron elevadas en la cirugía. Estos cambios aparecieron no solo en pacientes cuyos tumores desaparecieron, sino también en aquellas con enfermedad residual, lo que indica que la estrategia reactivó de forma amplia la inmunidad antitumoral.
Primeros indicios sobre protección a largo plazo
Los investigadores también siguieron a las pacientes después de la cirugía para ver si el cáncer reaparecía. Tras una mediana de seguimiento de casi cuatro años, solo cuatro mujeres habían desarrollado metástasis a distancia, y ninguna de ellas había alcanzado una desaparición completa del tumor en la cirugía. En contraste, las siete pacientes cuyos tumores se eliminaron permanecieron libres de recurrencia. Aunque los números son pequeños y el estudio carece de un grupo comparador, este patrón respalda la idea de que eliminar el tumor visible tras el tratamiento se asocia estrechamente con mejores resultados a largo plazo, incluso en este grupo de alto riesgo.
Qué podría significar esto para las pacientes
El ensayo PROMETEO muestra que añadir de forma breve un virus oncolítico más un anticuerpo activador del sistema inmune entre la quimioterapia y la cirugía es factible y parece seguro para mujeres con cáncer de mama HER2‑negativo que ha sobrevivido al tratamiento inicial. El enfoque desencadenó signos claros de activación inmune dentro de tumores resistentes y produjo desaparición completa del tumor en una fracción relevante de pacientes, especialmente en aquellas con enfermedad hormonorreceptor positiva, donde tales respuestas suelen ser raras. Aunque se necesitan ensayos aleatorizados más amplios para confirmar si esta estrategia mejora realmente las tasas de curación, los resultados sugieren que transformar el tumor en un área inflamada y rica en células inmunitarias justo antes de la cirugía podría ofrecer una nueva vía para reducir el riesgo de recaída en pacientes con opciones limitadas actualmente.
Cita: Pascual, T., Vidal, M., Cejalvo, J.M. et al. Talimogene laherparepvec and atezolizumab in HER2-negative breast cancer following neoadjuvant chemotherapy: a window-of-opportunity phase II trial (SOLTI-1503 PROMETEO). Nat Commun 17, 2817 (2026). https://doi.org/10.1038/s41467-026-69222-5
Palabras clave: virus oncolítico, inmunoterapia en cáncer de mama, HER2-negativo, enfermedad residual, quimioterapia neoadyuvante