Clear Sky Science · sv
Talimogene laherparepvec och atezolizumab vid HER2‑negativ bröstcancer efter neoadjuvant kemoterapi: en window-of-opportunity fas II‑studie (SOLTI-1503 PROMETEO)
Ny hopp för svårbehandlade brösttumörer
Många kvinnor med tidig bröstcancer får i dag intensiv kemoterapi före operation. För vissa krymper tumören så mycket att ingen cancer kan hittas vid operationstillfället, och prognosen därefter är utmärkt. Men andra lämnas med en synlig knuta av cancer som har motstått behandlingen. Dessa patienter har en högre risk för återfall. PROMETEO‑studien testade ett nytt sätt att ”väcka” immunförsvaret mot den kvarstående cancern genom att använda ett cancerdödande virus tillsammans med en immunstimulerande antikropp.
Att göra ett virus till en allierad
Studien fokuserade på kvinnor vars tumörer saknade HER2‑proteinet, en vanlig typ av bröstcancer som kan vara hormonkänslig eller trippelnegativ. Alla hade redan slutfört standardiserad preoperativ kemoterapi men hade fortfarande en massa om minst en centimeter på röntgen och biopsi, vilket visade att deras tumörer var läkemedelsresistenta. Forskare använde talimogene laherparepvec (T‑VEC), ett modifierat herpesvirus som infekterar och förstör cancerceller samtidigt som det frigör signaler som lockar immunceller. Det kombinerades med atezolizumab, en antikropp som blockerar PD‑L1‑“bromsen” som tumörer använder för att stänga av immunsvar. Behandlingen gavs under ett 11‑veckors fönster mellan kemoterapi och operation.
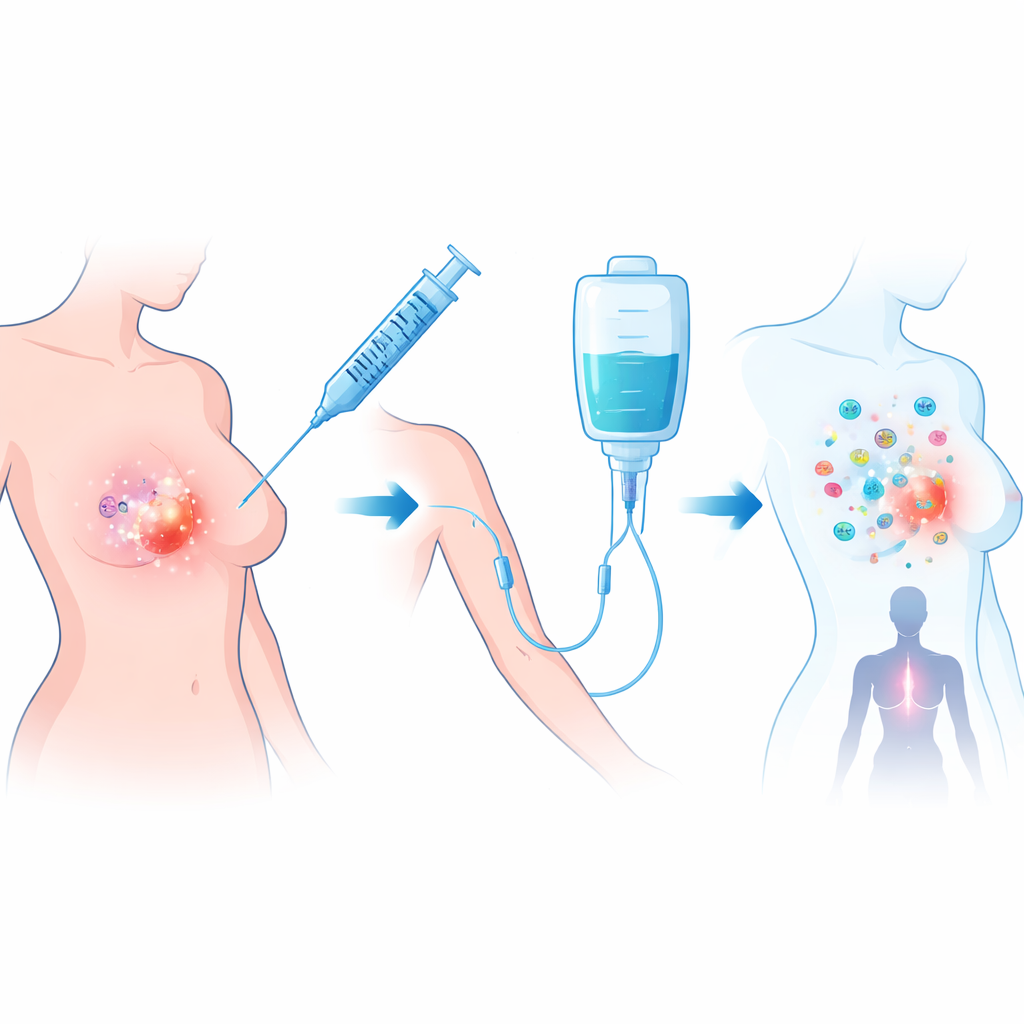
Vad studien fann i operationssalen
Tjugoåtta kvinnor behandlades; de flesta hade hormonkänsliga, HER2‑negativa tumörer och resten hade trippelnegativ sjukdom. Varje patient fick en lågdosinjektion av T‑VEC direkt i brösttumören, följt av fyra högre dosinjektioner tillsammans med infusioner av atezolizumab. När kirurgerna senare avlägsnade tumörerna mätte patologerna noggrant hur mycket cancer som återstod. Hos 7 av 26 utvärderbara patienter — ungefär en av fyra — återstod ingen invasiv cancer i bröst eller lymfkörtlar, ett resultat känt som patologisk komplett respons. Detta uppfyllde studiens fördefinierade mål och är anmärkningsvärt eftersom alla dessa tumörer redan hade visat sig vara resistenta mot kemoterapi. Behandlingen tolererades i allmänhet väl, med mestadels milda biverkningar såsom feber, ledvärk och tillfälliga förändringar i blodprover; inga livshotande reaktioner eller behandlingsrelaterade dödsfall noterades.
Att följa hur immunförsvaret vaknar
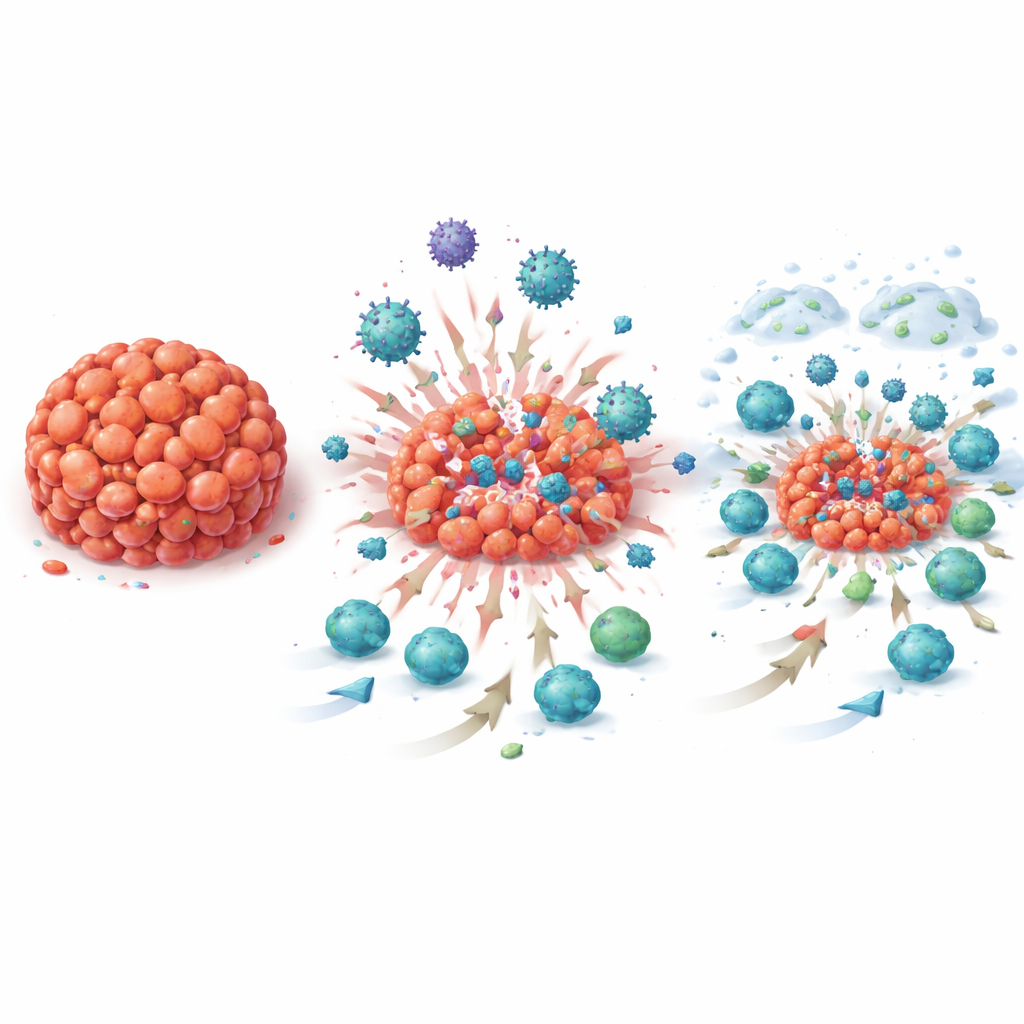
Eftersom detta var en ”window‑of‑opportunity”‑studie samlade teamet flera biopsier före, under och efter den nya behandlingen, vilket gav en sällsynt film‑liknande bild av hur tumörmiljön förändrades över tid. Under mikroskopet såg forskarna ökande antal tumörinfiltrerande lymfocyter — vita blodkroppar som kan angripa cancer — i takt med att behandlingen fortskred. Strukturer som liknar små lymfkörtlar, så kallade tertiära lymfoida strukturer, blev vanligare, och tumörerna visade oftare tecken på PD‑L1, det direkta målet för atezolizumab. Genaktivitetsanalyser av tumörproverna bekräftade dessa visuella förändringar: hundratals immunrelaterade gensignaturer, inklusive de kopplade till B‑celler, T‑celler och antikroppsproduktion, ökade markant efter T‑VEC ensam och ytterligare efter kombinationsbehandlingen, och förblev höga vid operation. Dessa förändringar syntes inte bara hos patienter vars tumörer försvann utan även hos dem med kvarvarande sjukdom, vilket tyder på att strategin i bred mening återaktiverade antitumörimmunitet.
Första tecken på långsiktigt skydd
Forskarna följde också patienterna efter operation för att se om cancern återkom. Efter en medianuppföljning på nästan fyra år hade endast fyra kvinnor utvecklat fjärrmetastaser, och ingen av dessa hade uppnått komplett tumorförsvinnande vid operation. Däremot förblev alla sju patienter vars tumörer rensades fria från återfall. Även om antalet är litet och studien saknar en jämförelsegrupp stöder detta mönster idén att eliminering av synlig cancer efter behandling är starkt kopplat till bättre långtidsresultat, även i denna hög‑riskgrupp.
Vad detta kan innebära för patienter
PROMETEO‑studien visar att det kortvarigt går att lägga till ett cancerdödande virus plus en immunsystemaktiverande antikropp mellan kemoterapi och operation och att detta verkar vara genomförbart och säkert för kvinnor med HER2‑negativ bröstcancer som överlevt initial behandling. Metoden utlöste starka tecken på immunaktivering inne i resistenta tumörer och ledde till komplett tumörförsvinnande hos en meningsfull andel patienter, särskilt bland dem med hormonkänslig sjukdom där sådana svar vanligtvis är sällsynta. Även om större randomiserade studier behövs för att bekräfta om strategin verkligen förbättrar botfrekvensen, antyder resultaten att omvandla tumören till ett inflammerat, immurrikt område strax före operation kan erbjuda ett nytt sätt att minska risken för återfall för patienter som i dag har begränsade alternativ.
Citering: Pascual, T., Vidal, M., Cejalvo, J.M. et al. Talimogene laherparepvec and atezolizumab in HER2-negative breast cancer following neoadjuvant chemotherapy: a window-of-opportunity phase II trial (SOLTI-1503 PROMETEO). Nat Commun 17, 2817 (2026). https://doi.org/10.1038/s41467-026-69222-5
Nyckelord: onkotiskt virus, immunoterapi vid bröstcancer, HER2‑negativ, residual sjukdom, neoadjuvant kemoterapi