Clear Sky Science · it
Talimogene laherparepvec e atezolizumab nel carcinoma mammario HER2-negativo dopo chemioterapia neoadiuvante: uno studio di fase II "window-of-opportunity" (SOLTI-1503 PROMETEO)
Nuova speranza per tumori mammari ostinati
Molte donne con carcinoma mammario iniziale ricevono oggi chemioterapie intensive prima dell’intervento chirurgico. Per alcune la massa tumorale si riduce così tanto da risultare assente al momento dell’operazione, con prospettive a lungo termine eccellenti. Altre però restano con un nodulo visibile di tumore che ha resistito al trattamento. Queste pazienti corrono un rischio maggiore di recidiva. Lo studio PROMETEO ha testato un nuovo approccio per «risvegliare» il sistema immunitario contro il cancro residuo usando un virus oncolitico insieme a un anticorpo che potenzia la risposta immune.
Trasformare un virus in un alleato
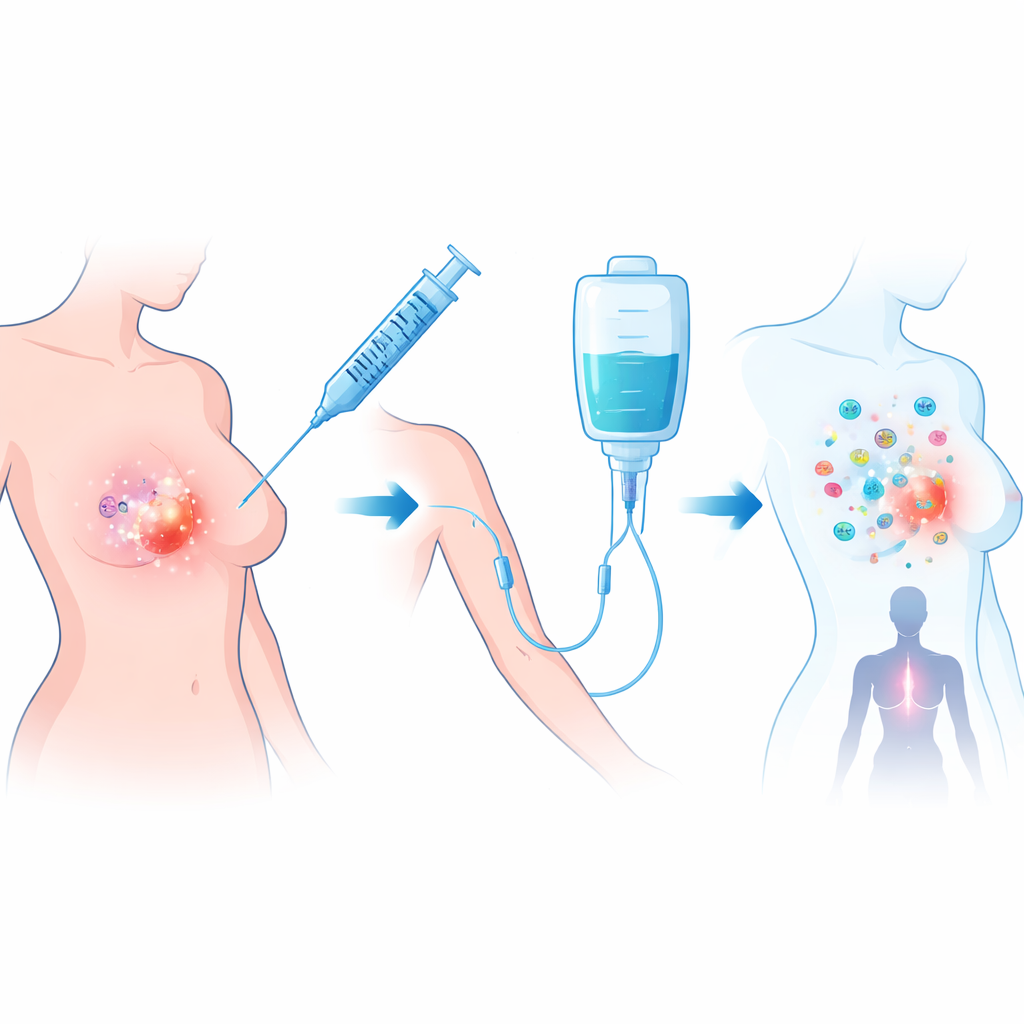
Lo studio ha coinvolto donne i cui tumori non esprimevano la proteina HER2, una forma comune di carcinoma mammario che può essere guidata dagli ormoni o essere triple-negativa. Tutte avevano già completato la chemioterapia preoperatoria standard ma presentavano ancora una massa di almeno un centimetro alla TC e alla biopsia, segno di resistenza ai farmaci. I ricercatori hanno impiegato talimogene laherparepvec (T-VEC), un virus dell’herpes modificato che infetta e distrugge le cellule tumorali rilasciando segnali che attirano cellule immunitarie. Lo hanno associato ad atezolizumab, un anticorpo che blocca il «freno» PD-L1 che i tumori usano per spegnere gli attacchi del sistema immunitario. Il trattamento è stato somministrato durante una finestra di 11 settimane tra chemioterapia e chirurgia.
Cosa ha rivelato lo studio in sala operatoria
Ventotto donne sono state trattate; la maggior parte aveva tumori HR-positivi e HER2-negativi, mentre le rimanenti presentavano malattia triple-negativa. Ogni paziente ha ricevuto un’iniezione a basso dosaggio di T-VEC direttamente nel tumore mammario, seguita da quattro iniezioni a dose più alta abbinate a infusioni di atezolizumab. Quando i chirurghi hanno poi rimosso i tumori, i patologi hanno valutato con cura la quantità di cancro residuo. In 7 delle 26 pazienti valutabili — circa una su quattro — non è risultato alcun carcinoma invasivo né nella mammella né nei linfonodi, un esito definito risposta patologica completa. Questo ha soddisfatto l’obiettivo prefissato dallo studio ed è significativo perché tutti questi tumori avevano già dimostrato resistenza alla chemioterapia. Il trattamento è stato generalmente ben tollerato, con effetti avversi per lo più lievi come febbre, dolori articolari e alterazioni transitorie degli esami del sangue; non si sono verificate reazioni potenzialmente letali né decessi correlati alla terapia.
Osservare il risveglio del sistema immunitario
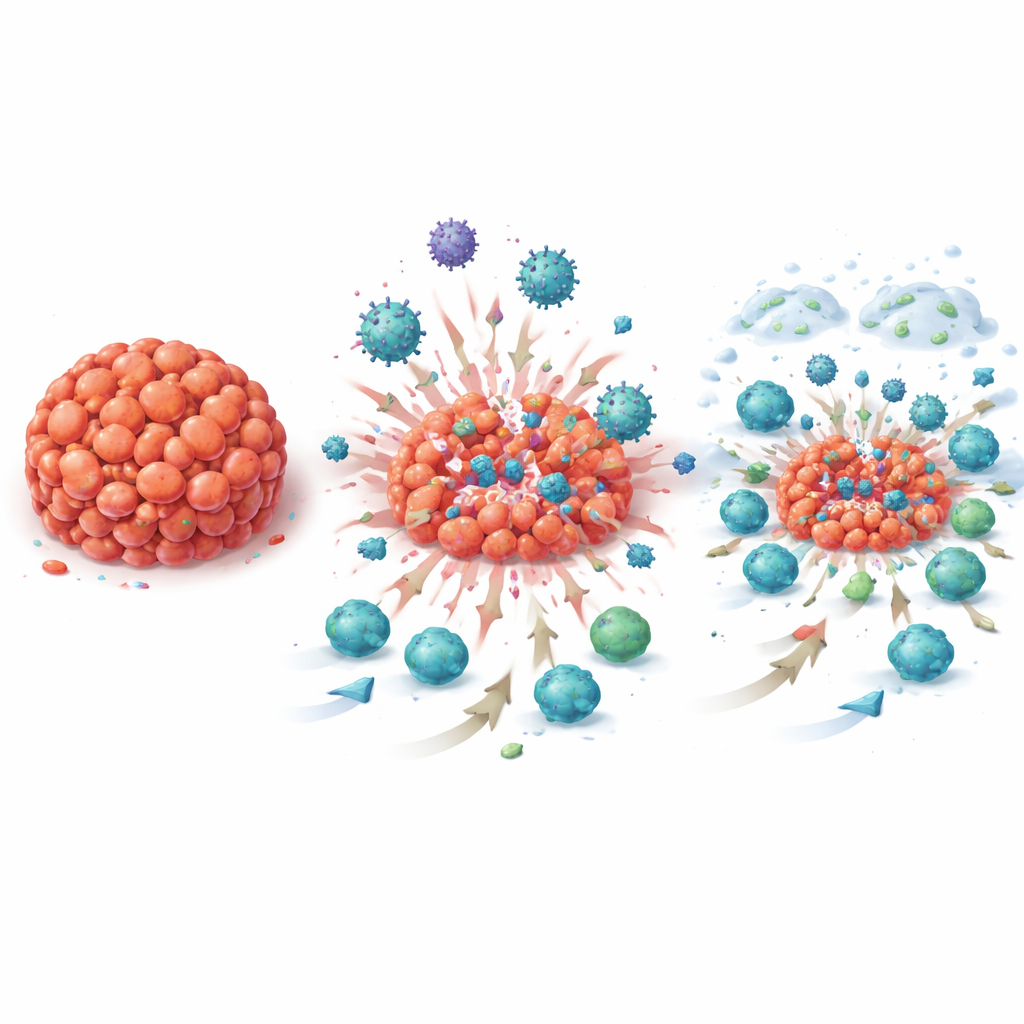
Essendo uno studio di tipo "window-of-opportunity", il team ha raccolto più biopsie prima, durante e dopo il nuovo trattamento, offrendo una rara visione «a film» di come l’ambiente tumorale cambi nel tempo. Al microscopio i ricercatori hanno osservato un aumento delle cellule immunitarie infiltranti il tumore — linfociti capaci di attaccare il cancro — man mano che il trattamento progrediva. Sono diventate più frequenti strutture simili a piccoli linfonodi, chiamate strutture linfatiche terziarie, e i tumori hanno mostrato più spesso segni di espressione di PD-L1, il bersaglio di atezolizumab. Le analisi dell’attività genica sui campioni tumorali hanno rispecchiato questi cambiamenti visivi: centinaia di firme geniche legate all’immunità, incluse quelle associate a cellule B, cellule T e produzione di anticorpi, sono aumentate nettamente dopo T-VEC da solo e di nuovo dopo la terapia combinata, rimanendo elevate al momento della chirurgia. Questi spostamenti sono emersi non solo nelle pazienti i cui tumori sono scomparsi, ma anche in quelle con malattia residua, indicando che la strategia ha rivitalizzato in modo ampio l’immunità anti-tumorale.
Primi indizi sulla protezione a lungo termine
I ricercatori hanno anche seguito le pazienti dopo l’intervento per verificare eventuali recidive. Dopo un follow-up mediano di quasi quattro anni, solo quattro donne hanno manifestato metastasi a distanza, e nessuna di queste aveva ottenuto la scomparsa completa del tumore alla chirurgia. Al contrario, tutte e sette le pazienti il cui tumore era stato azzerato sono rimaste libere da recidive. Pur trattandosi di numeri ridotti e di uno studio privo di gruppo di controllo, questo andamento supporta l’idea che l’eliminazione del cancro visibile dopo il trattamento sia strettamente collegata a migliori risultati a lungo termine, anche in questo gruppo ad alto rischio.
Cosa potrebbe significare per le pazienti
Lo studio PROMETEO dimostra che aggiungere per un breve periodo un virus oncolitico e un anticorpo immune-attivante tra chemioterapia e chirurgia è fattibile e appare sicuro per donne con carcinoma mammario HER2-negativo che ha resistito al trattamento iniziale. L’approccio ha innescato forti segnali di attivazione immunitaria all’interno di tumori resistenti e ha portato alla scomparsa completa del tumore in una frazione significativa di pazienti, soprattutto nelle forme HR-positive, dove tali risposte sono generalmente rare. Sebbene siano necessari studi randomizzati più ampi per confermare se questa strategia migliori realmente i tassi di guarigione, i risultati suggeriscono che trasformare il tumore in un’area infiammata e ricca di cellule immunitarie appena prima dell’intervento potrebbe offrire un nuovo modo per ridurre il rischio di recidiva in pazienti che oggi hanno opzioni limitate.
Citazione: Pascual, T., Vidal, M., Cejalvo, J.M. et al. Talimogene laherparepvec and atezolizumab in HER2-negative breast cancer following neoadjuvant chemotherapy: a window-of-opportunity phase II trial (SOLTI-1503 PROMETEO). Nat Commun 17, 2817 (2026). https://doi.org/10.1038/s41467-026-69222-5
Parole chiave: virus oncolitico, immunoterapia del carcinoma mammario, HER2-negativo, malattia residua, chemioterapia neoadiuvante