Clear Sky Science · pt
Talimogene laherparepvec e atezolizumabe no câncer de mama HER2-negativo após quimioterapia neoadjuvante: um ensaio de fase II tipo janela de oportunidade (SOLTI-1503 PROMETEO)
Nova esperança para tumores de mama persistentes
Muitas mulheres com câncer de mama em estágio inicial recebem hoje quimioterapia intensa antes da cirurgia. Para algumas, isso reduz tanto o tumor que nenhum câncer é encontrado no momento da operação, e a perspectiva de longo prazo é excelente. Mas outras ficam com um nódulo visível de câncer que resistiu ao tratamento. Essas pacientes enfrentam maior risco de recidiva da doença. O estudo PROMETEO testou uma nova forma de “despertar” o sistema imunológico contra esse câncer residual usando um vírus que mata células cancerosas em conjunto com um anticorpo que potencializa a resposta imune.
Transformando um vírus em aliado
O ensaio concentrou-se em mulheres cujos tumores não expressavam a proteína HER2, um tipo comum de câncer de mama que pode ser dirigido por hormônios ou triple‑negative. Todas já haviam concluído a quimioterapia padrão pré‑cirúrgica, mas ainda apresentavam uma massa de pelo menos um centímetro em imagens e biópsia, indicando resistência medicamentosa. Os pesquisadores usaram talimogene laherparepvec (T‑VEC), um vírus herpes modificado que infecta e destrói células tumorais enquanto libera sinais que atraem células imunes. Ele foi combinado com atezolizumabe, um anticorpo que bloqueia o “freio” PD‑L1 que os tumores usam para desligar ataques imunes. O tratamento foi administrado durante uma janela de 11 semanas entre a quimioterapia e a cirurgia.
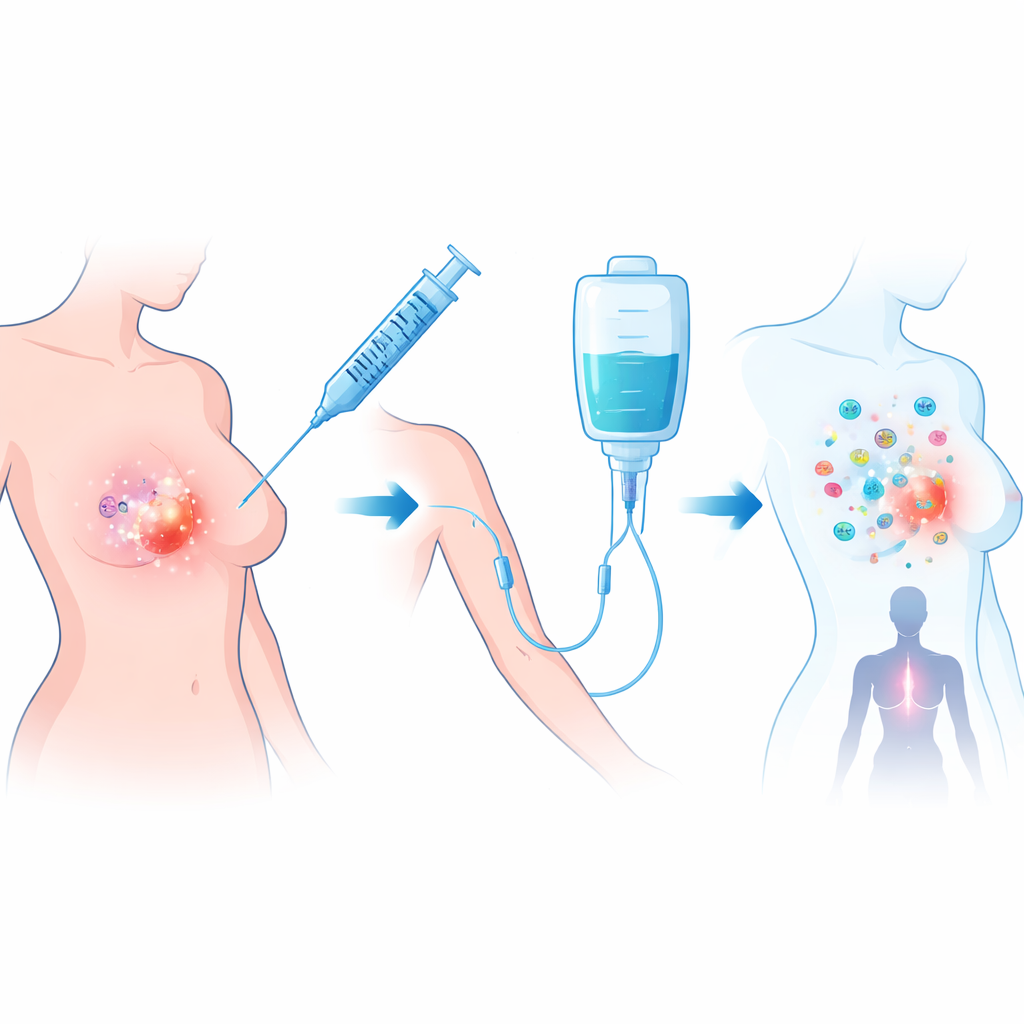
O que o estudo encontrou na sala de cirurgia
Vinte e oito mulheres foram tratadas; a maioria tinha tumores positivos para receptor hormonal e HER2‑negativos, e o restante tinha doença triple‑negative. Cada paciente recebeu uma injeção de T‑VEC em baixa dose diretamente no tumor da mama, seguida por quatro injeções em dose mais alta juntamente com infusões de atezolizumabe. Quando os cirurgiões removeram os tumores, os patologistas avaliaram cuidadosamente quanto câncer restava. Em 7 de 26 pacientes avaliáveis — cerca de uma em cada quatro — não restou câncer invasivo na mama nem nos linfonodos, um resultado conhecido como resposta patológica completa. Isso atingiu a meta predefinida do ensaio e é notável porque todos esses tumores já haviam mostrado resistência à quimioterapia. O tratamento foi geralmente bem tolerado, com efeitos colaterais majoritariamente leves, como febre, dores articulares e alterações transitórias em exames de sangue; não houve reações com risco de vida nem mortes relacionadas ao tratamento.
Observando o despertar do sistema imunológico
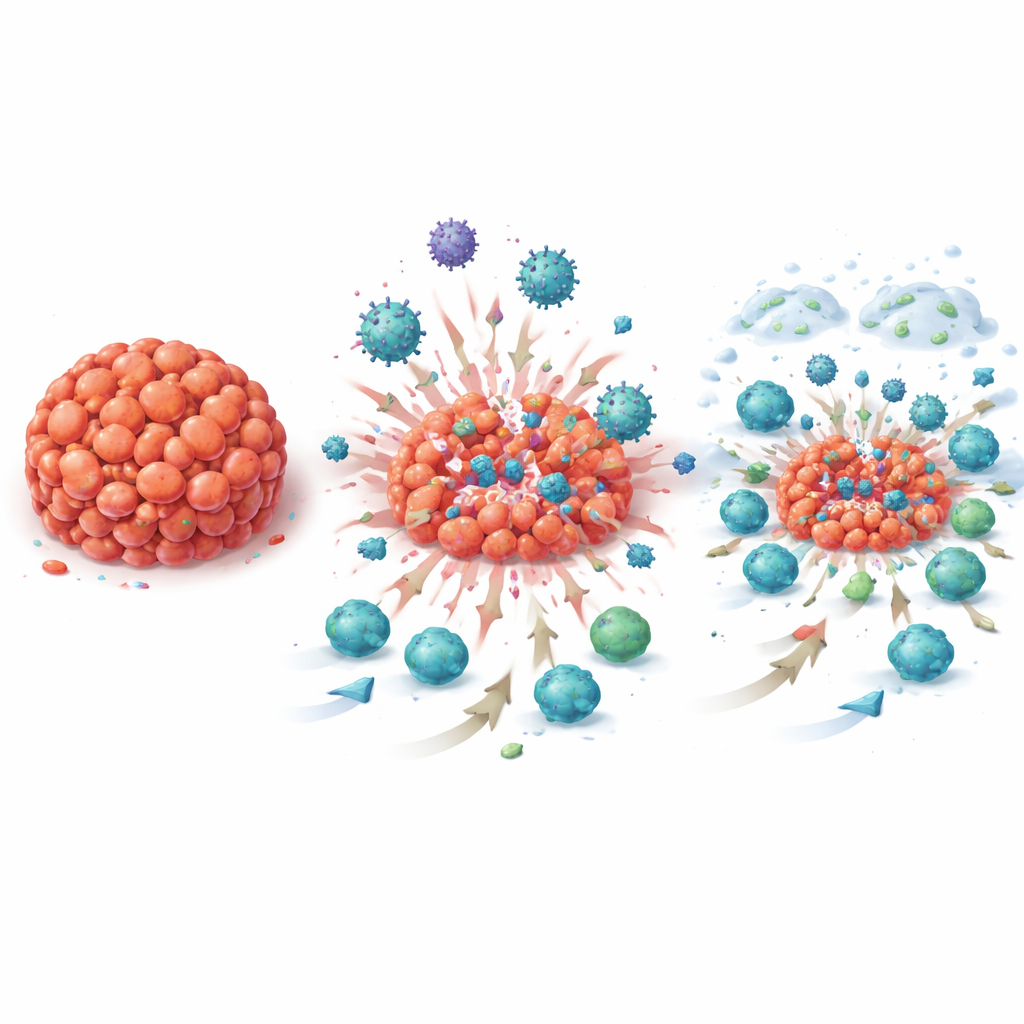
Como este foi um ensaio do tipo “janela de oportunidade”, a equipe coletou múltiplas biópsias antes, durante e após o novo tratamento, oferecendo uma visão rara em forma de filme de como o microambiente tumoral mudou ao longo do tempo. Ao microscópio, os pesquisadores observaram aumento no número de linfócitos infiltrantes de tumor — glóbulos brancos que podem atacar o câncer — conforme o tratamento progredia. Estruturas semelhantes a pequenos linfonodos, chamadas estruturas linfoides terciárias, tornaram‑se mais frequentes, e os tumores passaram a mostrar com mais frequência sinais de PD‑L1, o alvo do atezolizumabe. Análises de atividade gênica das amostras tumorais corroboraram essas mudanças visuais: centenas de assinaturas gênicas relacionadas ao sistema imune, incluindo aquelas associadas a células B, células T e produção de anticorpos, aumentaram fortemente após o T‑VEC isoladamente e novamente após a terapia combinada, mantendo‑se elevadas na cirurgia. Essas alterações apareceram não apenas em pacientes cujos tumores desapareceram, mas também naquelas com doença residual, indicando que a estratégia reenergizou de forma ampla a resposta antitumoral.
Primeiras pistas sobre proteção a longo prazo
Os pesquisadores também acompanharam as pacientes após a cirurgia para verificar se o câncer retornava. Após um seguimento mediano de quase quatro anos, apenas quatro mulheres tiveram metástases à distância, e nenhuma delas havia alcançado desaparecimento completo do tumor na cirurgia. Em contraste, todas as sete pacientes cujos tumores foram eliminados permaneceram livres de recidiva. Embora os números sejam pequenos e o estudo não tenha um grupo de comparação, esse padrão apoia a ideia de que eliminar o câncer visível após o tratamento está intimamente ligado a melhores desfechos a longo prazo, mesmo neste grupo de alto risco.
O que isso pode significar para as pacientes
O ensaio PROMETEO mostra que adicionar brevemente um vírus oncolítico mais um anticorpo ativador do sistema imune entre a quimioterapia e a cirurgia é factível e aparenta ser seguro para mulheres com câncer de mama HER2‑negativo que sobreviveu ao tratamento inicial. A abordagem desencadeou sinais fortes de ativação imune dentro de tumores resistentes e levou ao desaparecimento completo do tumor em uma fração significativa de pacientes, especialmente naquelas com doença positiva para receptor hormonal, em que respostas desse tipo são normalmente raras. Embora ensaios randomizados maiores sejam necessários para confirmar se essa estratégia realmente melhora as taxas de cura, os resultados sugerem que transformar o tumor em uma área inflamada e rica em células imunes pouco antes da cirurgia pode oferecer uma nova maneira de reduzir o risco de recidiva para pacientes que atualmente têm opções limitadas.
Citação: Pascual, T., Vidal, M., Cejalvo, J.M. et al. Talimogene laherparepvec and atezolizumab in HER2-negative breast cancer following neoadjuvant chemotherapy: a window-of-opportunity phase II trial (SOLTI-1503 PROMETEO). Nat Commun 17, 2817 (2026). https://doi.org/10.1038/s41467-026-69222-5
Palavras-chave: vírus oncolítico, imunoterapia do câncer de mama, HER2-negativo, doença residual, quimioterapia neoadjuvante