Clear Sky Science · zh
TGM2 介导的 GPX4 血清素化赋予铁死亡抗性以促进胃肿瘤发生
神经化学物质如何帮助胃肿瘤存活
大多数人将血清素视为影响情绪的“让人感觉良好”的化学物质,但这种分子也在肠道和血液中循环。研究表明,在胃癌患者体内,血清素的作用远不止在神经细胞之间传递信号。它能够直接改变肿瘤细胞内的关键蛋白,帮助细胞抵抗一种细胞死亡方式并更具侵袭性地生长。理解神经系统与癌细胞之间这种隐藏的化学联系,或能为胃癌的诊断和治疗开辟新途径。
肠道化学与胃癌之间的隐秘联系
研究人员首先在有无胃癌的血液样本中测量了数百种小分子,发现癌症患者的血清素水平始终较高。当他们在体外培养的胃癌细胞中加入血清素时,细胞增殖加快;在给予额外血清素的小鼠体内,肿瘤生长也更快。抑制一种名为 TGM2 的酶消除了这种促肿瘤效应,提示血清素的影响不仅依赖于其常见的细胞表面受体,而是通过细胞内更直接的化学修饰发挥作用。
血清素作为蛋白标记的化学物
血清素可以以共价方式连接到蛋白上,这一过程称为“血清素化”,由 TGM2 催化。为找出在胃癌细胞中被如此标记的蛋白,研究团队使用了一种特制的类似血清素的探针,该探针可与蛋白发生“点击”反应,随后被富集并通过质谱鉴定。这一化学蛋白组学筛查发现了 800 多个候选蛋白,许多参与代谢、DNA 修复以及一种由铁驱动的细胞死亡形式——铁死亡。在这些蛋白中,有一种酶尤为突出:GPX4,它是保护细胞膜免受氧化损伤的核心防护者。
肿瘤细胞如何阻断自毁通路
铁死亡是一种内在的自毁程序,当细胞膜中的脂质被高度氧化时会导致细胞死亡。GPX4 通常负责抑制这一过程;当 GPX4 丢失或失活时,铁死亡被触发,癌细胞可能死亡。研究显示,TGM2 在 GPX4 的两个精确位点上化学性地连接血清素。这种血清素化使 GPX4 更加稳定,防止其被另一种标记物——泛素标记,从而送入细胞的蛋白降解机制。没有血清素化时,GPX4 更容易被名为 TRIM25 的酶识别并标记以便降解。经血清素化后,GPX4 得以保存,细胞膜保持受保护,铁死亡被遏制。
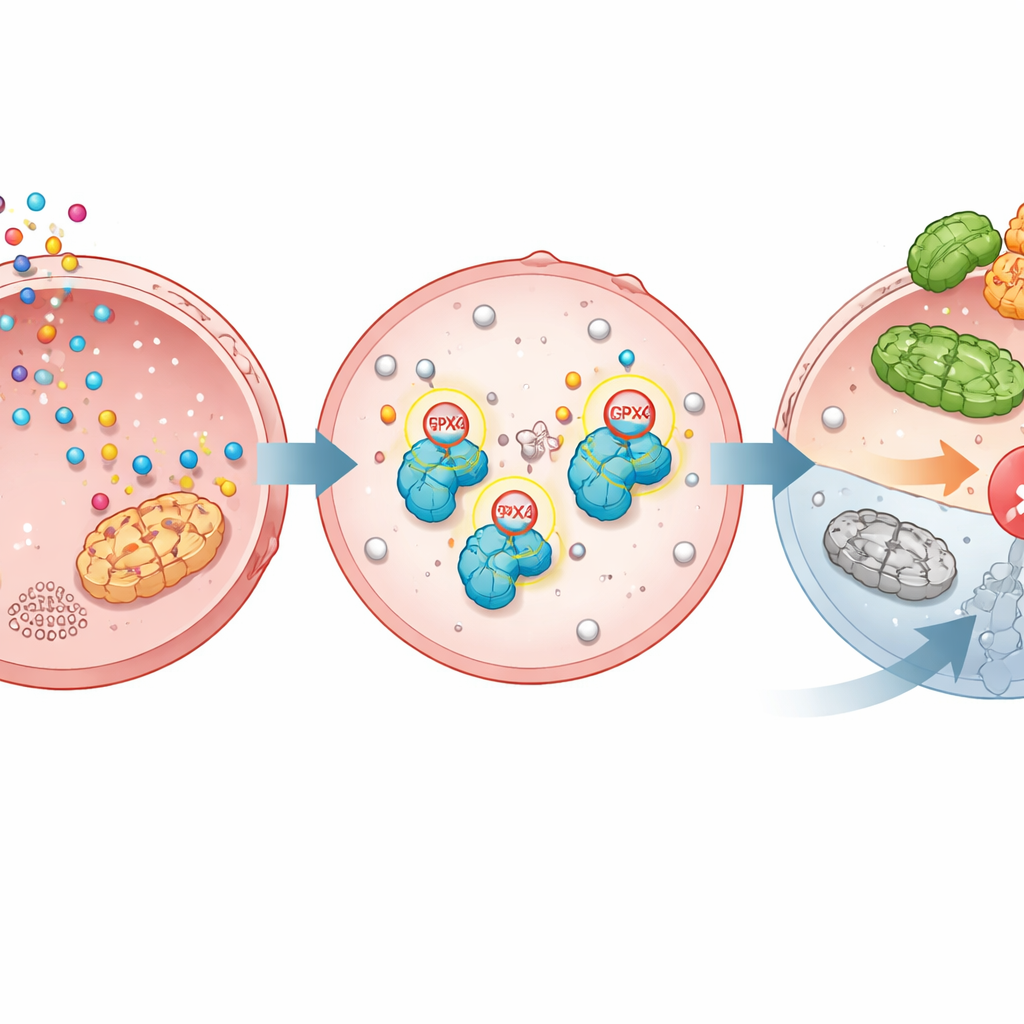
来自工程细胞、小鼠和患者样本的证据
为检验该修饰的重要性,科学家构建了被去除 GPX4 的胃癌细胞,然后分别用正常版本或无法在这两个关键位点被血清素化的突变体替代。只有在存在正常 GPX4 时,血清素才增加细胞生长并保护细胞免受诱导铁死亡药物的侵害,使用不可修饰的版本则无此效果。在小鼠肿瘤模型中,给予血清素加速了携带正常 GPX4 的肿瘤生长,但对携带突变酶的肿瘤影响甚微。在患者数据集和组织样本中,TGM2 和 GPX4 在肿瘤中均高于邻近正常胃组织,且任一者的高表达都与较差的生存率相关,强调了该通路的临床重要性。
这对患者和未来疗法意味着什么
通俗地说,这项工作表明胃肿瘤可以劫持一种通常与情绪相关的神经化学物质,为自身披上对抗强大死亡程序的盔甲。通过将血清素直接连接到 GPX4,肿瘤使用一种化学“锁”使该保护性酶免于被分解,从而使癌细胞在本应致死的条件下存活。该发现提示,检测血清素驱动的 GPX4 修饰可能有助于识别高风险胃癌;针对 TGM2、血清素进入细胞的途径或 GPX4 稳定性的药物,可能恢复铁死亡使肿瘤更易被击败。总之,破坏这一血清素–GPX4 的“安全盾”或可成为治疗胃癌的新策略。
引用: Bai, J., Geng, D., Chen, X. et al. TGM2-mediated serotonylation of GPX4 confers ferroptosis resistance to promote gastric tumorigenesis. Cell Discov 12, 30 (2026). https://doi.org/10.1038/s41421-026-00885-6
关键词: 胃癌, 血清素, 铁死亡, GPX4, 蛋白修饰