Clear Sky Science · nl
TGM2-gemedieerde serotonylatie van GPX4 biedt ferroptoseweerstand en bevordert maagtumorvorming
Hoe zenuwchemie maagtumoren kan helpen overleven
De meeste mensen kennen serotonine als de “goed-gevoel”-stof die stemming beïnvloedt, maar hetzelfde molecuul circuleert ook in de darm en het bloed. Deze studie toont aan dat bij patiënten met maagkanker serotonine veel meer doet dan alleen signalen tussen zenuwcellen doorgeven. Het kan sleutelproteïnen binnen tumorcellen rechtstreeks veranderen, waardoor die cellen resistent worden tegen een bepaalde vorm van celdood en agressiever groeien. Inzicht in deze verborgen chemie tussen het zenuwstelsel en kankercellen kan nieuwe wegen openen voor diagnose en behandeling van maagkanker.
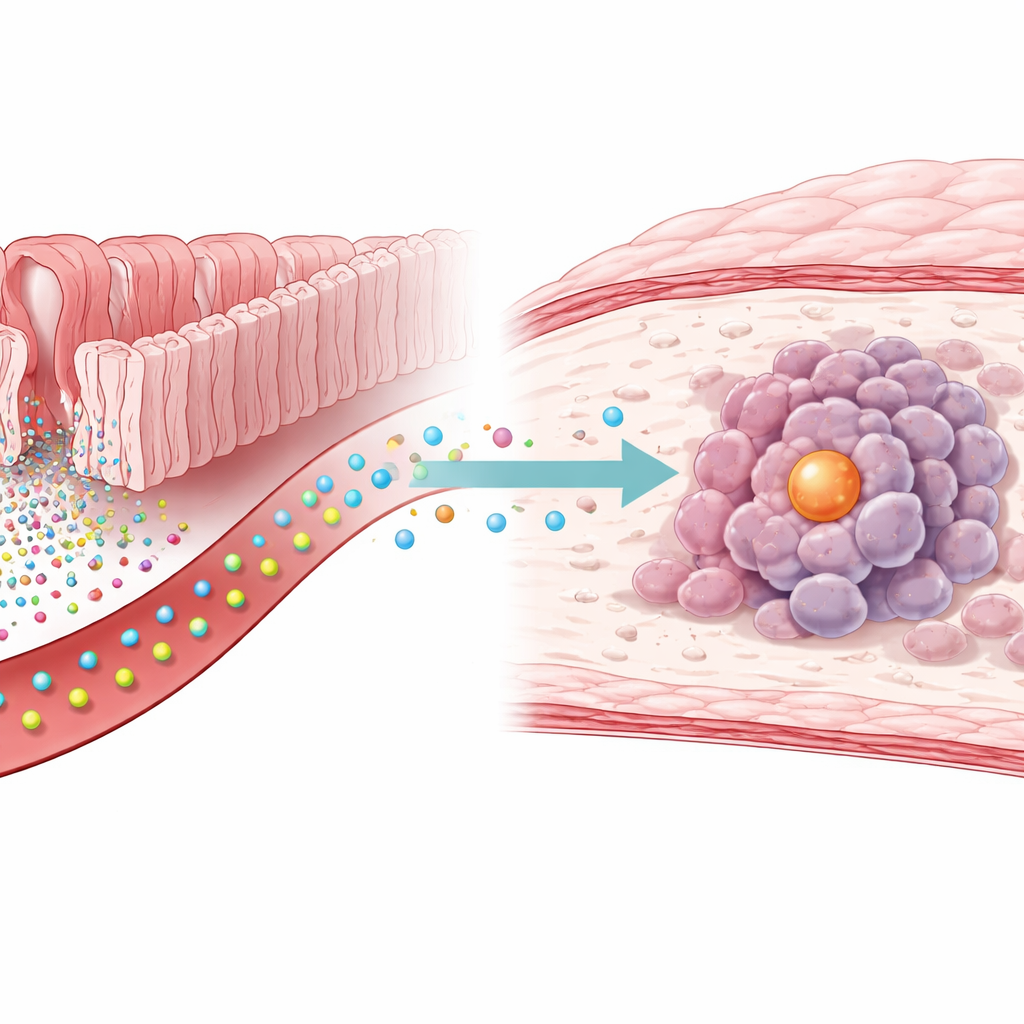
Een verborgen link tussen darmchemie en maagkanker
De onderzoekers begonnen met het meten van honderden kleine moleculen in bloedmonsters van mensen met en zonder maagkanker. Ze vonden dat serotoninespiegels consequent hoger waren bij patiënten met kanker. Wanneer ze serotonine toevoegden aan in het laboratorium gekweekte maagkankercellen, deelden die cellen sneller en groeiden tumoren sneller in muizen die extra serotonine kregen. Het blokkeren van een bepaald enzym, TGM2, wist dit tumorbevorderende effect uit, wat suggereert dat de invloed van serotonine niet alleen van zijn gebruikelijke oppervlaktereceptoren afhangt, maar van een directere chemische modificatie binnen cellen.
Serotonine als eiwit-labelende chemische stof
Serotonine kan covalent aan eiwitten worden gehecht in een proces dat “serotonylatie” wordt genoemd, gecatalyseerd door TGM2. Om te zien welke eiwitten op deze manier werden gemarkeerd in maagkankercellen, gebruikte het team een speciaal ontworpen serotonine-achtig probe dat op eiwitten klikt en kan worden opgevisd en geïdentificeerd met massaspectrometrie. Deze chemoproteomische screening onthulde meer dan 800 kandidaat-eiwitten, veel betrokken bij metabolisme, DNA-herstel en een type ijzergedreven celdood genaamd ferroptose. Daarbij stak één enzym boven de rest uit: GPX4, een belangrijke verdediger die celmembranen beschermt tegen vernietiging door oxidatieve schade.
Hoe tumorcellen een zelfvernietigingspad blokkeren
Ferroptose is een ingebouwd zelfvernietigingsprogramma dat cellen doodt wanneer vetmoleculen in hun membranen sterk geoxideerd raken. GPX4 houdt dit normaal gesproken onder controle; wanneer GPX4 verloren gaat of uitgeschakeld wordt, wordt ferroptose geactiveerd en kunnen kankercellen sterven. De studie laat zien dat TGM2 serotonine chemisch aan GPX4 hecht op twee precieze posities. Deze serotonylatie maakt GPX4 stabieler en beschermt het tegen het worden gemarkeerd met een ander molecuul, ubiquitine, dat het naar de eiwitvernietigingsmachine van de cel zou sturen. Zonder serotonylatie wordt GPX4 makkelijker herkend door een enzym genaamd TRIM25 dat het markeert voor afbraak. Met serotonylatie blijft GPX4 aanwezig, blijven membranen beschermd en wordt ferroptose tegengehouden.
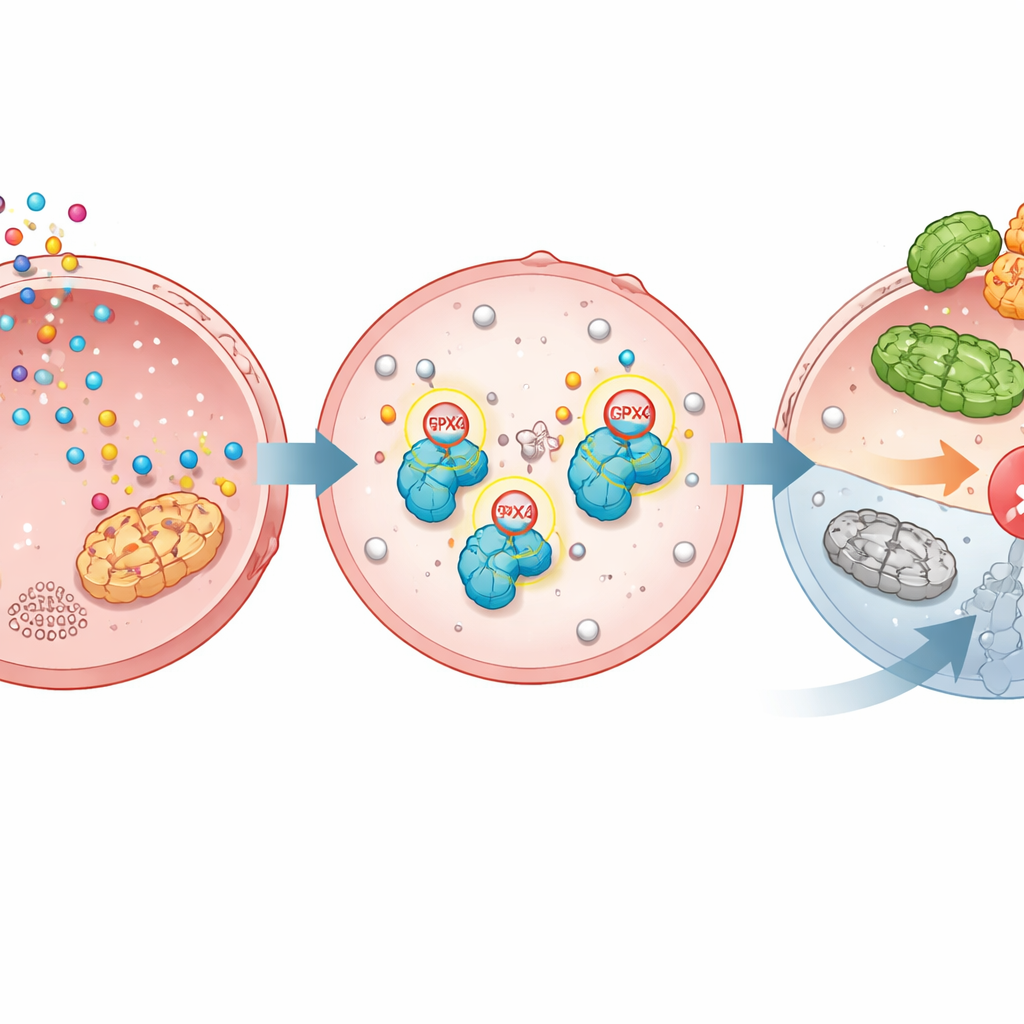
Bewijs uit gemodificeerde cellen, muizen en patiëntmonsters
Om te testen hoe cruciaal deze modificatie is, maakten de wetenschappers maagkankercellen waarin GPX4 werd verwijderd en vervolgens vervangen door ofwel de normale versie ofwel een mutante vorm die niet op de twee sleutelposities serotonylatie kan ondergaan. Serotonine verhoogde de groei en beschermde cellen tegen ferroptose-inducerende medicijnen alleen wanneer normale GPX4 aanwezig was, niet wanneer de niet-bewerkbare versie werd gebruikt. In muismodellen voor tumoren versnelde toediening van serotonine de groei van tumoren met normale GPX4, maar had weinig effect op tumoren met het gemuteerde enzym. In patiëntgegevens en weefselmonsters waren zowel TGM2 als GPX4 verhoogd in tumoren vergeleken met nabijgelegen normaal maagweefsel, en hogere niveaus van één of beide waren verbonden met slechtere overleving, wat het klinische belang van dit pad onderstreept.
Wat dit betekent voor patiënten en toekomstige therapieën
In toegankelijke termen toont dit werk aan dat maagtumoren een zenuwchemicalie die gewoonlijk met stemming geassocieerd wordt, kunnen kapen om zichzelf te bepantseren tegen een krachtig doodsprogramma. Door serotonine rechtstreeks aan GPX4 te hechten, gebruikt de tumor een chemisch “slot” dat dit beschermende enzym tegen afbraak beschermt, waardoor kankercellen kunnen overleven onder omstandigheden die hen normaal zouden doden. Deze ontdekking suggereert dat het meten van serotoninegedreven GPX4-modificatie kan helpen bij het identificeren van hoogrisico-maagkankers en dat geneesmiddelen die TGM2, de serotonine-opname in cellen of de stabiliteit van GPX4 remmen, ferroptose mogelijk kunnen herstellen en tumoren kwetsbaarder maken. Samengevat: het verstoren van dit serotonine–GPX4-veiligheidsmechanisme zou een nieuwe strategie kunnen worden om maagkanker te behandelen.
Bronvermelding: Bai, J., Geng, D., Chen, X. et al. TGM2-mediated serotonylation of GPX4 confers ferroptosis resistance to promote gastric tumorigenesis. Cell Discov 12, 30 (2026). https://doi.org/10.1038/s41421-026-00885-6
Trefwoorden: maagkanker, serotonine, ferroptose, GPX4, eiwitmodificatie