Clear Sky Science · es
La serotonilación mediada por TGM2 de GPX4 confiere resistencia a la ferroptosis y promueve la tumorigénesis gástrica
Cómo los químicos nerviosos pueden ayudar a que los tumores estomacales sobrevivan
La mayoría de la gente conoce la serotonina como el químico que “mejora el ánimo”, pero esa misma molécula también circula en el intestino y en la sangre. Este estudio revela que en pacientes con cáncer gástrico, la serotonina hace mucho más que enviar señales entre neuronas. Puede alterar directamente proteínas clave dentro de las células tumorales, ayudándolas a resistir una forma de muerte celular y a crecer de manera más agresiva. Entender esta química oculta entre el sistema nervioso y las células cancerosas puede abrir nuevas vías para diagnosticar y tratar el cáncer de estómago.
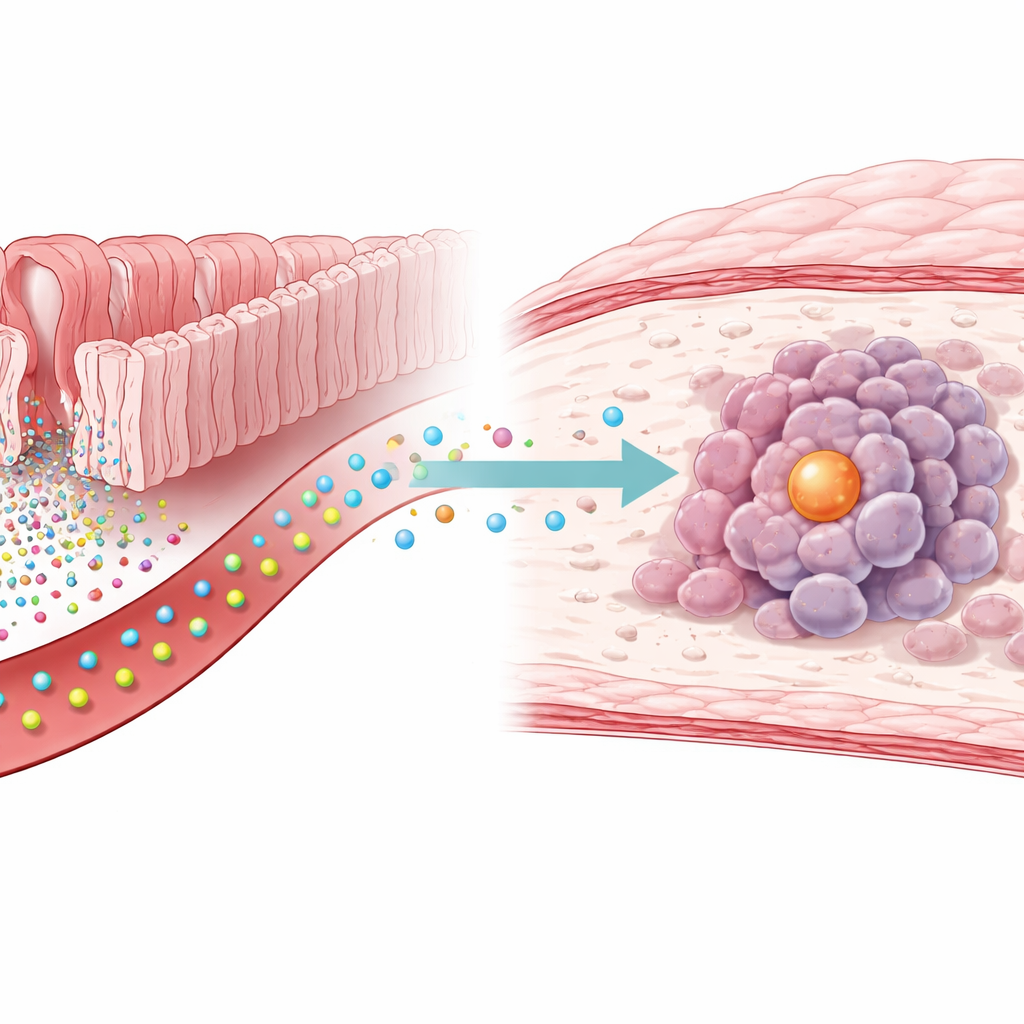
Un vínculo oculto entre la química intestinal y el cáncer de estómago
Los investigadores empezaron midiendo cientos de pequeñas moléculas en muestras de sangre de personas con y sin cáncer gástrico. Encontraron que los niveles de serotonina eran sistemáticamente más altos en los pacientes con cáncer. Cuando añadieron serotonina a células de cáncer gástrico cultivadas en el laboratorio, las células se multiplicaron más rápido, y los tumores crecieron más deprisa en ratones alimentados con serotonina adicional. Bloquear una enzima concreta llamada TGM2 eliminó este efecto de potenciación tumoral, lo que sugiere que la influencia de la serotonina no dependía solo de sus receptores en la superficie, sino de una modificación química más directa dentro de las células.
La serotonina como químico que etiqueta proteínas
La serotonina puede unirse covalentemente a proteínas en un proceso conocido como “serotonilación”, catalizado por TGM2. Para ver qué proteínas eran marcadas así en células de cáncer gástrico, el equipo utilizó una sonda diseñada a partir de serotonina que se enlaza a las proteínas y puede ser recuperada e identificada por espectrometría de masas. Este cribado quimio-proteómico descubrió más de 800 proteínas candidatas, muchas implicadas en metabolismo, reparación del ADN y en un tipo de muerte celular impulsada por hierro llamada ferroptosis. Entre ellas destacó una enzima: GPX4, un defensor maestro que protege las membranas celulares de ser destruidas por daño oxidativo.
Cómo las células tumorales bloquean una vía de autodestrucción
La ferroptosis es un programa de autodestrucción que mata células cuando los lípidos de sus membranas se oxidan en exceso. GPX4 normalmente mantiene esto bajo control; cuando GPX4 se pierde o se inactiva, se desencadena la ferroptosis y las células cancerosas pueden morir. El estudio muestra que TGM2 une químicamente serotonina a GPX4 en dos posiciones precisas. Esta serotonilación hace a GPX4 más estable, protegiéndola de ser marcada con otra molécula, la ubiquitina, que la enviaría al triturador proteico de la célula. Sin serotonilación, GPX4 es más fácilmente reconocida por una enzima llamada TRIM25 que la marca para su destrucción. Con la serotonilación, GPX4 persiste, las membranas permanecen protegidas y la ferroptosis queda contenida.
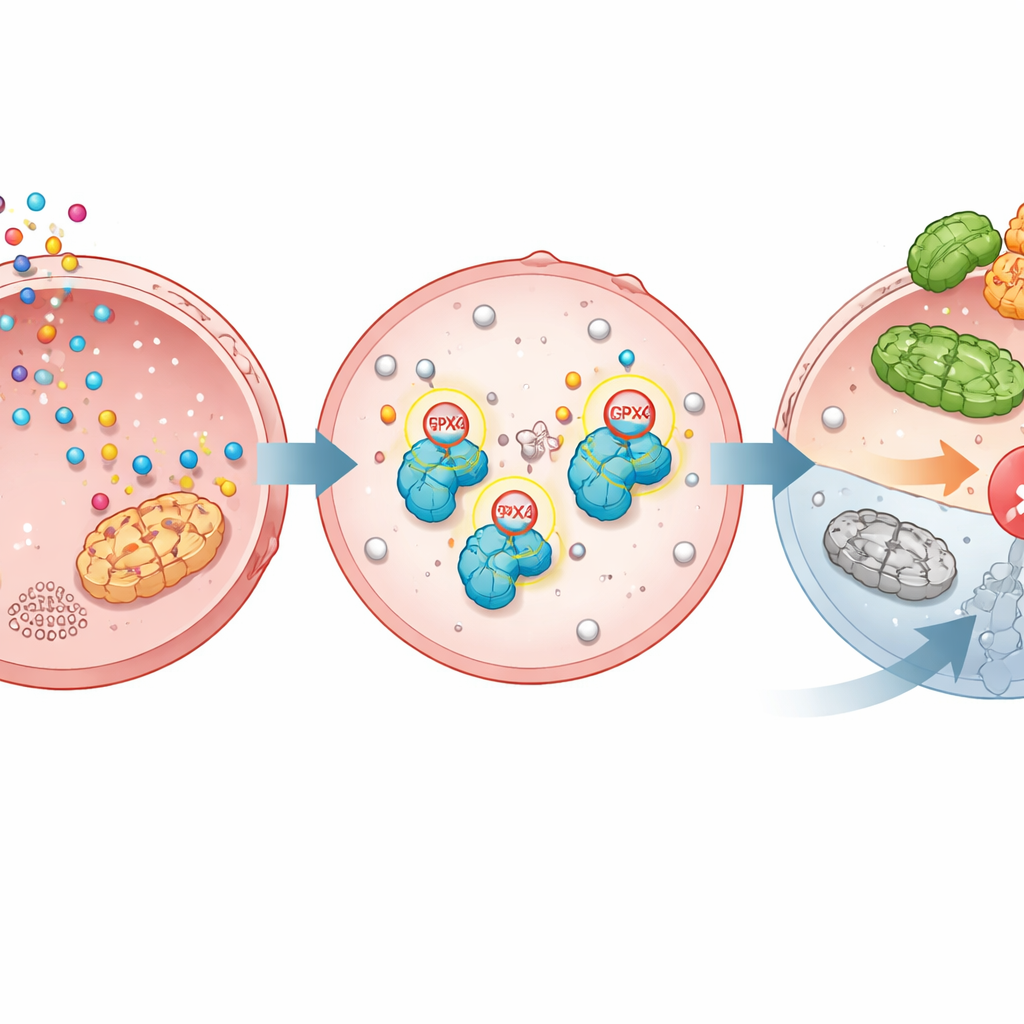
Pruebas con células modificadas, ratones y muestras de pacientes
Para comprobar cuán crucial es esta modificación, los científicos diseñaron células de cáncer gástrico en las que GPX4 fue eliminada y luego reemplazada por la versión normal o por una forma mutante que no puede ser serotonilada en las dos posiciones clave. La serotonina aumentó el crecimiento y protegió a las células frente a fármacos inductores de ferroptosis solo cuando estaba presente la GPX4 normal, no cuando se usó la versión no modificable. En modelos tumorales en ratones, suministrar serotonina aceleró el crecimiento de tumores con GPX4 normal, pero tuvo poco efecto en tumores con la enzima mutante. En conjuntos de datos clínicos y muestras de tejido, tanto la enzima TGM2 como GPX4 estaban elevadas en los tumores en comparación con el tejido gástrico normal adyacente, y niveles más altos de cualquiera de las dos se asociaron con peor supervivencia, subrayando la importancia clínica de esta vía.
Qué implica esto para los pacientes y las terapias futuras
En términos accesibles, este trabajo muestra que los tumores de estómago pueden secuestrar un químico nervioso habitualmente asociado al estado de ánimo para protegerse frente a un potente programa de muerte. Al unir la serotonina directamente a GPX4, el tumor emplea una “cerradura” química que impide que esta enzima protectora sea degradada, permitiendo que las células cancerosas sobrevivan en condiciones que deberían matarlas. Este descubrimiento sugiere que medir la modificación de GPX4 impulsada por serotonina podría ayudar a identificar cánceres gástricos de alto riesgo y que fármacos dirigidos a TGM2, al transporte de serotonina hacia el interior celular o a la estabilidad de GPX4 podrían restaurar la ferroptosis y hacer a los tumores más vulnerables. En resumen, desactivar este escudo de serotonina–GPX4 podría convertirse en una nueva estrategia para tratar el cáncer de estómago.
Cita: Bai, J., Geng, D., Chen, X. et al. TGM2-mediated serotonylation of GPX4 confers ferroptosis resistance to promote gastric tumorigenesis. Cell Discov 12, 30 (2026). https://doi.org/10.1038/s41421-026-00885-6
Palabras clave: cáncer gástrico, serotonina, ferroptosis, GPX4, modificación de proteínas