Clear Sky Science · it
La serotonilazione mediata da TGM2 di GPX4 conferisce resistenza alla ferroptosi promuovendo la tumorigenesi gastrica
Come le sostanze chimiche nervose possono aiutare i tumori allo stomaco a sopravvivere
La maggior parte delle persone conosce la serotonina come la sostanza che migliora l’umore, ma la stessa molecola circola anche nell’intestino e nel sangue. Questo studio rivela che nei pazienti con cancro gastrico la serotonina fa molto più che trasmettere segnali tra le cellule nervose. Può modificare direttamente proteine chiave all’interno delle cellule tumorali, aiutandole a resistere a una forma di morte cellulare e a crescere più aggressivamente. Comprendere questa chimica nascosta tra il sistema nervoso e le cellule tumorali potrebbe aprire nuove vie per diagnosticare e trattare il cancro dello stomaco.
Un legame nascosto tra chimica intestinale e cancro gastrico
I ricercatori hanno iniziato misurando centinaia di piccole molecole in campioni di sangue di persone con e senza cancro gastrico. Hanno riscontrato che i livelli di serotonina erano costantemente più alti nei pazienti con tumore. Quando hanno aggiunto serotonina a cellule di cancro gastrico coltivate in laboratorio, le cellule si sono moltiplicate più rapidamente, e i tumori sono cresciuti più velocemente nei topi a cui è stata somministrata serotonina aggiuntiva. Il blocco di un particolare enzima chiamato TGM2 ha annullato questo effetto promotore del tumore, suggerendo che l’influenza della serotonina non dipendeva solo dai suoi recettori superficiali abituali, ma da una modifica chimica diretta all’interno delle cellule.
La serotonina come agente che etichetta le proteine
La serotonina può essere legata covalentemente alle proteine in un processo noto come “serotonilazione”, catalizzato da TGM2. Per vedere quali proteine erano marcate in questo modo nelle cellule di cancro gastrico, il gruppo ha usato una sonda simile alla serotonina progettata per legarsi alle proteine e poter essere pescata e identificata mediante spettrometria di massa. Questo screening chemoproteomico ha rivelato oltre 800 proteine candidate, molte coinvolte nel metabolismo, nella riparazione del DNA e in un tipo di morte cellulare guidata dal ferro chiamata ferroptosi. Tra queste, un enzima è emerso come particolarmente rilevante: GPX4, un difensore principale che protegge le membrane cellulari dall’essere distrutte dal danno ossidativo.
Come le cellule tumorali bloccano un percorso di autodistruzione
La ferroptosi è un programma di autodistruzione che uccide le cellule quando i lipidi nelle loro membrane diventano fortemente ossidati. GPX4 normalmente mantiene questo processo sotto controllo; quando GPX4 viene perso o disattivato, si innesca la ferroptosi e le cellule tumorali possono morire. Lo studio mostra che TGM2 attacca chimicamente la serotonina a GPX4 in due posizioni precise. Questa serotonilazione rende GPX4 più stabile, proteggendolo dall’essere marcato con un’altra molecola, l’ubiquitina, che lo manderebbe al trituratore proteico della cellula. In assenza di serotonilazione, GPX4 è più facilmente riconosciuto da un enzima chiamato TRIM25 che lo segnala per la distruzione. Con la serotonilazione, GPX4 persiste, le membrane rimangono protette e la ferroptosi viene tenuta a bada.
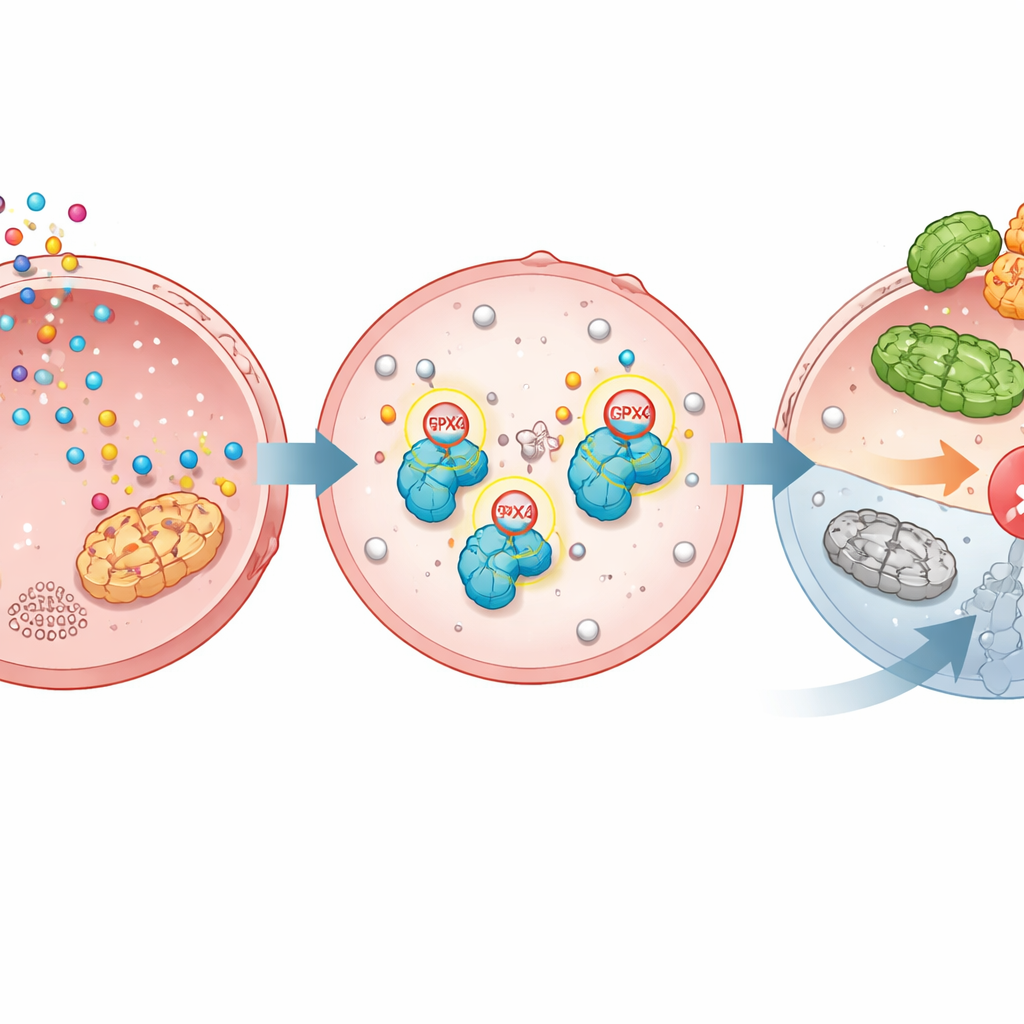
Prove da cellule ingegnerizzate, topi e campioni di pazienti
Per verificare l’importanza di questa modifica, gli scienziati hanno ingegnerizzato cellule di cancro gastrico in cui GPX4 è stato rimosso e poi ricompreso o con la versione normale o con una forma mutante che non può essere serotonilata nelle due posizioni chiave. La serotonina ha aumentato la crescita e protetto le cellule dai farmaci che inducono la ferroptosi solo quando era presente GPX4 normale, non quando era usata la versione non modificabile. Nei modelli tumorali murini, la somministrazione di serotonina ha accelerato la crescita dei tumori portatori di GPX4 normale, ma ha avuto poco effetto sui tumori con l’enzima mutante. Nei set di dati dei pazienti e nei campioni tissutali, sia l’enzima TGM2 che GPX4 risultavano elevati nei tumori rispetto al tessuto gastrico normale adiacente, e livelli più alti di uno o dell’altro erano associati a una sopravvivenza peggiore, sottolineando l’importanza clinica di questa via.
Cosa significa per i pazienti e per le terapie future
In termini accessibili, questo lavoro mostra che i tumori gastrici possono sfruttare una sostanza chimica nervosa solitamente associata all’umore per armarsi contro un potente programma di morte. Attaccando la serotonina direttamente a GPX4, il tumore utilizza una «serratura» chimica che impedisce a questo enzima protettivo di essere degradato, permettendo alle cellule cancerose di sopravvivere a condizioni che dovrebbero ucciderle. Questa scoperta suggerisce che misurare la modificazione di GPX4 guidata dalla serotonina potrebbe aiutare a identificare i tumori gastrici ad alto rischio e che farmaci mirati contro TGM2, contro l’ingresso della serotonina nelle cellule o contro la stabilità di GPX4 potrebbero ripristinare la ferroptosi e rendere i tumori più vulnerabili. In sintesi, interrompere questo scudo di sicurezza serotonina–GPX4 potrebbe diventare una nuova strategia per trattare il cancro dello stomaco.
Citazione: Bai, J., Geng, D., Chen, X. et al. TGM2-mediated serotonylation of GPX4 confers ferroptosis resistance to promote gastric tumorigenesis. Cell Discov 12, 30 (2026). https://doi.org/10.1038/s41421-026-00885-6
Parole chiave: cancro gastrico, serotonina, ferroptosi, GPX4, modificazione proteica