Clear Sky Science · de
TGM2-vermittelte Serotonylierung von GPX4 verleiht Ferroptose-Resistenz und fördert die Entstehung von Magenkrebs
Wie Nervenchemikalien Magen-Tumoren beim Überleben helfen können
Die meisten Menschen kennen Serotonin als den „Wohlfühl“-Botenstoff, der die Stimmung beeinflusst. Dieselbe Substanz zirkuliert jedoch auch im Darm und im Blut. Diese Studie zeigt, dass Serotonin bei Patientinnen und Patienten mit Magenkrebs weit mehr tut als Signale zwischen Nervenzellen zu übertragen. Es kann Schlüsselproteine in Tumorzellen direkt verändern, wodurch diese einer Form des Zelltods widerstehen und aggressiver wachsen. Das Verständnis dieser verborgenen Chemie zwischen Nervensystem und Krebszellen könnte neue Wege zur Diagnose und Behandlung von Magenkrebs eröffnen.
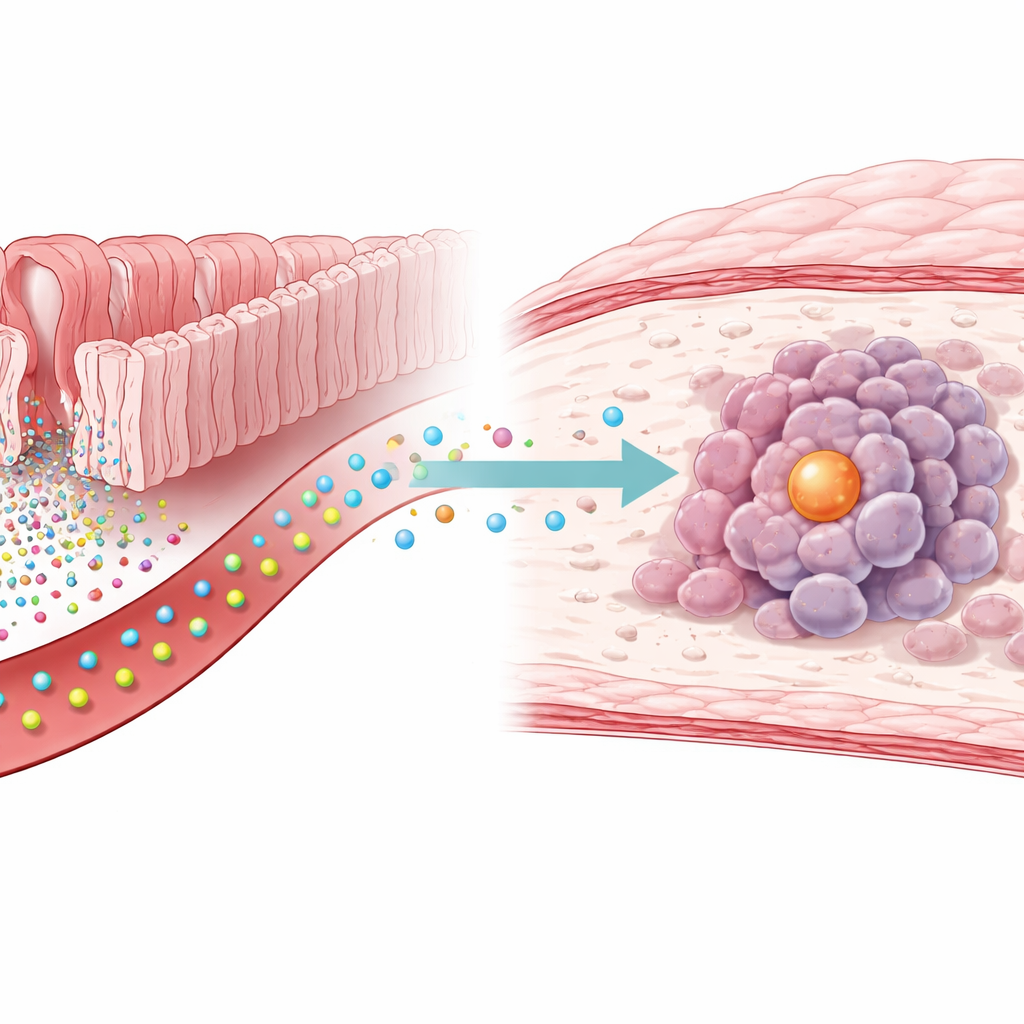
Eine verborgene Verbindung zwischen Darmchemie und Magenkrebs
Die Forschenden begannen damit, Hunderte kleiner Moleküle in Blutproben von Menschen mit und ohne Magenkrebs zu messen. Sie stellten fest, dass die Serotoninwerte bei Patientinnen und Patienten mit Krebs durchgehend erhöht waren. Als sie Serotonin zu im Labor gezüchteten Magenkrebszellen hinzufügten, teilten sich die Zellen schneller, und bei Mäusen, die zusätzliches Serotonin erhielten, wuchsen Tumoren schneller. Die Blockade eines bestimmten Enzyms namens TGM2 beseitigte diesen tumorfördernden Effekt, was darauf hindeutet, dass Serotonins Einfluss nicht allein von seinen üblichen Oberflächenrezeptoren abhängt, sondern von einer direkteren chemischen Modifikation innerhalb der Zellen.
Serotonin als Protein-Markierungsstoff
Serotonin kann kovalent an Proteine gebunden werden in einem Prozess, der als „Serotonylierung“ bekannt ist und von TGM2 katalysiert wird. Um herauszufinden, welche Proteine in Magenkrebszellen auf diese Weise markiert werden, setzte das Team eine speziell entwickelte, serotoninähnliche Sonde ein, die an Proteine anclickt und per Massenspektrometrie herausgefischt und identifiziert werden kann. Dieses Chemoproteomik-Screening deckte mehr als 800 Kandidatenproteine auf, viele davon in Stoffwechselwegen, der DNA-Reparatur und einer eisenabhängigen Form des Zelltods namens Ferroptose. Unter diesen stach ein Enzym besonders hervor: GPX4, ein zentraler Schutzmechanismus, der Zellmembranen vor zerstörerischen oxidativen Schäden bewahrt.
Wie Tumorzellen einen Selbstmordmechanismus blockieren
Ferroptose ist ein eingebautes Selbstzerstörungsprogramm, das Zellen tötet, wenn Fettsäuren in ihren Membranen stark oxidiert werden. GPX4 hält dies normalerweise in Schach; geht GPX4 verloren oder wird es deaktiviert, wird Ferroptose ausgelöst und Krebszellen können absterben. Die Studie zeigt, dass TGM2 Serotonin chemisch an GPX4 an zwei genauen Positionen anbindet. Diese Serotonylierung macht GPX4 stabiler und schützt es davor, mit einem anderen Molekül, Ubiquitin, markiert zu werden, das es zum zellulären Proteinaschenvernichter schicken würde. Ohne Serotonylierung wird GPX4 leichter von einem Enzym namens TRIM25 erkannt, das es für den Abbau markiert. Mit Serotonylierung bleibt GPX4 erhalten, die Membranen sind geschützt und Ferroptose wird unterdrückt.
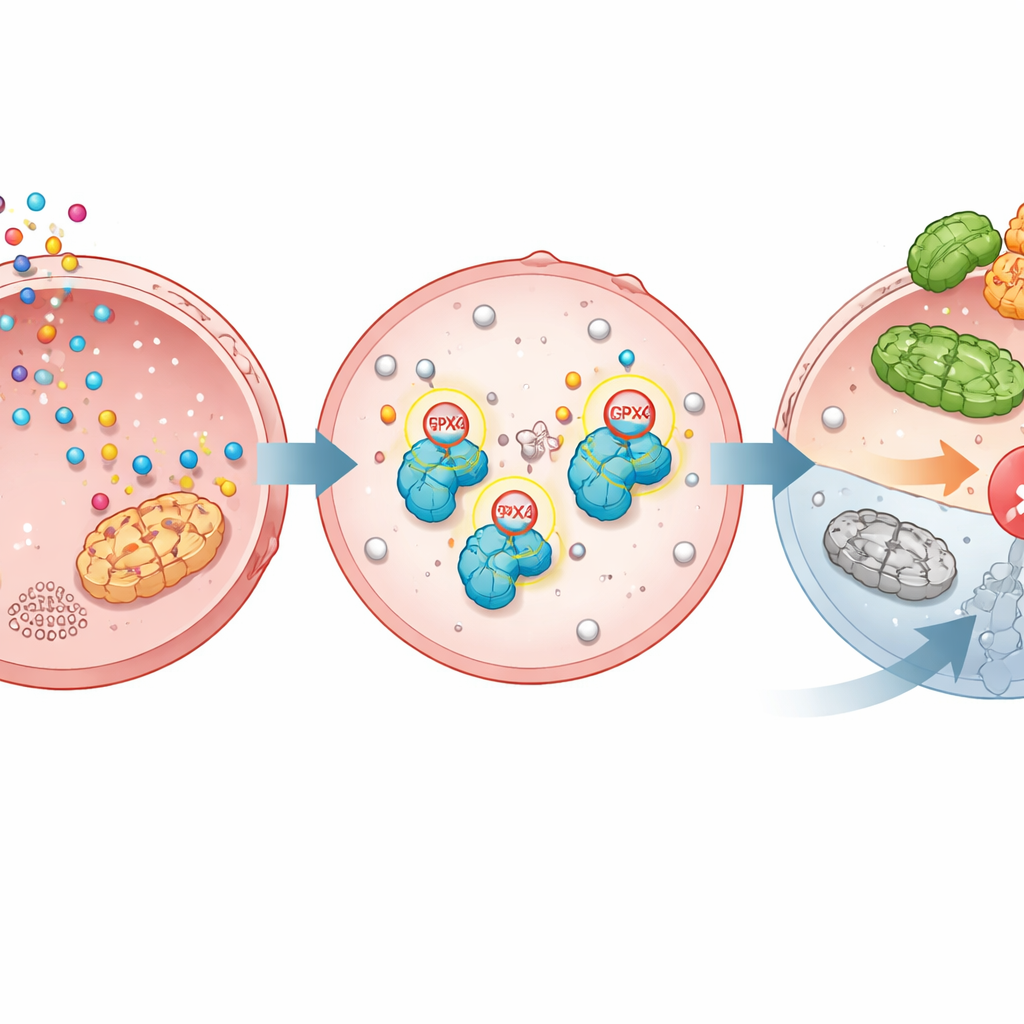
Belege aus gentechnisch veränderten Zellen, Mäusen und Patientenproben
Um die Bedeutung dieser Modifikation zu prüfen, konstruierten die Wissenschaftlerinnen und Wissenschaftler Magenkrebszellen, bei denen GPX4 entfernt und anschließend entweder durch die normale Version oder durch eine Mutante ersetzt wurde, die an den beiden Schlüsselstellen nicht serotonylierbar ist. Serotonin förderte Wachstum und schützte Zellen vor ferroptoseauslösenden Wirkstoffen nur, wenn normales GPX4 vorhanden war, nicht jedoch, wenn die nicht veränderbare Version eingesetzt wurde. In Maus-Tumormodellen beschleunigte die Verabreichung von Serotonin das Wachstum von Tumoren mit normalem GPX4, hatte aber kaum Wirkung auf Tumoren mit der mutierten Form. In Patientendatensätzen und Gewebeproben waren sowohl das Enzym TGM2 als auch GPX4 in Tumoren gegenüber dem angrenzenden normalen Magengewebe erhöht, und höhere Werte eines der beiden waren mit schlechterem Überleben verknüpft — ein Hinweis auf die klinische Relevanz dieses Weges.
Was das für Patientinnen, Patienten und zukünftige Therapien bedeutet
Einfach ausgedrückt zeigt diese Arbeit, dass Magen-Tumoren einen Nervenbotenstoff, der normalerweise mit Stimmung assoziiert wird, kapern können, um sich gegen ein mächtiges Todesprogramm zu wappnen. Indem sie Serotonin direkt an GPX4 anbringen, nutzt der Tumor ein chemisches „Schloss“, das dieses schützende Enzym vor dem Abbau bewahrt und so den Krebszellen erlaubt, Bedingungen zu überleben, die sie eigentlich töten sollten. Diese Entdeckung legt nahe, dass die Messung serotonylierungsabhängiger GPX4-Modifikationen helfen könnte, Hochrisiko-Magenkrebserkrankungen zu identifizieren, und dass Wirkstoffe, die TGM2 hemmen, den Serotonin-Transport in die Zellen blockieren oder die Stabilität von GPX4 beeinträchtigen, die Ferroptose wiederherstellen und Tumoren verwundbarer machen könnten. Kurz gesagt: Die Störung dieses Serotonin–GPX4-Schutzschilds könnte eine neue Strategie zur Behandlung von Magenkrebs werden.
Zitation: Bai, J., Geng, D., Chen, X. et al. TGM2-mediated serotonylation of GPX4 confers ferroptosis resistance to promote gastric tumorigenesis. Cell Discov 12, 30 (2026). https://doi.org/10.1038/s41421-026-00885-6
Schlüsselwörter: Magenkrebs, Serotonin, Ferroptose, GPX4, Proteinmodifikation