Clear Sky Science · fr
La sérotonylation de GPX4 médiée par TGM2 confère une résistance à la ferroptose favorisant la tumorigenèse gastrique
Comment les substances chimiques nerveuses peuvent aider les tumeurs de l’estomac à survivre
La plupart des gens connaissent la sérotonine comme le « messager du bien-être » qui influence l’humeur, mais cette même molécule circule aussi dans l’intestin et le sang. Cette étude révèle que, chez les patients atteints de cancer gastrique, la sérotonine fait bien plus que transmettre des signaux entre cellules nerveuses. Elle peut modifier directement des protéines clés à l’intérieur des cellules tumorales, les aidant à résister à une forme de mort cellulaire et à croître plus agressivement. Comprendre cette chimie cachée entre le système nerveux et les cellules cancéreuses pourrait ouvrir de nouvelles voies pour diagnostiquer et traiter le cancer de l’estomac.
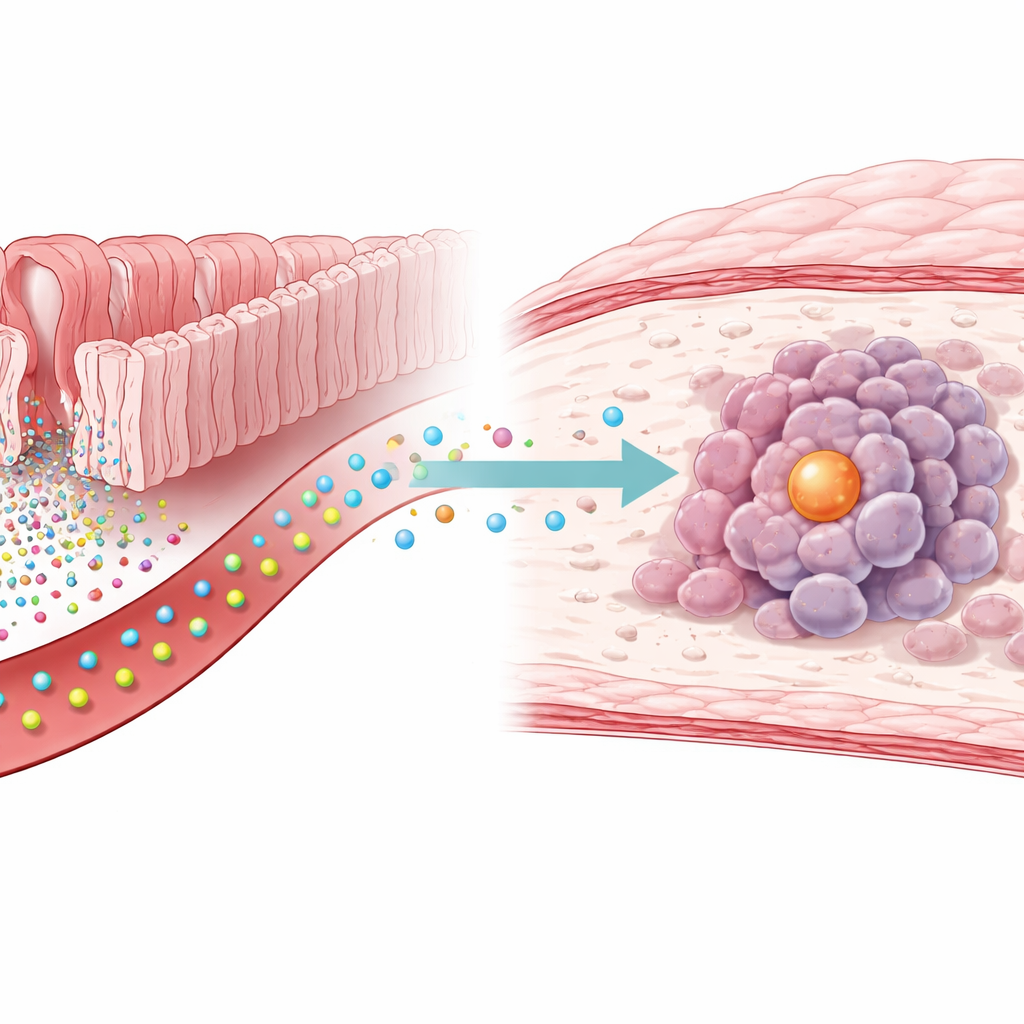
Un lien méconnu entre la chimie intestinale et le cancer gastrique
Les chercheurs ont commencé par mesurer des centaines de petites molécules dans des échantillons de sang de personnes avec ou sans cancer gastrique. Ils ont constaté que les niveaux de sérotonine étaient systématiquement plus élevés chez les patients atteints de cancer. Lorsqu’ils ont ajouté de la sérotonine à des cellules de cancer gastrique cultivées en laboratoire, les cellules se sont multipliées plus rapidement, et les tumeurs ont progressé plus vite chez des souris recevant un apport supplémentaire de sérotonine. Le blocage d’une enzyme particulière appelée TGM2 a annulé cet effet stimulant la tumeur, suggérant que l’influence de la sérotonine ne dépendait pas seulement de ses récepteurs de surface habituels, mais d’une modification chimique plus directe à l’intérieur des cellules.
La sérotonine, étiqueteuse chimique des protéines
La sérotonine peut être attachée de façon covalente aux protéines dans un processus connu sous le nom de « sérotonylation », catalysé par TGM2. Pour identifier quelles protéines étaient marquées de cette manière dans les cellules de cancer gastrique, l’équipe a utilisé une sonde spécialement conçue, semblable à la sérotonine, qui se fixe aux protéines et peut être récupérée puis identifiée par spectrométrie de masse. Ce criblage chimio-protéomique a mis au jour plus de 800 protéines candidates, beaucoup impliquées dans le métabolisme, la réparation de l’ADN et une forme de mort cellulaire pilotée par le fer appelée ferroptose. Parmi elles, une enzyme s’est distinguée : GPX4, un défenseur majeur qui protège les membranes cellulaires contre la destruction par les dommages oxydatifs.
Comment les cellules tumorales bloquent une voie d’autodestruction
La ferroptose est un programme d’autodestruction qui tue les cellules lorsque les lipides des membranes sont fortement oxydés. GPX4 maintient normalement ce processus sous contrôle ; quand GPX4 est perdu ou inactivé, la ferroptose se déclenche et les cellules cancéreuses peuvent mourir. L’étude montre que TGM2 attache chimiquement la sérotonine à GPX4 en deux positions précises. Cette sérotonylation rend GPX4 plus stable, le protégeant de l’étiquetage par une autre molécule, l’ubiquitine, qui enverrait GPX4 vers la broyeuse protéique de la cellule. Sans sérotonylation, GPX4 est plus facilement reconnu par une enzyme appelée TRIM25 qui le marque pour destruction. Avec la sérotonylation, GPX4 persiste, les membranes restent protégées et la ferroptose est contenue.
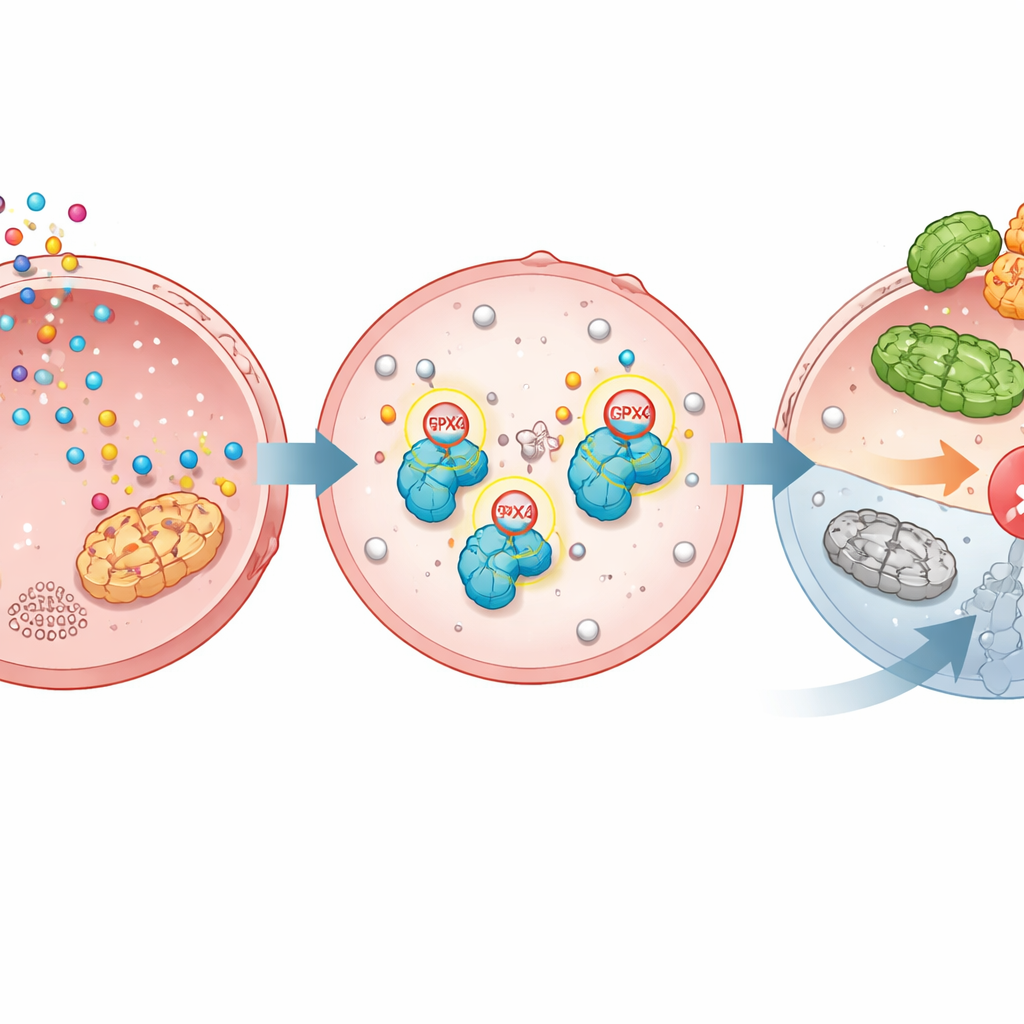
Preuves issues de cellules modifiées, de souris et d’échantillons de patients
Pour tester l’importance cruciale de cette modification, les scientifiques ont modifié des cellules de cancer gastrique dont GPX4 avait été supprimé, puis réintroduit soit la version normale, soit une forme mutante qui ne peut pas être sérotonylée aux deux positions clés. La sérotonine a favorisé la croissance et protégé les cellules des médicaments induisant la ferroptose uniquement lorsque GPX4 normal était présent, pas lorsque la version non modifiable était utilisée. Dans des modèles tumoraux murins, l’administration de sérotonine a accéléré la croissance des tumeurs portant GPX4 normal, mais a eu peu d’effet sur celles exprimant l’enzyme mutante. Dans les jeux de données patients et les échantillons tissulaires, l’enzyme TGM2 et GPX4 étaient tous deux élevés dans les tumeurs comparées au tissu gastrique normal adjacent, et des niveaux plus élevés de l’un ou l’autre étaient associés à une survie plus faible, soulignant l’importance clinique de cette voie.
Ce que cela signifie pour les patients et les thérapies futures
En termes accessibles, ce travail montre que les tumeurs gastriques peuvent détourner une molécule nerveuse habituellement associée à l’humeur pour se protéger contre un puissant programme de mort. En fixant la sérotonine directement sur GPX4, la tumeur utilise une « verrou chimique » qui empêche cette enzyme protectrice d’être dégradée, permettant aux cellules cancéreuses de survivre à des conditions qui devraient les tuer. Cette découverte suggère que mesurer la modification de GPX4 induite par la sérotonine pourrait aider à identifier les cancers gastriques à haut risque et que des médicaments ciblant TGM2, le transport de la sérotonine dans les cellules ou la stabilité de GPX4 pourraient restaurer la ferroptose et rendre les tumeurs plus vulnérables. En bref, perturber ce bouclier sérotonine–GPX4 pourrait devenir une nouvelle stratégie pour traiter le cancer de l’estomac.
Citation: Bai, J., Geng, D., Chen, X. et al. TGM2-mediated serotonylation of GPX4 confers ferroptosis resistance to promote gastric tumorigenesis. Cell Discov 12, 30 (2026). https://doi.org/10.1038/s41421-026-00885-6
Mots-clés: cancer gastrique, sérotonine, ferroptose, GPX4, modification protéique