Clear Sky Science · ru
Серотонилирование GPX4, опосредованное TGM2, обеспечивает устойчивость к ферроптозу и способствует гастрическому опухолеобразованию
Как нервные химические вещества помогают выживанию опухолей в желудке
Большинство людей знают серотонин как «гормон хорошего самочувствия», влияющий на настроение, но эта же молекула также циркулирует в кишечнике и крови. В этом исследовании показано, что у пациентов с раком желудка серотонин делает гораздо больше, чем просто передаёт сигналы между нервными клетками. Он может напрямую изменять ключевые белки внутри опухолевых клеток, помогая им сопротивляться одному из видов гибели клеток и расти более агрессивно. Понимание этой скрытой химии между нервной системой и раковыми клетками может открыть новые пути диагностики и лечения рака желудка.
Скрытая связь между химией кишечника и раком желудка
Исследователи начали с измерения сотен малых молекул в образцах крови людей с раком желудка и без него. Они обнаружили, что у больных уровень серотонина последовательно выше. Когда серотонин добавляли к культурам клеток рака желудка в лаборатории, клетки делились быстрее, а опухоли у мышей при дополнительном введении серотонина росли быстрее. Блокирование особенно важного фермента под названием TGM2 устраняло этот опухолеукрепляющий эффект, что указывает на то, что влияние серотонина не ограничивается только его обычными поверхностными рецепторами, а связано с более прямой химической модификацией внутри клеток.
Серотонин как химическое «ярлыкование» белков
Серотонин может ковалентно присоединяться к белкам в процессе, известном как «серотонилирование», катализируемом TGM2. Чтобы понять, какие белки помечаются таким образом в клетках рака желудка, команда использовала специально разработанный серотониноподобный зонд, который связывается с белками и затем извлекается и идентифицируется методом масс-спектрометрии. Этот хемопротеомный скрининг выявил более 800 кандидатных белков, многие из которых участвуют в метаболизме, репарации ДНК и в типе клеточной гибели, зависящей от железа, называемой ферроптозом. Среди них выделялся один фермент: GPX4, ключевой защитник, который оберегает клеточные мембраны от разрушения окислительным повреждением.
Как опухолевые клетки блокируют программу самоуничтожения
Ферроптоз — это встроенная программа самоуничтожения, которая убивает клетки, когда липиды в их мембранах сильно окисляются. GPX4 обычно держит этот процесс под контролем; при утрате или инактивации GPX4 запускается ферроптоз, и раковые клетки могут погибать. В исследовании показано, что TGM2 химически присоединяет серотонин к GPX4 в двух точных позициях. Это серотонилирование делает GPX4 более стабильным, защищая его от пометки другим молекулой — убиквитином, которая направила бы его в протеасому для разрушения. Без серотонилирования GPX4 легче распознаётся ферментом TRIM25, помечается для уничтожения. При серотонилировании GPX4 сохраняется, мембраны остаются защищёнными, и ферроптоз не наступает.
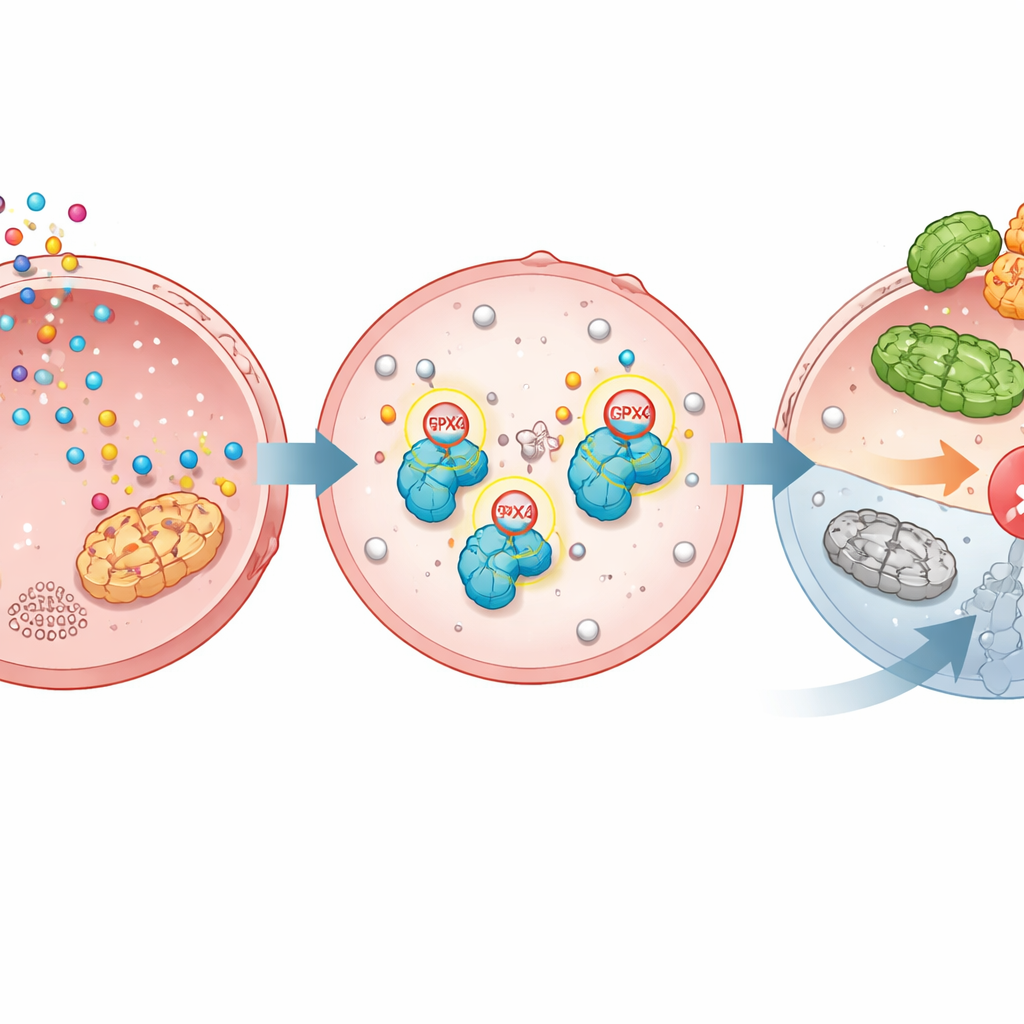
Доказательства от модифицированных клеток, мышей и образцов пациентов
Чтобы проверить важность этой модификации, учёные создали клетки рака желудка, в которых GPX4 удаляли, а затем восстанавливали либо нормальной версией, либо мутантной формой, не способной на серотонилирование в двух ключевых позициях. Серотонин стимулировал рост и защищал клетки от препаратов, индуцирующих ферроптоз, только при наличии нормального GPX4, но не при использовании немодифицируемой версии. В мышиных опухолевых моделях введение серотонина ускоряло рост опухолей с нормальным GPX4, но мало влияло на опухоли с мутантным ферментом. В наборах клинических данных и тканевых образцах ферменты TGM2 и GPX4 оба были повышены в опухолях по сравнению с рядом нормальной ткани желудка, а более высокие уровни любого из них связывались с худшим выживанием, что подчёркивает клиническое значение этого пути.
Что это значит для пациентов и будущих терапий
Проще говоря, эта работа показывает, что опухоли желудка могут присвоить себе нервный химикат, обычно ассоциируемый с настроением, чтобы укрепить собственную защиту против мощной программы гибели. Присоединяя серотонин напрямую к GPX4, опухоль использует химический «замок», который препятствует разрушению этого защитного фермента, позволяя раковым клеткам выживать в условиях, при которых они должны погибнуть. Это открытие предполагает, что измерение серотонин-опосредованной модификации GPX4 может помочь идентифицировать высокорисковые случаи рака желудка, а препараты, нацеленные на TGM2, транспорт серотонина в клетки или стабильность GPX4, могли бы восстановить ферроптоз и сделать опухоли уязвимее. Иными словами, разрушение этого защитного щита серотонин–GPX4 может стать новой стратегией лечения рака желудка.
Цитирование: Bai, J., Geng, D., Chen, X. et al. TGM2-mediated serotonylation of GPX4 confers ferroptosis resistance to promote gastric tumorigenesis. Cell Discov 12, 30 (2026). https://doi.org/10.1038/s41421-026-00885-6
Ключевые слова: рак желудка, серотонин, ферроптоз, GPX4, модификация белков