Clear Sky Science · sv
TGM2-medierad serotonylation av GPX4 ger ferroptosresistens och främjar magsakturorer
Hur nervkemikalier kan hjälpa magtumörer att överleva
De flesta känner till serotonin som det ”må-bra”-ämne som påverkar humöret, men samma molekyl cirkulerar också i tarmen och i blodet. Denna studie visar att hos patienter med magsäckscancer gör serotonin mycket mer än att bara skicka signaler mellan nervceller. Den kan direkt förändra nyckelproteiner inne i tumörceller, vilket hjälper dem att motstå en form av celldöd och växa mer aggressivt. Att förstå denna dolda kemi mellan nervsystemet och cancerceller kan öppna nya vägar för diagnostik och behandling av magsäckscancer.
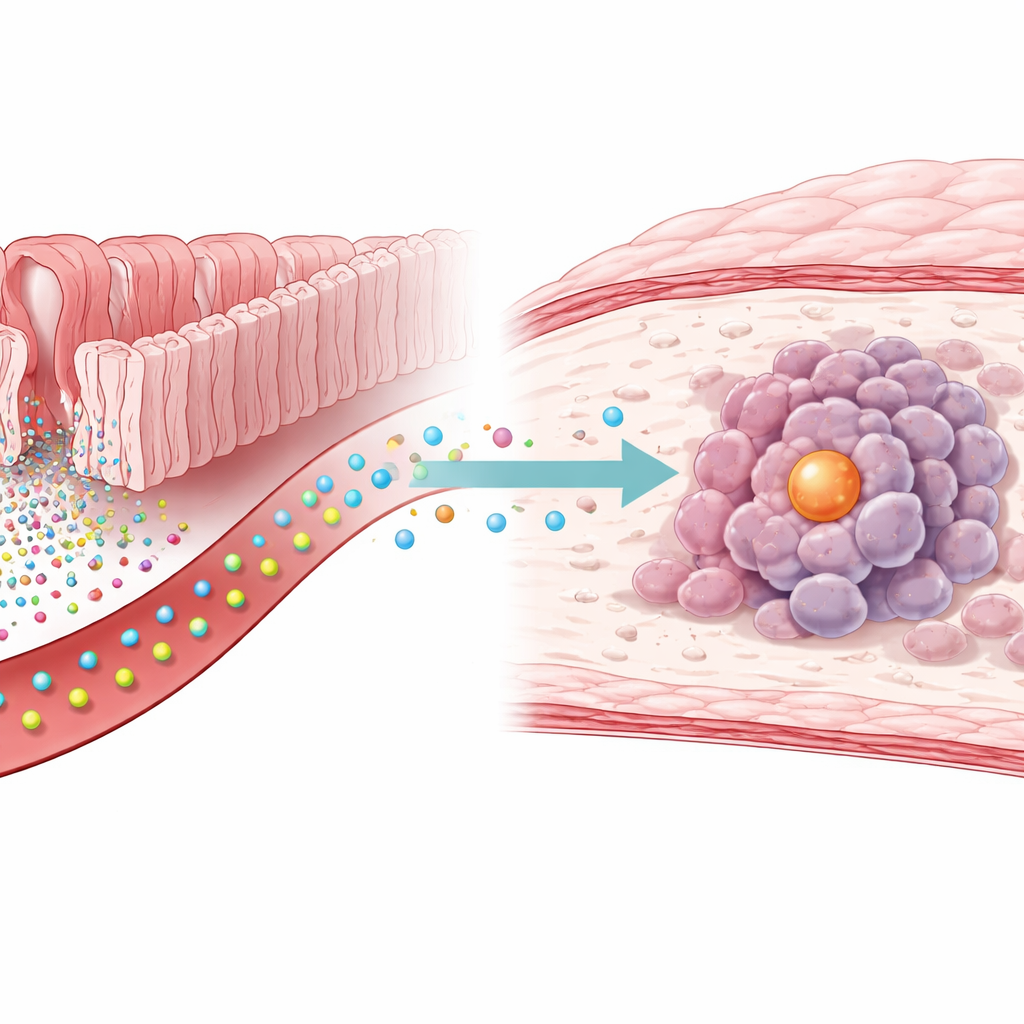
En dold koppling mellan tarmkemi och magsäckscancer
Forskarna började med att mäta hundratals små molekyler i blodprover från personer med och utan magsäckscancer. De fann att serotoninnivåerna konsekvent var högre hos patienter med cancer. När de tillsatte serotonin till magsäckscancerceller odlade i labbet delade cellerna snabbare, och tumörer växte snabbare hos möss som fick extra serotonin. Blockering av ett visst enzym kallat TGM2 utplånade denna tumörfrämjande effekt, vilket antyder att serotonins påverkan inte bara beror på dess vanliga ytreceptorer, utan på en mer direkt kemisk modifiering inne i cellerna.
Serotonin som ett proteinmärkande ämne
Serotonin kan kovalent fästas på proteiner i en process som kallas ”serotonylation”, katalyserad av TGM2. För att se vilka proteiner som märktes på detta sätt i magsäckscancerceller använde teamet en specialdesignad serotoninliknande probe som fäster på proteiner och kan fiskas upp och identifieras med masspektrometri. Detta kemoproteomiska urval avslöjade mer än 800 kandidatproteiner, många involverade i ämnesomsättning, DNA-reparation och en typ av järndriven celldöd kallad ferroptos. Bland dessa utmärkte sig ett enzym: GPX4, en central försvarare som skyddar cellmembran från att förstöras av oxidativ skada.
Hur tumörceller blockerar en självdödsväg
Ferroptos är ett inbyggt självdödsprogram som dödar celler när fettsyror i deras membran blir kraftigt oxiderade. GPX4 håller normalt detta i schack; när GPX4 förloras eller inaktiveras utlöses ferroptos och cancerceller kan dö. Studien visar att TGM2 kemiskt fäster serotonin på GPX4 vid två precisa positioner. Denna serotonylation gör GPX4 mer stabilt och skyddar det från att märkas med ett annat molekylärt märke, ubiquitin, som skulle skicka det till cellens proteinnedbrytningssystem. Utan serotonylation känns GPX4 lättare igen av ett enzym kallat TRIM25 som markerar det för nedbrytning. Med serotonylation kvarstår GPX4, membranen förblir skyddade och ferroptos hålls tillbaka.
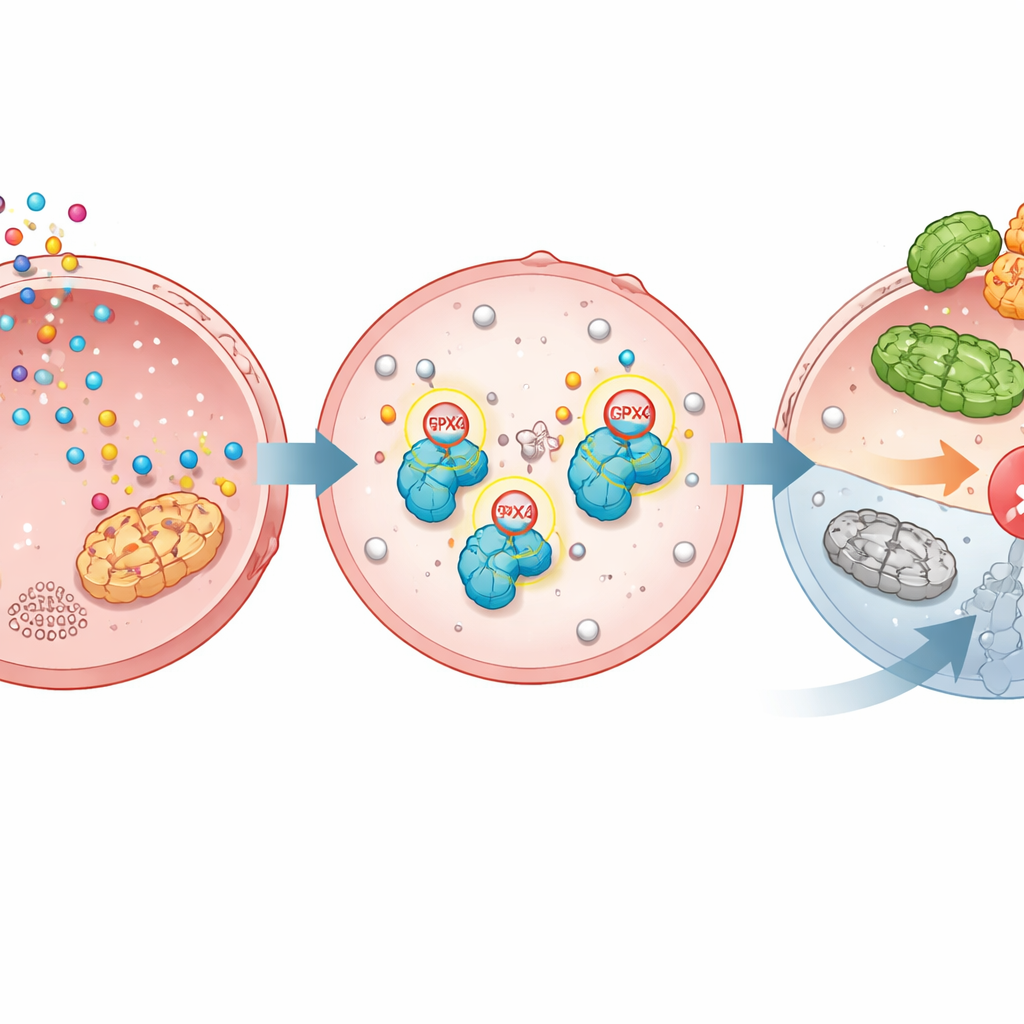
Bevis från manipulerade celler, möss och patientprover
För att testa hur avgörande denna modifiering är konstruerade forskarna magsäckscancerceller där GPX4 togs bort och sedan ersattes antingen med den normala versionen eller med en muterad form som inte kan serotonylas vid de två nyckelpositionerna. Serotonin ökade tillväxt och skyddade cellerna från ferroptosinducerande läkemedel endast när normal GPX4 fanns närvarande, inte när den icke-modifierbara varianten användes. I musemodeller för tumörer gav tillförsel av serotonin snabbare tillväxt av tumörer med normal GPX4, men hade liten effekt på tumörer med den muterade formen. I patientdatamängder och vävnadsprover var både enzymet TGM2 och GPX4 förhöjda i tumörer jämfört med intilliggande normal magsäcksvävnad, och högre nivåer av endera var kopplade till sämre överlevnad, vilket understryker vägledningens kliniska betydelse.
Vad detta betyder för patienter och framtida terapier
Enkelt uttryckt visar arbetet att magsäckstumörer kan kapra en nervkemikal som vanligtvis associeras med humör för att bepansra sig mot ett kraftfullt dödsprogram. Genom att fästa serotonin direkt på GPX4 använder tumören ett kemiskt ”lås” som hindrar detta skyddande enzym från att brytas ner, vilket gör att cancerceller kan överleva förhållanden som annars skulle döda dem. Denna upptäckt tyder på att mätning av serotonindriven GPX4-modifiering kan hjälpa till att identifiera högrisk-magsäckscancer och att läkemedel som riktar sig mot TGM2, serotonintransport in i celler eller GPX4-stabilitet kan återställa ferroptos och göra tumörer mer sårbara. Kort sagt, att störa detta serotonin–GPX4-säkerhetsskalsystem kan bli en ny strategi för att behandla magsäckscancer.
Citering: Bai, J., Geng, D., Chen, X. et al. TGM2-mediated serotonylation of GPX4 confers ferroptosis resistance to promote gastric tumorigenesis. Cell Discov 12, 30 (2026). https://doi.org/10.1038/s41421-026-00885-6
Nyckelord: magcancer, serotonin, ferroptos, GPX4, proteinmodifiering