Clear Sky Science · pt
TGM2-mediada serotonilação de GPX4 confere resistência à ferroptose e promove a tumorogênese gástrica
Como os químicos nervosos podem ajudar tumores do estômago a sobreviver
A maioria das pessoas conhece a serotonina como o químico “do bem-estar” que afeta o humor, mas essa mesma molécula também circula no intestino e no sangue. Este estudo revela que, em pacientes com câncer gástrico, a serotonina faz muito mais do que transmitir sinais entre neurônios. Ela pode alterar diretamente proteínas-chave dentro das células tumorais, ajudando-as a resistir a uma forma de morte celular e a crescer de maneira mais agressiva. Compreender essa química oculta entre o sistema nervoso e as células cancerosas pode abrir novas vias para diagnosticar e tratar o câncer de estômago.
Um elo oculto entre a química intestinal e o câncer de estômago
Os pesquisadores começaram medindo centenas de pequenas moléculas em amostras de sangue de pessoas com e sem câncer gástrico. Eles descobriram que os níveis de serotonina eram consistentemente maiores em pacientes com câncer. Quando adicionaram serotonina a células de câncer gástrico cultivadas em laboratório, as células se multiplicaram mais rapidamente, e tumores cresceram mais depressa em camundongos que receberam serotonina extra. Bloquear uma enzima específica chamada TGM2 apagou esse efeito de aumento tumoral, sugerindo que a influência da serotonina não dependia apenas de seus receptores de superfície usuais, mas de uma modificação química mais direta dentro das células.
Serotonina como um químico que marca proteínas
A serotonina pode ser ligada covalentemente a proteínas em um processo conhecido como “serotonilação”, catalisado pela TGM2. Para ver quais proteínas eram marcadas dessa forma em células de câncer gástrico, a equipe usou uma sonda especialmente projetada, semelhante à serotonina, que se liga às proteínas e pode ser isolada e identificada por espectrometria de massa. Essa triagem químico-proteômica revelou mais de 800 proteínas candidatas, muitas envolvidas no metabolismo, reparo de DNA e em um tipo de morte celular dirigida pelo ferro chamado ferroptose. Entre elas, uma enzima se destacou: GPX4, um defensor principal que protege as membranas celulares contra destruição por dano oxidativo.
Como células tumorais bloqueiam um caminho de autodestruição
A ferroptose é um programa de autodestruição embutido que mata células quando moléculas de gordura nas membranas ficam fortemente oxidadas. O GPX4 normalmente mantém isso sob controle; quando o GPX4 é perdido ou desativado, a ferroptose é desencadeada e as células cancerosas podem morrer. O estudo mostra que a TGM2 liga quimicamente a serotonina ao GPX4 em dois pontos precisos. Essa serotonilação torna o GPX4 mais estável, protegendo-o de ser marcado com outra molécula, a ubiquitina, que o enviaria para o triturador de proteínas da célula. Sem serotonilação, o GPX4 é mais facilmente reconhecido por uma enzima chamada TRIM25, que o sinaliza para destruição. Com a serotonilação, o GPX4 persiste, as membranas permanecem protegidas e a ferroptose é contida.
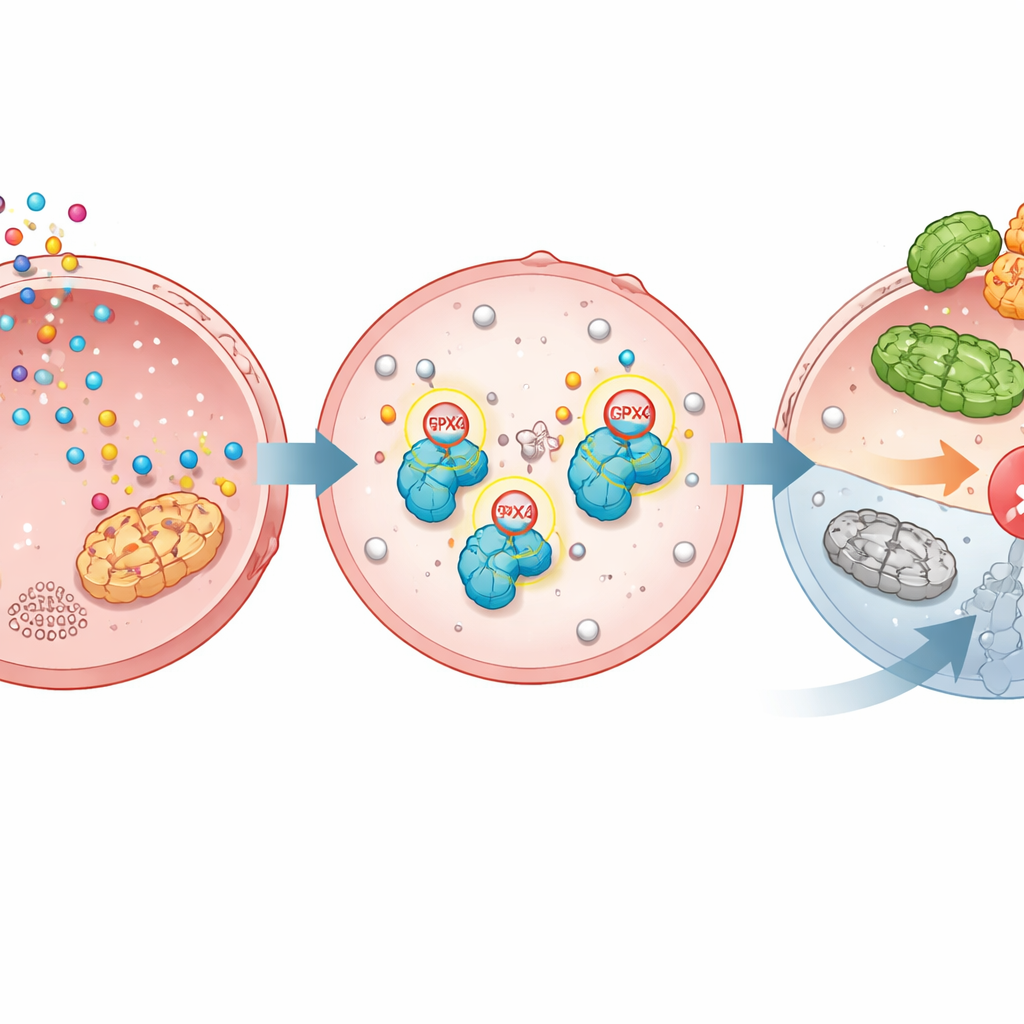
Provas a partir de células geneticamente modificadas, camundongos e amostras de pacientes
Para testar o quão crucial é essa modificação, os cientistas criaram células de câncer gástrico nas quais o GPX4 foi removido e então substituído pela versão normal ou por uma forma mutante que não pode ser serotonilada nos dois pontos-chave. A serotonina impulsionou o crescimento e protegeu as células de drogas que induzem ferroptose somente quando o GPX4 normal estava presente, não quando a versão não modificável era usada. Em modelos tumorais de camundongos, administrar serotonina acelerou o crescimento de tumores que carregavam o GPX4 normal, mas teve pouco efeito em tumores com a enzima mutante. Em conjuntos de dados de pacientes e amostras de tecido, a enzima TGM2 e o GPX4 estavam ambos elevados nos tumores em comparação com o tecido gástrico normal adjacente, e níveis maiores de qualquer um deles foram associados a pior sobrevida, ressaltando a importância clínica dessa via.
O que isso significa para pacientes e terapias futuras
Em termos acessíveis, este trabalho mostra que tumores do estômago podem sequestrar um químico nervoso usualmente associado ao humor para se blindar contra um poderoso programa de morte. Ao ligar a serotonina diretamente ao GPX4, o tumor usa uma “trava” química que impede que essa enzima protetora seja degradada, permitindo que as células cancerosas sobrevivam a condições que deveriam matá-las. Essa descoberta sugere que medir a modificação de GPX4 induzida pela serotonina pode ajudar a identificar cânceres gástricos de alto risco e que medicamentos que atinjam a TGM2, o transporte de serotonina para dentro das células ou a estabilidade do GPX4 poderiam restaurar a ferroptose e tornar os tumores mais vulneráveis. Em suma, romper esse escudo serotonina–GPX4 pode se tornar uma nova estratégia para tratar o câncer de estômago.
Citação: Bai, J., Geng, D., Chen, X. et al. TGM2-mediated serotonylation of GPX4 confers ferroptosis resistance to promote gastric tumorigenesis. Cell Discov 12, 30 (2026). https://doi.org/10.1038/s41421-026-00885-6
Palavras-chave: câncer gástrico, serotonina, ferroptose, GPX4, modificação de proteína