Clear Sky Science · ar
التسورتينيلة بوساطة TGM2 لبروتين GPX4 تمنح مقاومة للفروبتوز وتساعد على تكون الأورام المعدية
كيف تساعد مواد عصبية الأورام المعدية على البقاء
يعرف معظم الناس السيروتونين على أنه «المادة المسببة للشعور الجيد» التي تؤثر على المزاج، لكن هذه الجزيئة نفسها تدور أيضاً في الأمعاء والدم. تكشف هذه الدراسة أنه عند مرضى سرطان المعدة، يقوم السيروتونين بأكثر من إرسال إشارات بين الخلايا العصبية. يمكنه تعديل بروتينات رئيسية داخل خلايا الورم مباشرةً، مما يساعدها على مقاومة شكل من أشكال موت الخلايا والنمو بشكل أكثر عدوانية. قد يفتح فهم هذه الكيمياء الخفية بين الجهاز العصبي وخلايا السرطان طرقاً جديدة لتشخيص وعلاج سرطان المعدة.
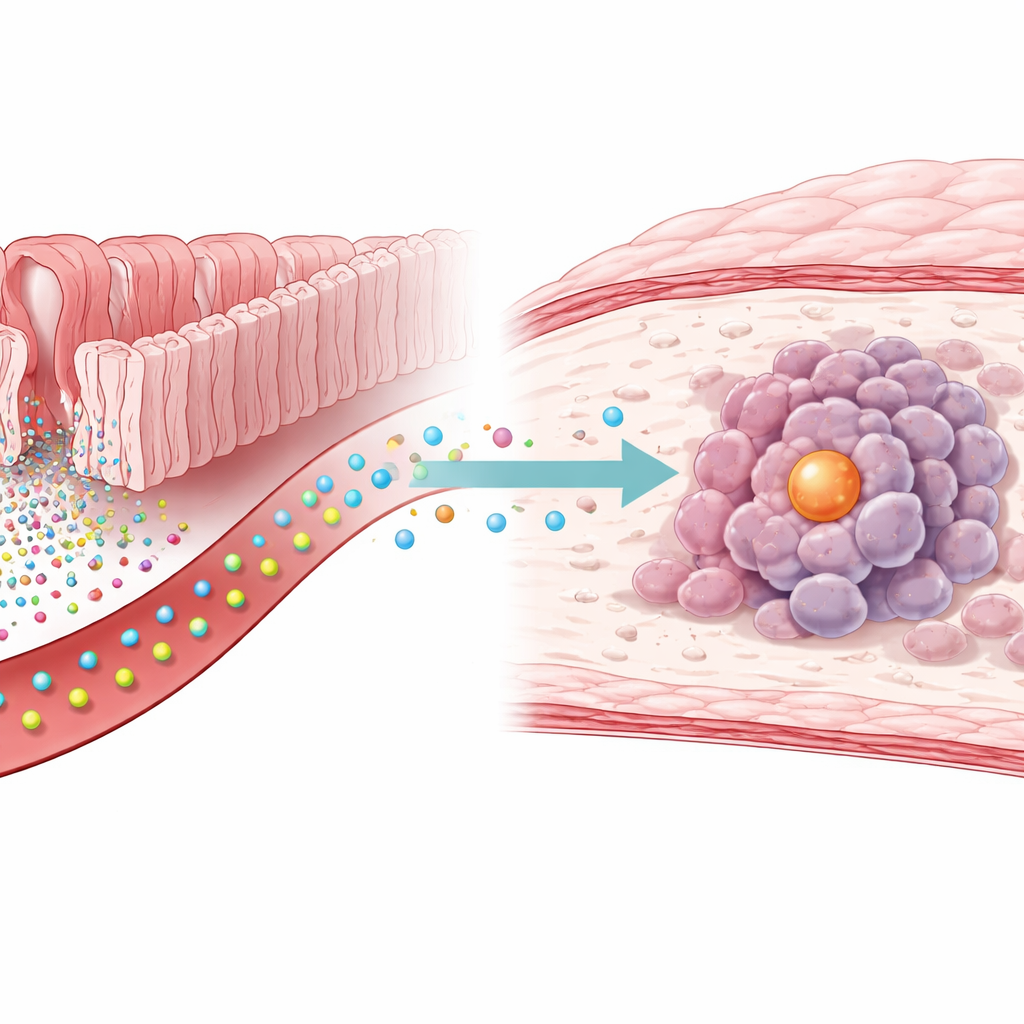
رابط خفي بين كيمياء الأمعاء وسرطان المعدة
بدأ الباحثون بقياس مئات الجزيئات الصغيرة في عينات دم أشخاص مصابين وغير مصابين بسرطان المعدة. وجدوا أن مستويات السيروتونين كانت أعلى باستمرار لدى المرضى المصابين بالسرطان. عندما أضافوا السيروتونين إلى خلايا سرطان المعدة المزروعة في المختبر، زاد تكاثر الخلايا، ونمت الأورام أسرع في الفئران التي أعطيت لها كمية إضافية من السيروتونين. إيقاف إنزيم محدد يُدعى TGM2 ألغى هذا التأثير المعزز للورم، مما يوحي بأن تأثير السيروتونين لم يقتصر على مستقبلاته السطحية المعتادة، بل شمل تعديلًا كيميائياً مباشراً داخل الخلايا.
السيروتونين كمادة وسمية للبروتينات
يمكن ربط السيروتونين تساهمياً بالبروتينات في عملية تعرف باسم «التسورتينلة»، والتي يحفزها إنزيم TGM2. لرصد أي البروتينات تُوسم بهذه الطريقة في خلايا سرطان المعدة، استخدم الفريق مسباراً شبيهاً بالسيروتونين يمكنه الالتصاق بالبروتينات وسحبه وتحديده بواسطة مطيافية الكتلة. كشفت هذه الشاشة الكيميائية-البروتينية عن أكثر من 800 بروتين مرشح، العديد منها يشارك في الأيض وإصلاح الحمض النووي ونوع من موت الخلايا المعتمد على الحديد يُسمى الفروبتوز. من بين هذه البروتينات، برز إنزيم واحد: GPX4، المدافع الرئيسي الذي يحمي أغشية الخلايا من التحلل الناتج عن الأكسدة.
كيف تمنع خلايا الورم مسار الانتحار الذاتي
الفروبتوز هو برنامج انتحار مدمج يقتل الخلايا عندما تتأكسد جزيئات الدهون في أغشيتها بشكل كبير. عادة ما يكبح GPX4 هذا المسار؛ عندما يفقد GPX4 أو يتعطل، يُثار الفروبتوز وقد تموت الخلايا السرطانية. تظهر الدراسة أن TGM2 يربط السيروتونين كيميائياً بـGPX4 في موقعين محددين. تجعل هذه التسورتينلة GPX4 أكثر استقراراً، فتقيه من أن يُوسم بمركب آخر يُدعى اليوبكويتين الذي يرسله إلى آلة تحطيم البروتينات داخل الخلية. بدون التسورتينلة، يصبح GPX4 أكثر عرضة للتعرف عليه من قبل إنزيم يُدعى TRIM25 يقوم بوضع علامة لتدميره. بوجود التسورتينلة، يبقى GPX4 مستمراً، وتحافظ الأغشية على حمايتها، ويُكبح الفروبتوز.
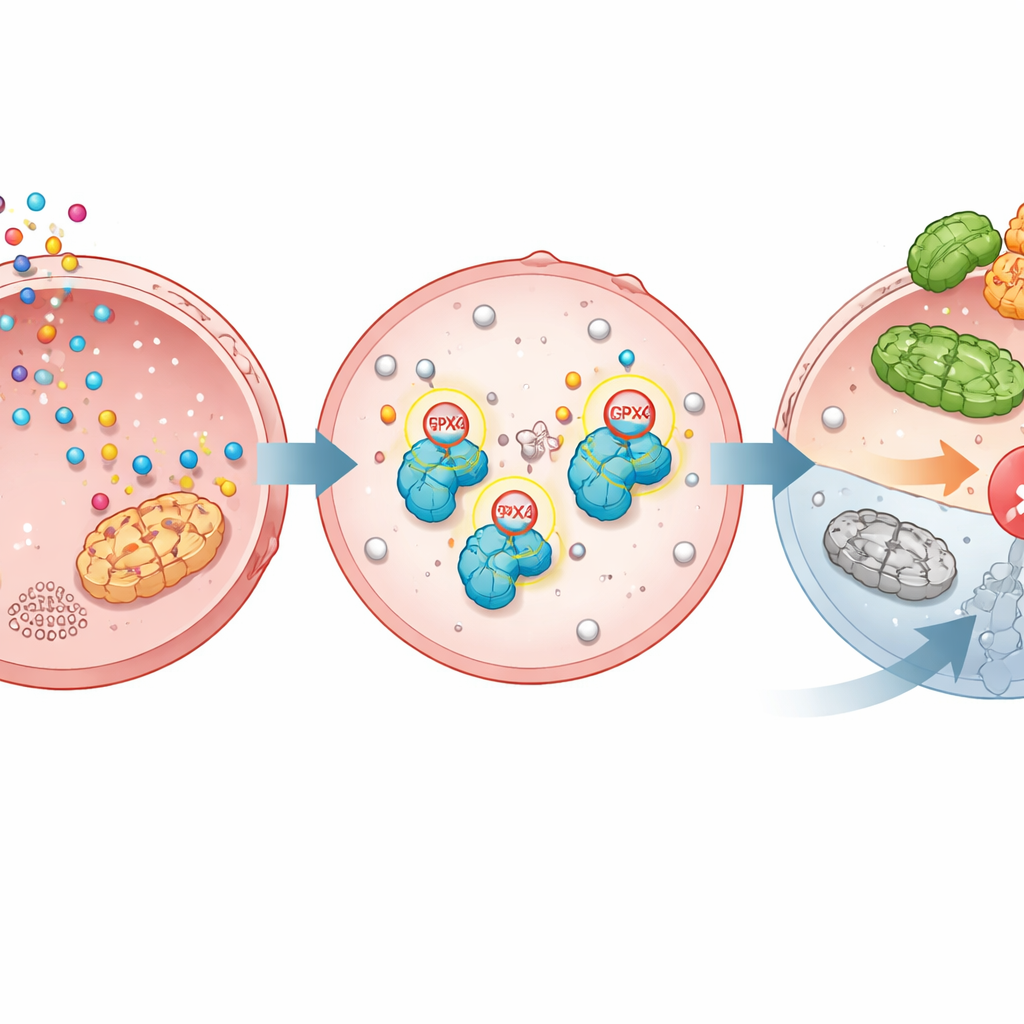
دليل من خلايا مهندسة وفئران وعينات مرضى
لاختبار أهمية هذا التعديل، هندس العلماء خلايا سرطان معدة أُزيل منها GPX4 ثم أُعيد إدخالها إما بالإصدار الطبيعي أو بشكل طفري لا يمكن تسورتينلته في الموقعين الرئيسيين. عزز السيروتونين النمو وحمى الخلايا من الأدوية المحفزة للفروبتوز فقط عندما كان GPX4 الطبيعي موجوداً، وليس عندما استُخدم الشكل غير القابل للتعديل. في نماذج أورام الفئران، سرّع إعطاء السيروتونين نمو الأورام الحاملة لـGPX4 الطبيعي، لكن كان له تأثير ضئيل على الأورام التي تحوي الإنزيم الطفري. في مجموعات بيانات وعينات الأنسجة للمرضى، كانت مستويات كل من إنزيم TGM2 وGPX4 مرتفعة في الأورام مقارنةً بأنسجة المعدة السليمة المجاورة، وكانت المستويات الأعلى لأي منهما مرتبطة ببقاء أسوأ، مما يؤكد الأهمية السريرية لهذا المسار.
ما معنى هذا للمرضى والعلاجات المستقبلية
بعبارات مبسطة، تظهر هذه الدراسة أن أورام المعدة قادرة على استغلال مادة عصبية عادةً ما ترتبط بالمزاج لتدريع نفسها ضد برنامج موت قوي. من خلال ربط السيروتونين مباشرةً بـGPX4، تستخدم الخلايا الورمية «قفلًا» كيميائياً يمنع تحلل هذا الإنزيم الحامي، مما يتيح للخلايا السرطانية البقاء في ظروف كان ينبغي أن تقتلها. تشير هذه الاكتشافات إلى أن قياس تعديل GPX4 المحفز بالسيروتونين قد يساعد في التعرف على سرطانات معدة عالية الخطورة، وأن أدوية تستهدف TGM2 أو نقل السيروتونين إلى داخل الخلايا أو استقرار GPX4 قد تستعيد الفروبتوز وتجعل الأورام أكثر عرضة للعلاج. باختصار، قد يصبح تعطيل درع السيروتونين–GPX4 استراتيجية جديدة لعلاج سرطان المعدة.
الاستشهاد: Bai, J., Geng, D., Chen, X. et al. TGM2-mediated serotonylation of GPX4 confers ferroptosis resistance to promote gastric tumorigenesis. Cell Discov 12, 30 (2026). https://doi.org/10.1038/s41421-026-00885-6
الكلمات المفتاحية: سرطان المعدة, السيروتونين, الفروبتوز, GPX4, تعديل البروتين