Clear Sky Science · pl
TGM2-pośredniczona serotoninylacja GPX4 nadaje oporność na ferroptozę i sprzyja nowotworzeniu żołądka
Jak substancje nerwowe pomagają przetrwać nowotworom żołądka
Większość osób zna serotoninę jako „hormon dobrego samopoczucia” wpływający na nastrój, ale ta sama cząsteczka krąży także w jelitach i we krwi. Badanie ujawnia, że u pacjentów z rakiem żołądka serotonina pełni znacznie więcej ról niż przekazywanie sygnałów między komórkami nerwowymi. Może ona bezpośrednio modyfikować kluczowe białka wewnątrz komórek nowotworowych, pomagając im opierać się pewnemu typowi śmierci komórki i rosnąć bardziej agresywnie. Zrozumienie tej ukrytej chemii między układem nerwowym a komórkami nowotworowymi może otworzyć nowe drogi diagnostyki i terapii raka żołądka.
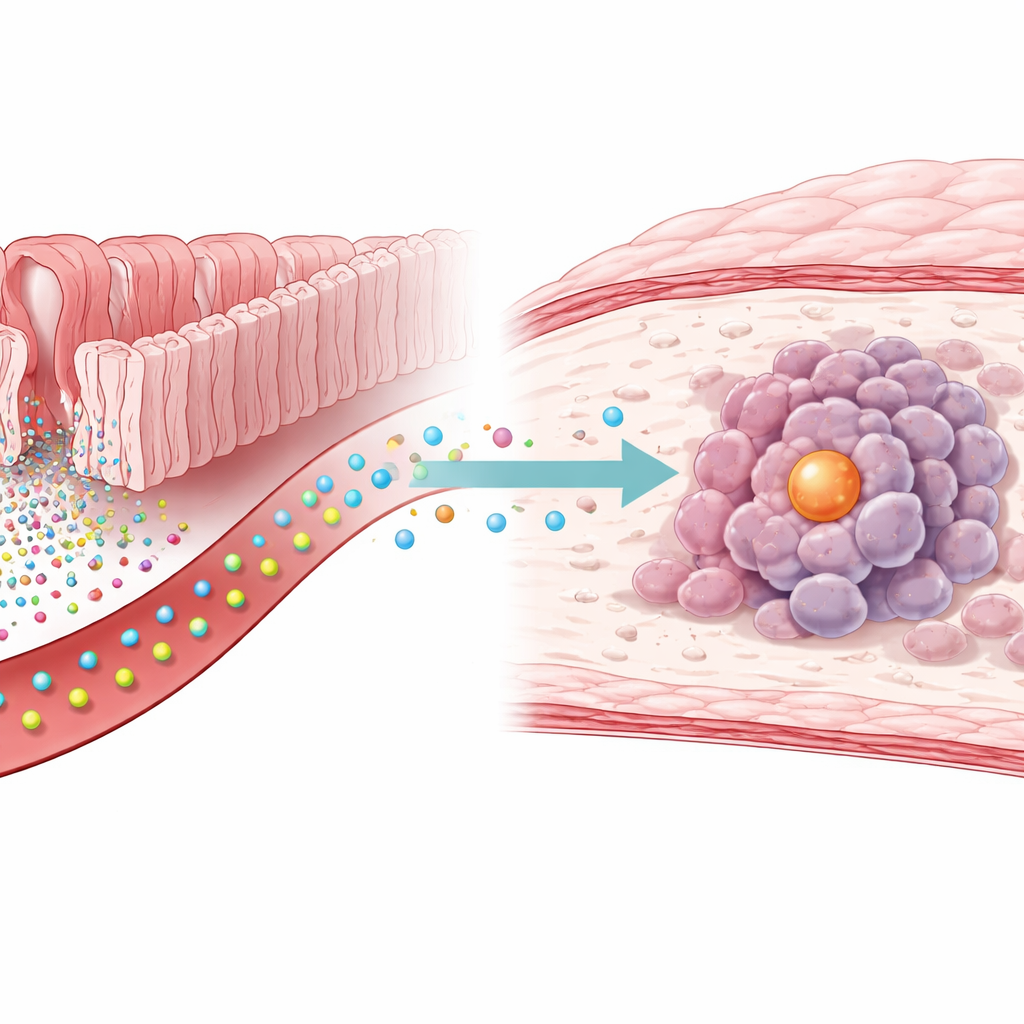
Ukryte powiązanie między chemią jelit a rakiem żołądka
Naukowcy zaczęli od pomiaru setek małych cząsteczek we krwi osób z rakiem żołądka i bez. Stwierdzili, że poziomy serotoniny były konsekwentnie wyższe u pacjentów z nowotworem. Gdy dodawano serotoninę do hodowanych w laboratorium komórek raka żołądka, komórki te mnożyły się szybciej, a guzy rosły szybciej u myszy otrzymujących dodatkową serotoninę. Zablokowanie pewnego enzymu nazwanego TGM2 znosiło ten efekt wzmacniający nowotwór, co sugeruje, że wpływ serotoniny nie zależał wyłącznie od jej zwykłych receptorów powierzchniowych, lecz także od bardziej bezpośredniej modyfikacji chemicznej wewnątrz komórek.
Serotonina jako chemiczny znacznik białek
Serotonina może być kowalencyjnie przyłączana do białek w procesie zwanym „serotonylacją”, katalizowanym przez TGM2. Aby ustalić, które białka są w ten sposób znakowane w komórkach raka żołądka, zespół użył specjalnie zaprojektowanego sondy przypominającej serotoninę, która przyłącza się do białek i może być wychwycona oraz zidentyfikowana przez spektrometrię mas. To chemoproteomiczne przesiewanie ujawniło ponad 800 kandydatów, wielu z nich zaangażowanych w metabolizm, naprawę DNA oraz w rodzaj ferroptozy napędzanej żelazem. Wśród nich wyróżnił się jeden enzym: GPX4, kluczowy obrońca chroniący błony komórkowe przed zniszczeniem wskutek uszkodzeń oksydacyjnych.
Jak komórki nowotworowe blokują mechanizm samozniszczenia
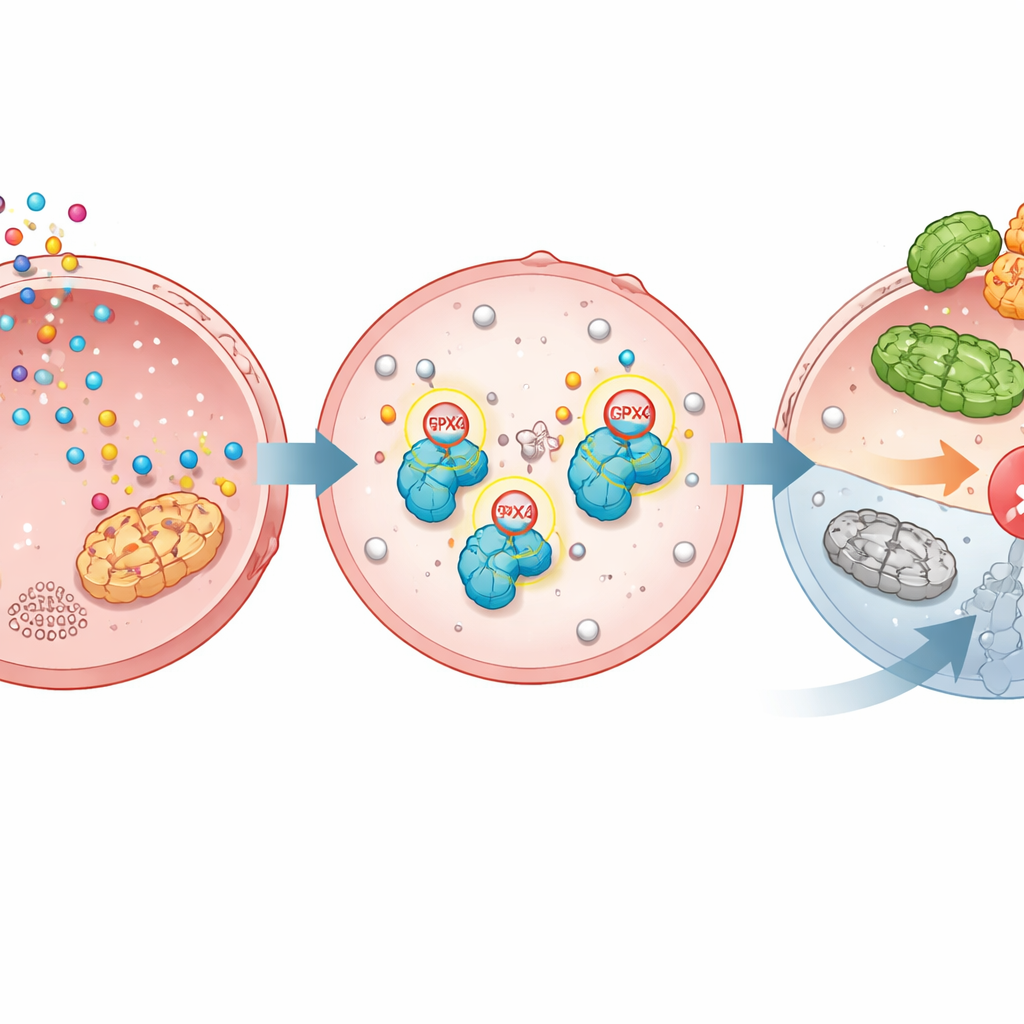
Ferroptoza to wrodzony program samozniszczenia, który zabija komórki, gdy lipidy w ich błonach ulegają silnej oksydacji. GPX4 zwykle to kontroluje; utrata lub wyłączenie GPX4 uruchamia ferroptozę i może prowadzić do śmierci komórek nowotworowych. Badanie pokazuje, że TGM2 chemicznie przyłącza serotoninę do GPX4 w dwóch precyzyjnych miejscach. Ta serotoninylacja stabilizuje GPX4, chroniąc go przed znakowaniem inną cząsteczką, ubikwityną, która skierowałaby go do komórkowego „niszczarki” białek. Bez serotoninylacji GPX4 łatwiej rozpoznaje enzym TRIM25, który oznacza go do zniszczenia. Dzięki serotoninylacji GPX4 utrzymuje się dłużej, błony pozostają chronione, a ferroptoza jest powstrzymana.
Dowody z komórek inżynierowanych, myszy i próbek pacjentów
Aby sprawdzić, jak istotna jest ta modyfikacja, naukowcy skonstruowali komórki raka żołądka, w których GPX4 usunięto, a następnie wprowadzono z powrotem albo w postaci normalnej, albo jako mutant, którego nie można serotoninylować w tych dwóch kluczowych miejscach. Serotonina zwiększała wzrost i chroniła komórki przed lekami wywołującymi ferroptozę tylko wtedy, gdy obecne było normalne GPX4, nie zaś gdy użyto niemodyfikowalnej wersji. W modelach mysich podawanie serotoniny przyspieszało wzrost guzów z normalnym GPX4, ale miało niewielki wpływ na guzy z enzymem-mutantem. W zbiorach danych pacjentów i próbkach tkankowych enzym TGM2 i GPX4 występowały w guzach na wyższym poziomie w porównaniu z sąsiednią zdrową tkanką żołądka, a wyższe poziomy któregokolwiek z nich wiązały się z gorszym przeżyciem, co podkreśla kliniczne znaczenie tej ścieżki.
Co to oznacza dla pacjentów i przyszłych terapii
Mówiąc prosto, praca ta pokazuje, że guzy żołądka potrafią zawłaszczyć chemiczny sygnał nerwowy zwykle kojarzony z nastrojem, aby opancerzyć się przeciw potężnemu programowi śmierci. Poprzez bezpośrednie przyłączenie serotoniny do GPX4 nowotwór stosuje chemiczny „zamek”, który chroni ten ochronny enzym przed rozkładem, pozwalając komórkom rakowym przetrwać warunki, które powinny je zabić. Odkrycie sugeruje, że mierzenie modyfikacji GPX4 zależnej od serotoniny mogłoby pomóc zidentyfikować nowotwory żołądka wysokiego ryzyka, a leki celujące w TGM2, transport serotoniny do komórek lub stabilność GPX4 mogłyby przywrócić ferroptozę i uczynić guzy bardziej podatnymi. Krótko mówiąc, zakłócenie tej ochronnej tarczy serotonin–GPX4 może stać się nową strategią leczenia raka żołądka.
Cytowanie: Bai, J., Geng, D., Chen, X. et al. TGM2-mediated serotonylation of GPX4 confers ferroptosis resistance to promote gastric tumorigenesis. Cell Discov 12, 30 (2026). https://doi.org/10.1038/s41421-026-00885-6
Słowa kluczowe: rak żołądka, serotonina, ferroptoza, GPX4, modyfikacja białek