Clear Sky Science · zh
在生理条件下AMPK对足细胞和肾小球功能并非必需,但在实验性糖尿病中可防止肾小球纤维化
为什么肾脏滤过细胞在糖尿病中很重要
我们的肾脏每天静静地过滤血液数千次,其中滤过结构的关键部分由称为足细胞的细胞构成。这些细胞包裹在称为肾小球的微小血管周围,既将蛋白质留在血液中,又允许废物和水分进入尿液。本研究提出了一个表面上看似简单但对糖尿病患者影响重大的问题:细胞中的一个主要能量感应开关AMPK是否真正保护这些滤过细胞并防止肾脏瘢痕形成?答案有些微妙——AMPK对日常肾功能并非必需,但在糖尿病给系统带来压力时变得至关重要。
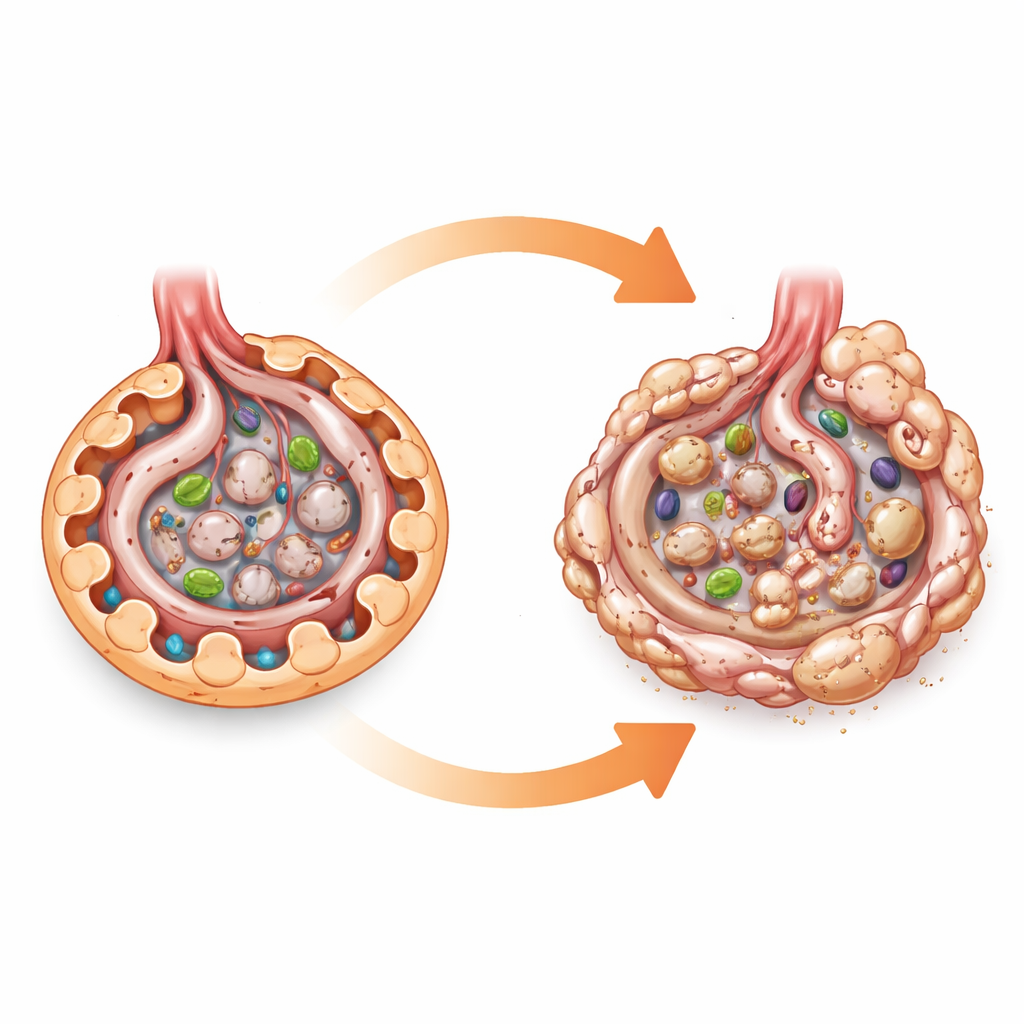
显微镜下的细胞燃料计
可以把AMPK看作细胞的燃料计。当能量不足时,它会启动燃烧脂肪与糖的过程,并支持诸如自噬等清理系统,帮助细胞回收老化的成分。由于糖尿病使肾脏细胞暴露于过量的糖和营养物,许多研究者假定AMPK活性下降会直接损害足细胞并推动糖尿病性肾病。大部分这一观点来自细胞培养研究和使用可激活AMPK的药物处理的动物实验,而这些药物可能有许多其他作用。为更清晰地检验AMPK的作用,作者构建了仅在足细胞中同时缺失两种主要AMPK亚基的小鼠,而身体其他部位的AMPK保持完整。
缺失AMPK的肾脏出人意料地正常
当这些基因工程小鼠在普通饮食下随访两年时,它们的肾脏在外观和功能上与正常同窝小鼠几乎无异。足细胞数量得以保留,肾小球的精细结构保持完整,尿液检测未见过量蛋白外漏。即使是AMPK已知会影响的关键过程——例如称为mTORC1的生长通路和细胞内部的回收系统——在这些足细胞中也未见明显异常。这表明在健康且营养充足的状态下,足细胞可以在不依赖AMPK的情况下维持功能,可能是借助执行类似任务的备用通路。
糖尿病揭示出潜在脆弱点
当采用类似1型的模型和一种结合高脂与低剂量毒素以模拟部分2型特征的模型诱导糖尿病时,情况明显改变。在相同的高血糖水平下,缺失足细胞AMPK的小鼠比正常糖尿病小鼠出现更严重的肾损伤。它们的肾小球更大、更瘢痕化,尿中白蛋白外漏更多,这是肾损伤的关键临床信号。详细染色显示肾小球中胶原和“应激”蛋白沉积更多,指向肾小球纤维化的加速——即细嫩的滤过组织逐渐被僵硬的瘢痕取代。
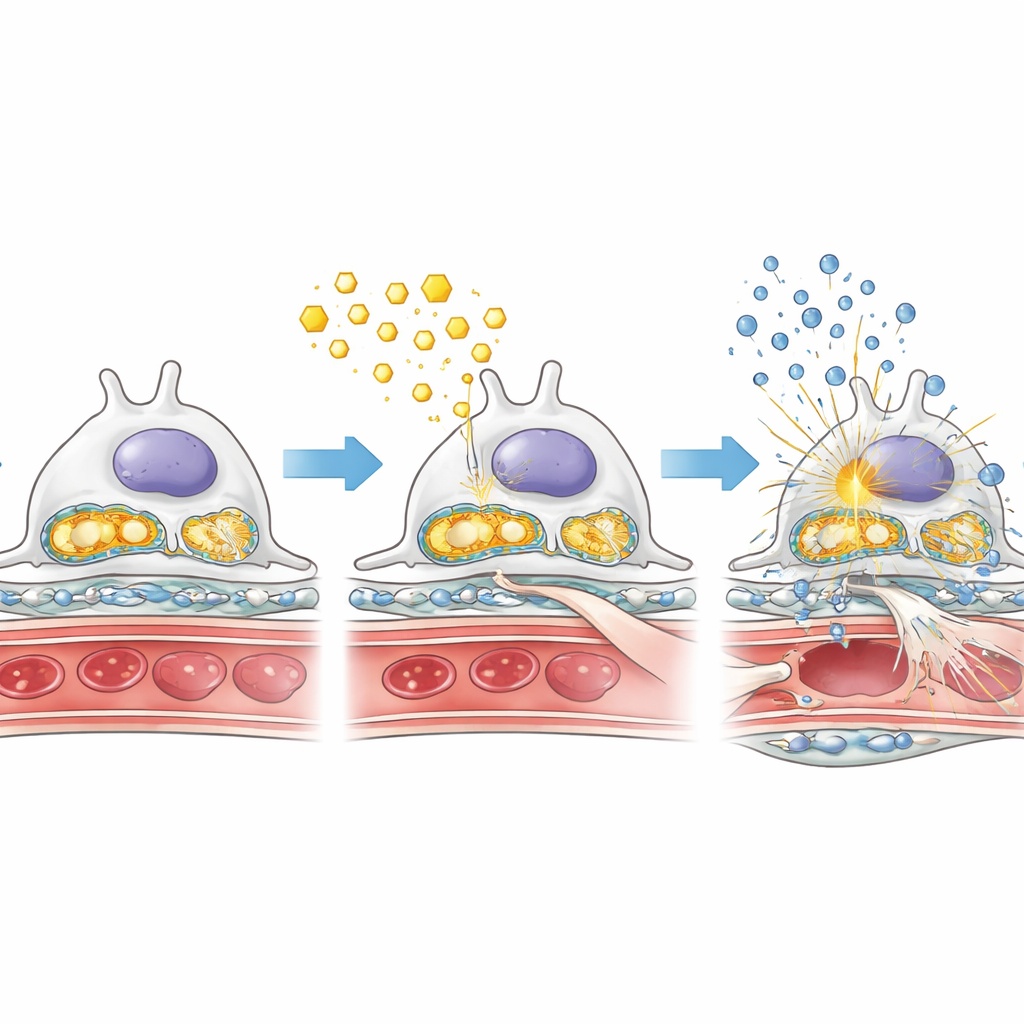
脂肪过载、受损的能量工厂与炎性警报
为了解为何缺失AMPK会加剧损伤,研究者仔细观察了糖尿病条件下足细胞如何处理脂肪和糖。在缺失足细胞AMPK的糖尿病小鼠中,肾小球内堆积了脂滴,而用于燃烧脂肪的关键酶水平降低。与此同时,驱动快速糖分解的酶更为活跃,暗示代谢向一种效率较低、更像“发酵”的方式转变,这种转变可能有利于纤维化。细胞的能量工厂——线粒体也受到影响:其维持蛋白减少,线粒体遗传物质渗入细胞质。泄漏的线粒体DNA似乎触发了一种被称为cGAS–STING的内在报警系统,进而激活诸如NF-κB之类的炎症开关并增加炎性分子产生。这些变化共同在肾脏滤过部位内部形成脂肪过载、线粒体损伤和慢性炎症的有毒组合。
从足细胞向邻近细胞的涟漪效应
足细胞并非孤立工作;它们直接位于肾小球内皮细胞对面,后者衬在滤过结构的血液侧。研究发现,在糖尿病中缺失足细胞AMPK时,这些相邻的内皮细胞更容易采取类似成纤维细胞的状态,这一过程被称为内皮向间质转化。在这种状态下,它们更积极地参与瘢痕形成。这些内皮细胞表现出与足细胞相同的代谢特征:燃烧脂肪的能力下降,更多依赖糖酵解。这表明受压的足细胞可间接推动邻近细胞走向有害行为,从而在整个肾小球中放大纤维化。
对糖尿病患者意味着什么
在日常情况下,足细胞似乎能够在很大程度上不依赖AMPK而工作。但在糖尿病的慢性压力下,正常足细胞中残留的AMPK活性成为一种默默的守护者,帮助它们正确燃烧脂肪、保护线粒体并抑制炎性报警。当这一安全网被移除时,脂肪和糖的处理紊乱,线粒体崩溃,炎性通路被激活,瘢痕在肾滤过结构中扩散开来。这些发现支持这样的观点:温和增强AMPK活性或模拟其对代谢和炎症的保护作用的疗法,可能有助于减缓或预防糖尿病性肾病——通过增强足细胞及其邻近细胞的抗逆性,而不仅仅是单靠改变血糖水平。
引用: Srivastava, S.P., Kopasz-Gemmen, O., Kunamneni, A. et al. AMPK is dispensable for physiological podocyte and glomerular functions but prevents glomerular fibrosis in experimental diabetes. Cell Death Discov. 12, 204 (2026). https://doi.org/10.1038/s41420-026-03078-y
关键词: 糖尿病性肾脏病, 足细胞, AMPK, 肾小球纤维化, 细胞代谢