Clear Sky Science · es
AMPK es prescindible para las funciones fisiológicas de los podocitos y del glomérulo pero evita la fibrosis glomerular en la diabetes experimental
Por qué importan las células filtrantes del riñón en la diabetes
Nuestros riñones filtran la sangre miles de veces al día de forma discreta, y una parte clave de ese filtro está formada por células llamadas podocitos. Estas células envuelven pequeños vasos sanguíneos en estructuras conocidas como glomérulos, reteniendo las proteínas en la sangre mientras permiten que los desechos y el agua pasen a la orina. Este estudio plantea una pregunta aparentemente simple con grandes implicaciones para las personas con diabetes: ¿protege realmente un interruptor energético celular importante, llamado AMPK, a estas células filtrantes y previene la cicatrización del riñón? La respuesta resulta ser sutil: AMPK no es necesaria para la función renal cotidiana, pero se vuelve crucial cuando la diabetes somete al sistema a estrés.
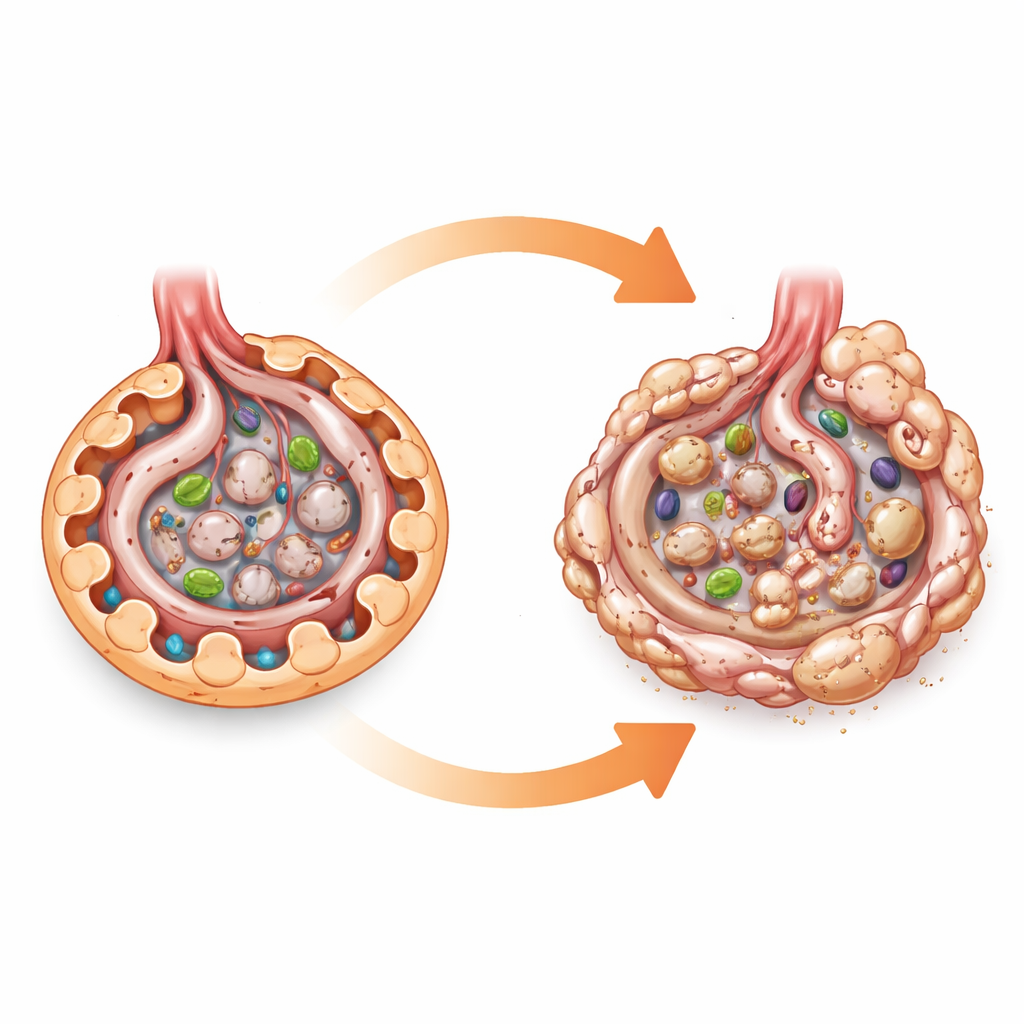
Un indicador de combustible celular bajo el microscopio
Se puede pensar en AMPK como un indicador de combustible celular. Cuando la energía es baja, activa procesos que queman grasa y azúcar y apoya sistemas de limpieza como la autofagia, que ayuda a las células a reciclar componentes desgastados. Dado que la diabetes sobrecarga a las células renales con azúcar y nutrientes, muchos investigadores han supuesto que una caída de la actividad de AMPK daña directamente a los podocitos y propicia la enfermedad renal diabética. Gran parte de esa creencia provino de estudios en cultivo celular y de animales tratados con fármacos que activan AMPK, los cuales pueden tener muchos efectos adicionales. Para probar el papel de AMPK de forma más nítida, los autores diseñaron ratones que carecían de ambas subunidades principales de AMPK específicamente en los podocitos, manteniendo AMPK intacta en el resto del organismo.
Riñones sorprendentemente normales en ausencia de AMPK
Cuando se siguió a estos ratones modificados durante dos años con una dieta normal, sus riñones parecían y funcionaban igual que los de sus crías normales. Se conservaron el número de podocitos, la estructura fina de los glomérulos permaneció intacta y las pruebas de orina no mostraron fuga excesiva de proteínas. Incluso procesos clave que se sabe que AMPK influye —como una vía de crecimiento llamada mTORC1 y el sistema interno de reciclaje celular— no parecían alterados de forma evidente en estos podocitos. Esto sugiere que en un estado sano y bien nutrido, los podocitos pueden mantener su función sin depender de AMPK, quizá apoyándose en vías alternativas que realizan trabajos similares.
La diabetes revela debilidades ocultas
El panorama cambió de forma pronunciada cuando se indujo la diabetes, empleando tanto un modelo similar a la tipo 1 como un modelo combinado de dieta alta en grasas y dosis bajas de toxina que imita aspectos de la diabetes tipo 2. Con los mismos niveles altos de glucosa en sangre, los ratones sin AMPK en podocitos desarrollaron una lesión renal más grave que los ratones diabéticos normales. Sus glomérulos eran más grandes y estaban más cicatrizados, y filtraban más albúmina a la orina, un signo clínico clave de daño renal. Tinciones detalladas mostraron una mayor acumulación de colágeno y proteínas de “estrés” en los glomérulos, lo que apunta a una aceleración de la fibrosis glomerular: la sustitución progresiva del delicado tejido filtrante por tejido rígido cicatricial.
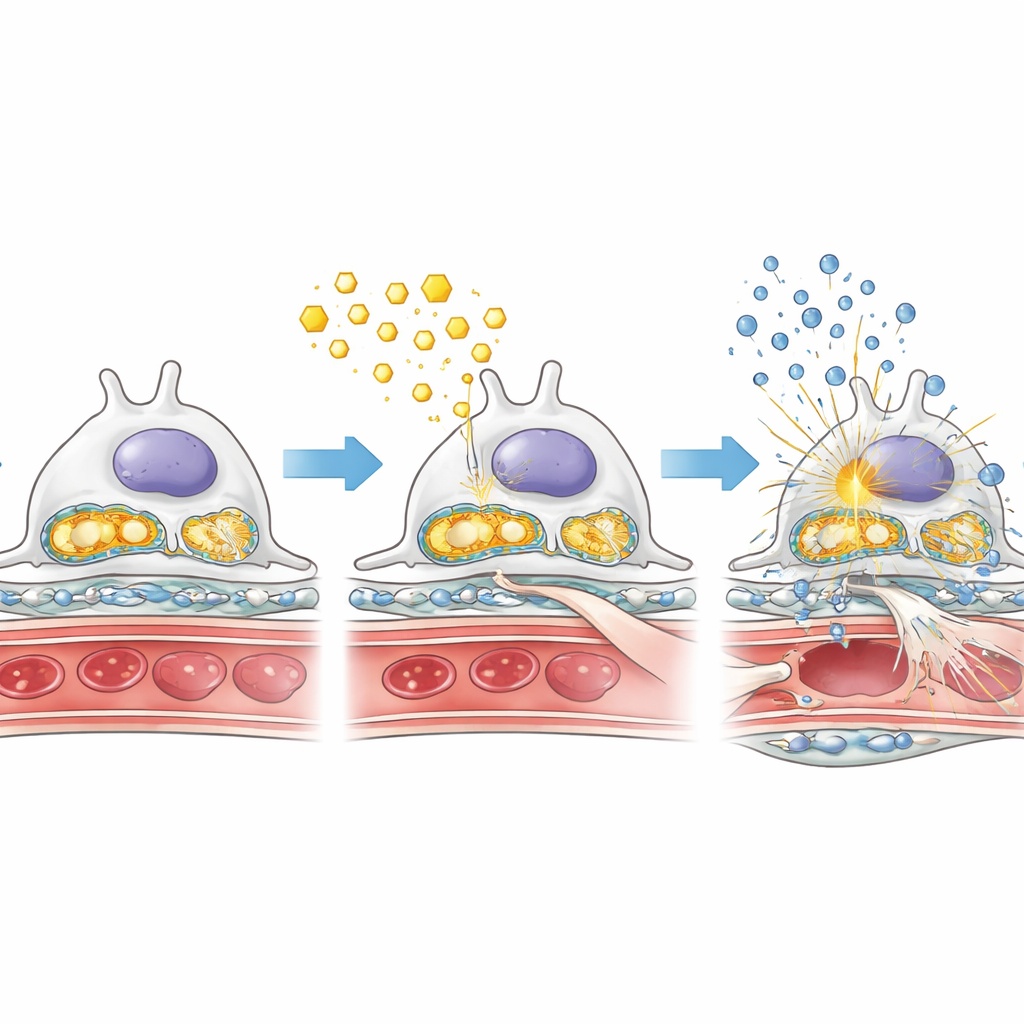
Sobrecarga de grasa, mitocondrias dañadas y alarmas inflamatorias
Para entender por qué la falta de AMPK agravó el daño, los investigadores examinaron de cerca cómo los podocitos manejaban grasas y azúcares en condiciones diabéticas. En los ratones diabéticos sin AMPK en podocitos, los glomérulos acumulaban gotas de grasa, mientras que una enzima clave para quemar ácidos grasos estaba reducida. Al mismo tiempo, las enzimas que impulsan la descomposición rápida de azúcares eran más activas, lo que sugiere un cambio hacia un metabolismo menos eficiente y más “fermentativo” que puede favorecer la cicatrización. Las fábricas de energía celular —las mitocondrias— también se vieron afectadas: sus proteínas de soporte estaban reducidas y su material genético se filtró al citosol. Este ADN mitocondrial filtrado parece activar un sistema de alarma interna conocido como vía cGAS–STING, que a su vez enciende interruptores inflamatorios como NF‑κB e incrementa la producción de moléculas proinflamatorias. En conjunto, estos cambios generan una mezcla tóxica de sobrecarga de grasas, daño mitocondrial e inflamación crónica dentro del filtro renal.
Ondas desde los podocitos hacia las células vecinas
Los podocitos no trabajan aisladamente; se sitúan justo enfrente de las células endoteliales glomerulares, que recubren el lado sanguíneo del filtro. El estudio encontró que cuando faltaba AMPK en los podocitos durante la diabetes, estas células endoteliales vecinas eran más propensas a adoptar un estado similar al de los fibroblastos, un proceso llamado transición endotelial‑a‑mesenquimal. En ese estado contribuyen de forma más activa a la formación de cicatrices. Estas células endoteliales mostraron las mismas firmas metabólicas observadas en los podocitos: menor capacidad para quemar grasa y mayor dependencia de la glucólisis. Esto sugiere que los podocitos estresados pueden empujar indirectamente a las células vecinas hacia comportamientos dañinos, amplificando la fibrosis en todo el glomérulo.
Qué significa esto para las personas con diabetes
En la vida cotidiana, los podocitos parecen poder funcionar sin mucha ayuda de AMPK. Pero bajo el estrés crónico de la diabetes, la actividad residual de AMPK en los podocitos normales actúa como una defensora silenciosa, ayudándoles a quemar grasa correctamente, proteger sus mitocondrias y mantener las alarmas inflamatorias bajo control. Cuando se retira esa red de seguridad, el manejo de grasas y azúcares se descompensa, las mitocondrias se deterioran, las vías inflamatorias se encienden y la cicatrización se extiende por el filtro renal. Estos hallazgos respaldan la idea de que terapias que incrementen suavemente la actividad de AMPK, o que imiten sus efectos protectores sobre el metabolismo y la inflamación, podrían ayudar a frenar o prevenir la enfermedad renal diabética —reforzando la resiliencia de los podocitos y sus vecinos cercanos en lugar de cambiar solo la glucemia—.
Cita: Srivastava, S.P., Kopasz-Gemmen, O., Kunamneni, A. et al. AMPK is dispensable for physiological podocyte and glomerular functions but prevents glomerular fibrosis in experimental diabetes. Cell Death Discov. 12, 204 (2026). https://doi.org/10.1038/s41420-026-03078-y
Palabras clave: enfermedad renal diabética, podocitos, AMPK, fibrosis glomerular, metabolismo celular