Clear Sky Science · tr
AMPK, fizyolojik podosit ve glomerüler işlevler için gereksizdir ancak deneysel diyabette glomerüler fibrozisi önler
Diyabette böbrek filtre hücrelerinin önemi
Böbreklerimiz günde binlerce kez kanı sessizce süzer ve bu filtrenin önemli bir parçası podosit adı verilen hücrelerden oluşur. Bu hücreler glomerul adı verilen yapılar içindeki küçük kılcal damarların etrafını sarar, proteinleri kanda tutarken atık ve suyun idrara geçmesine izin verir. Bu çalışma, diyabetli insanlar için büyük çıkarımları olan, aldatıcı derecede basit görünen bir soruyu soruyor: hücrelerdeki önemli bir enerji algılayıcısı olan AMPK gerçekten bu filtre hücrelerini koruyor ve böbrekte skarlaşmayı engelliyor mu? Cevap ince bir ayrıntı gösteriyor—AMPK günlük böbrek işlevi için gerekli değil, ancak diyabet sistemi zorladığında hayati hale geliyor.
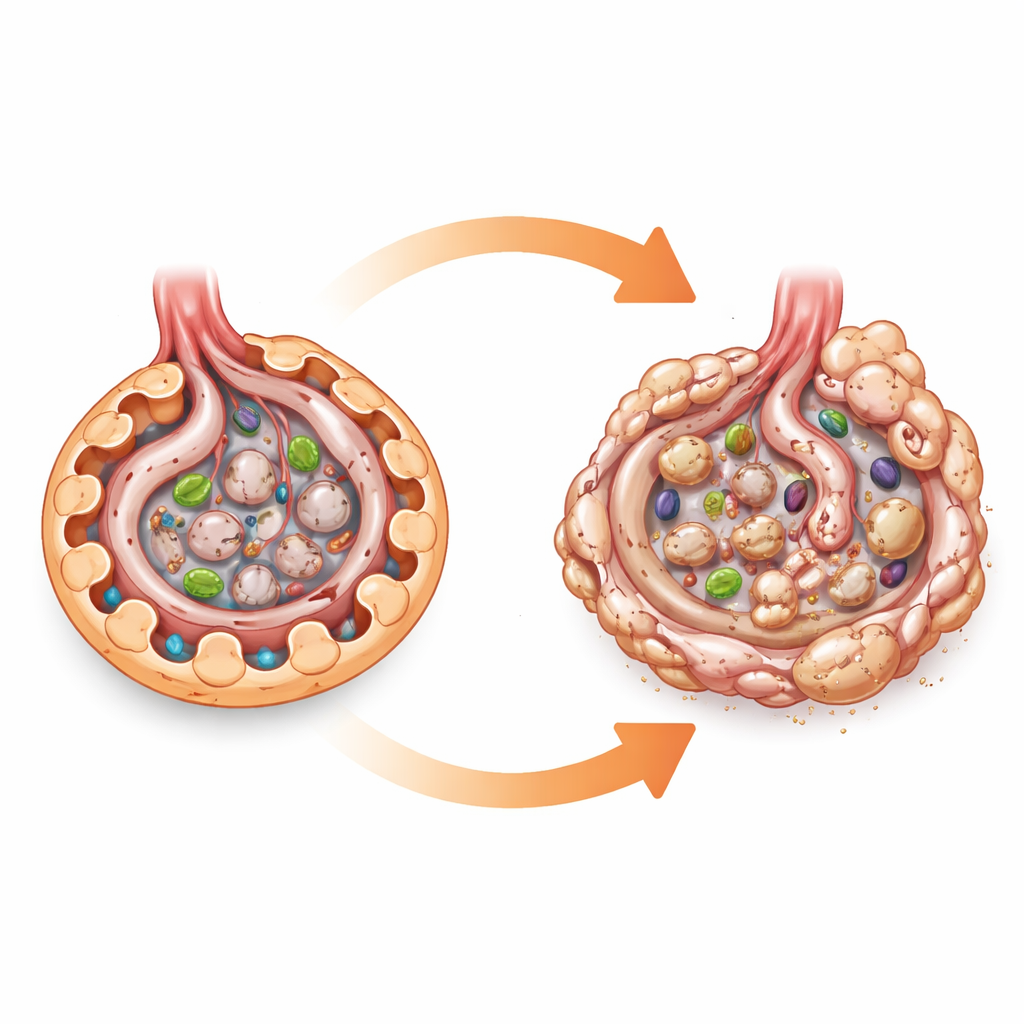
Mikroskop altında hücresel bir yakıt göstergesi
AMPK, hücresel bir yakıt göstergesi olarak düşünülebilir. Enerji düşük olduğunda yağ ve şekeri yakma süreçlerini açar ve otofaji gibi hücrelerin eski bileşenleri geri dönüştürmesine yardımcı olan temizlik sistemlerini destekler. Diyabet böbrek hücrelerini şeker ve besinlerle aşırı yüklediği için birçok araştırmacı AMPK aktivitesindeki düşüşün doğrudan podositlere zarar verdiğini ve diyabetik böbrek hastalığını tetiklediğini varsaymıştır. Bu inancın çoğu hücre kültürü çalışmaları ve AMPK’yi aktive eden ilaçlarla yapılan hayvan çalışmalarına dayanıyordu; bu ilaçların başka birçok etkisi olabilir. AMPK’nin rolünü daha temiz şekilde test etmek için yazarlar, AMPK’nin iki ana alt birimini özel olarak podositlerde ortadan kaldıran, geri kalan vücutta AMPK’yi koruyan fareler mühendislediler.
AMPK yokluğunda şaşırtıcı derecede normal böbrekler
Bu tasarlanmış fareler normal bir diyette iki yıl boyunca izlendiğinde, böbrekleri normal kardeşleriyle aynı görünümde ve işlevdeydi. Podosit sayısı korundu, glomerüllerin ince yapısı sağlam kaldı ve idrar testleri aşırı protein kaçağı göstermedi. AMPK’nin etkilediği bilinen ana süreçler—örneğin mTORC1 olarak adlandırılan büyüme yolu ve hücrenin iç geri dönüştürme sistemi—bu podositlerde belirgin şekilde bozulmamıştı. Bu, sağlıklı ve iyi beslenmiş bir durumda podositlerin AMPK’ye güvenmeden görevlerini sürdürebildiğini, muhtemelen benzer işleri yapan yedek yolaklara dayanarak yapabildiğini düşündürüyor.
Diyabet gizli zayıflıkları açığa çıkarıyor
Diyabet, tip 1’e benzer bir model ve tip 2 diyabetin bazı yönlerini taklit eden yüksek yağlı, düşük doz toksin kombinasyonlu model kullanılarak indüklendiğinde tablo keskin şekilde değişti. Aynı yüksek kan şekeri düzeyleri altında, podositlerinde AMPK eksik olan fareler normal diyabetik farelerden daha ağır böbrek hasarı geliştirdi. Glomerülleri daha büyük ve daha skarlıydı ve idrarda daha fazla albümin sızdırıyorlardı; bu böbrek hasarının önemli bir klinik işaretidir. Ayrıntılı boyamalar glomerüllerde kollajen ve “stres” proteinlerinin daha yoğun birikimini gösterdi ve bu da glomerüler fibrozun—nazik filtrasyon dokusunun sert skarla yer değiştirmesinin—hızlandığına işaret ediyordu.
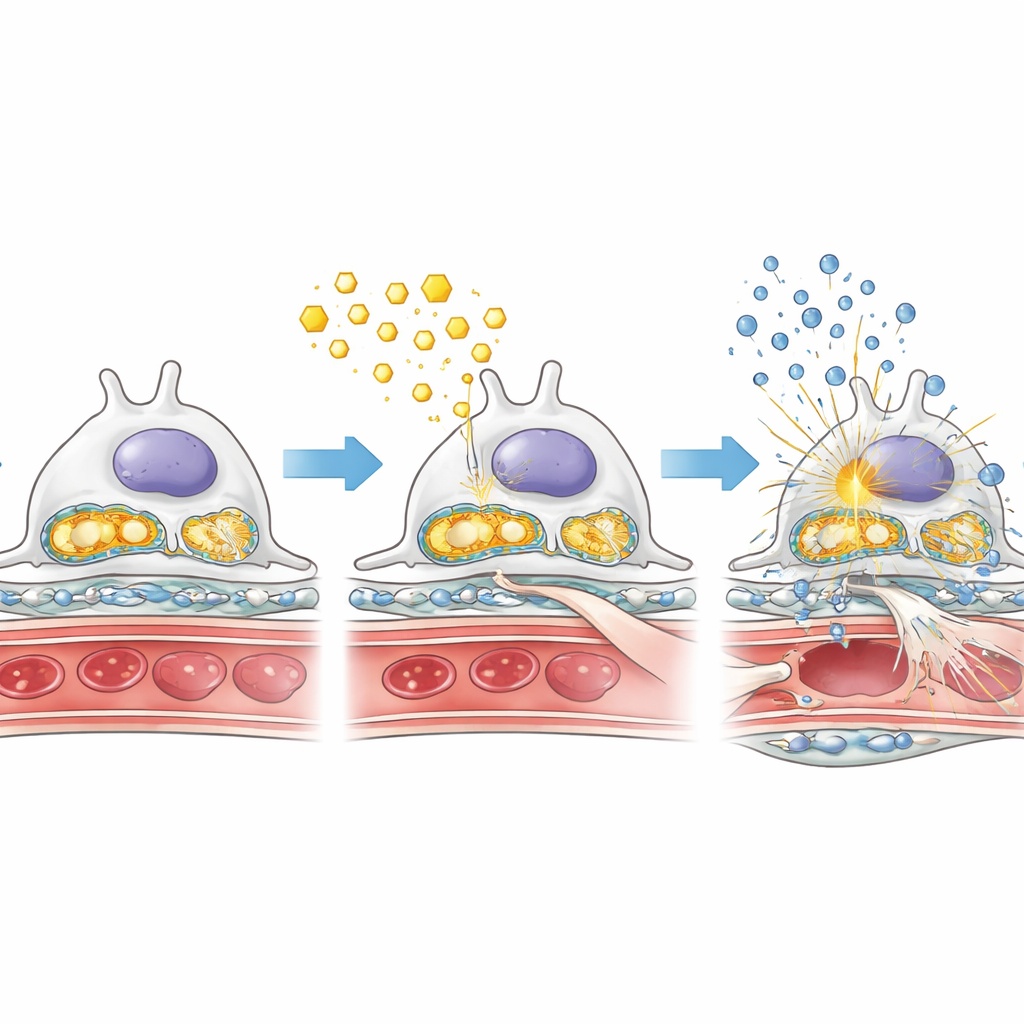
Yağ yükü, zarar görmüş enerji santralleri ve inflamatuar alarmlar
AMPK eksikliğinin hasarı neden kötüleştirdiğini anlamak için araştırmacılar diyabetik koşullar altında podositlerin yağ ve şekeri nasıl işlediğine yakından baktılar. Podositlerinde AMPK olmayan diyabetik farelerde glomerüller içinde yağ damlacıkları birikti, yağ asitlerini yakmada kritik bir enzim azalmıştı. Aynı zamanda hızlı şeker yıkımını yönlendiren enzimler daha aktifti; bu da skarlaşmayı kolaylaştırabilecek daha az verimli, daha “fermantatif” bir metabolizmaya kayışa işaret ediyordu. Hücrenin enerji fabrikaları olan mitokondriler de etkilendi: destek proteinleri daha düşüktü ve mitokondriyal genetik materyal hücre sıvısına sızdı. Bu sızan mitokondriyal DNA, cGAS–STING olarak bilinen iç bir alarm sistemini tetikliyor gibi görünüyor; bu yol da NF‑κB gibi inflamatuar anahtarları etkinleştiriyor ve inflamatuar molekül üretimini artırıyordu. Birlikte bu değişiklikler böbrek filtresi içinde yağ yükü, mitokondri hasarı ve kronik enflamasyonun toksik bir karışımını yaratıyor.
Podositlerden komşu hücrelere yayılan etkiler
Podositler izole çalışmaz; filtrenin kan tarafını döşeyen glomerüler endotel hücrelerinin tam karşısında otururlar. Çalışma, diyabette podosit AMPK’si eksik olduğunda bu komşu endotel hücrelerin fibroblast‑benzeri bir durumu benimseme olasılığının arttığını buldu; bu süreç endotelden mezenşimal geçiş olarak adlandırılır. Bu durumda skar oluşumuna daha aktif katkıda bulunurlar. Bu endotel hücreleri podositlerde görülen aynı metabolik imzaları gösteriyordu: yağı yakma kapasiteleri azalmış ve glikolize daha fazla bağımlı hale gelmişlerdi. Bu, stres altındaki podositlerin dolaylı olarak komşu hücreleri zararlı davranışlara itebileceğini ve tüm glomerul boyunca fibrozisi güçlendirebileceğini gösteriyor.
Diyabetli insanlar için anlamı
Günlük yaşamda podositler büyük ölçüde AMPK’den çok yardım almadan işlev gösterebiliyor gibi görünüyor. Ancak diyabetin kronik stresi altında, normal podositlerde kalan AMPK aktivitesi sessiz bir savunmacı haline geliyor; doğru şekilde yağ yakmalarına, mitokondrilerini korumalarına ve inflamatuar alarmları kontrol altında tutmalarına yardımcı oluyor. Bu güvenlik ağı kaldırıldığında, yağ ve şeker işlenmesi bozuluyor, mitokondriler çözüyor, inflamatuar yollar alevleniyor ve skarlaşma böbrek filtresi boyunca yayılıyor. Bu bulgular, AMPK aktivitesini nazikçe artıran veya metabolizma ve inflamasyon üzerindeki koruyucu etkilerini taklit eden tedavilerin diyabetik böbrek hastalığını yavaşlatmaya veya önlemeye yardımcı olabileceği fikrini destekliyor—kan şekerini değiştirmekten ziyade podositlerin ve yakın komşularının dayanıklılığını güçlendirerek.
Atıf: Srivastava, S.P., Kopasz-Gemmen, O., Kunamneni, A. et al. AMPK is dispensable for physiological podocyte and glomerular functions but prevents glomerular fibrosis in experimental diabetes. Cell Death Discov. 12, 204 (2026). https://doi.org/10.1038/s41420-026-03078-y
Anahtar kelimeler: diyabetik böbrek hastalığı, podositler, AMPK, glomerüler fibroz, hücresel metabolizma